Что будет если мужчине пить дюфастон
Влияние гипотензивной терапии на половую функцию мужчин
Широкое распространение артериальной гипертензии (АГ) и отчетливая тенденция к развитию этого заболевания у лиц более молодого возраста послужили поводом к изучению качества жизни и состояния половой функции у данной категории больных.
Широкое распространение артериальной гипертензии (АГ) и отчетливая тенденция к развитию этого заболевания у лиц более молодого возраста послужили поводом к изучению качества жизни и состояния половой функции у данной категории больных.
В то же время арсенал антигипертензивных средств, широко используемых в повседневной практике врачами различных специальностей, необычайно разнообразен. Однако при выборе конкретного препарата врачи нередко ориентируются на собственный опыт, а также побочные эффекты и противопоказания к его назначению. При этом в меньшей степени учитывается влияние антигипертензивных средств на показатели липидного и углеводного метаболизма, а также их воздействие на функциональное состояние различных систем организма, в том числе системы гипофиз-гонады. Развитие у лиц молодого возраста таких побочных эффектов, как снижение потенции, приводит не только к прекращению приема антигипертензивного препарата, но и к формированию стойкого негативного отношения больного к лечению. В связи с этим исследование влияния основных групп антигипертензивных препаратов, а именно блокаторов β-адренорецепторов (ББ), ингибиторов АПФ и блокаторов кальциевых каналов (БКК), на гонадостат больных АГ представляется важным.
Для решения поставленных задач были обследованы 125 мужчин с АГ в возрасте от 38 до 55 лет. Все пациенты на момент обследования и ранее (не менее чем в течение 2 мес) не получали гипотензивной терапии и имели АГ, по классификации ВНОАК-ВНОК, соответствующую I–II степени заболевания. Уровень систолического артериального давления (АД) у больных до включения в исследование колебался от 140 до 180 мм рт. ст., диастолического АД — от 90 до 110 мм рт. ст.
Все мужчины проходили общеклиническое, эндокринологическое, кардиологическое и андрологическое обследования.
Состояние углеводного обмена оценивали по результатам стандартного глюкозотолерантного теста при пероральной нагрузке глюкозой из расчета 1,75 г/кг массы тела, но не более 75 г. Уровень гликемии определялся в капиллярной крови глюкозо-оксидазным методом.
Пациентам с АГ проводилось суточное мониторирование ЭКГ по Холтеру. Больным, у которых выявлялись ишемические изменения (29 человек), назначалась терапия ББ — метопролол по 50 мг 2 раза в сутки. Всем остальным мужчинам с АГ назначалась терапия БКК (нифедипин ретард 40 мг/сут) или ингибиторами АПФ (эналаприл 20 мг/сут). Эта группа пациентов была разделена на две подгруппы — в зависимости от наличия отягощенной наследственности по АГ (АГ у родителей, диагностированная в возрасте до 60 лет с уровнем АД > 160/90 мм рт. ст., или хроническое использование ими гипотензивных препаратов). В нашем исследовании 27 человек имели отягощенную наследственность по АГ, у 35 человек наследственность была не отягощена, у 24 пациентов установить ее наличие было невозможно, и эти пациенты исключались из исследования.
Забор крови для обследования гормонального статуса (определение уровней свободного тестостерона (Тсв), дегидроэпиандростерона-сульфата (ДГЭАс), эстрадиола, кортизола, пролактина, лютеинизирующего гормона, фолликулостимулирующего гормона) проводился между 8.30 и 9.30 утра после 10-часового голодания. Образцы крови центрифугировались, и полученная сыворотка замораживалась при температуре –20°С. Определение уровней гормонов в крови производилось с помощью стандартизированных ВОЗ реагентов радиоиммунологическим и иммуноферментным методами на коммерческих наборах фирм Алкор Био (Россия) и DSL (США) до назначения лечения и на 30-й день терапии (+ 3 дня).
Для оценки влияния гипотензивной терапии на половую функцию мужчин с АГ использовалась шкала международного индекса эректильной функции (МИЭФ-15) [19].
Из исследования были исключены больные с признаками застойной сердечной недостаточности, сахарным диабетом, нарушением толерантности к глюкозе, а также имеющие заболевания желудочно-кишечного тракта в стадии обострения, признаки хронической почечной недостаточности, а также те пациенты, изменение веса которых за период наблюдения составило более 1,5 кг. В исследование не были включены пациенты с выраженным ожирением (с индексом массы тела > 35 кг/м 2 ). Контрольную группу составили 15 здоровых мужчин того же возраста, без вредных привычек с неотягощенной наследственностью по АГ и сахарному диабету.
Полученные в ходе исследования данные обрабатывались с помощью пакета прикладных программ Statistica (StatSoft, США). Сравниваемые группы имели нормальное распределение, что оценивалось с помощью теста Шапиро–Уилка. Статистическую значимость различий оценивали по t-тесту Стьюдента для независимых выборок. Уровень значимости p
Н. В. Иванов
СПбМАПО, Санкт-Петербург
Заместительная гормональная терапия для мужчин с возрастным андрогенным дефицитом
Специализация: урология, андрология
Синдром возрастного андрогенодефицита у мужчин — это нарушение биохимического баланса, возникающее в зрелом возрасте по причине недостаточности андрогенов в сыворотке крови, нередко сопровождающейся снижением чувствительности организма к андрогенам. Как правило, это приводит к значительному ухудшению качества жизни и неблагоприятно сказывается на функциях практически всех систем организма. Естественно, что огромный интерес вызывают вопросы терапии андрогенного дефицита, поскольку именно она ставит сложную задачу перед врачом-клиницистом: выбрать из широкого арсенала методов и препаратов гормональной терапии наиболее оптимальный, сочетающий в себе качество, эффективность, а также удобство в применении.
В настоящее время врачи-урологи и андрологи наиболее часто применяют заместительную терапию тестостероном. Данный метод позволяет решить целый ряд задач: снизить симптомы возрастного андрогенодефицита путем повышения либидо, общей сексуальной удовлетворенности, уменьшить выраженность либо полностью ликвидировать вегетососудистые и психические расстройства. Кроме того, если заместительная терапия тестостероном применяется более 1 года, у пациентов наблюдается повышение плотности костной массы, снижение выраженности висцерального ожирения, а также нарастание мышечной массы. Также после длительного курса лечения нормализуются лабораторные параметры: наблюдается повышение уровня гемоглобина или количества эритроцитов, снижение уровня ЛПОНП (липопротеинов очень низкой плотности) и ЛПНП (липопротеинов низкой плотности) при неизмененном уровне ЛПВП (липопротеинов высокой плотности). Многие авторы считают, что такого эффекта можно достичь, добившись восстановления концентрации тестостерона в крови до нормального уровня (10–35 нмоль/л). Следует также учитывать, что *17α-алкилированные препараты тестостерона флуоксиместеролон и метилтестостерон обладают выраженной гепатотоксичностью, оказывая токсическое и канцерогенное влияние на печень, а также отрицательно воздействуют на липидный спектр крови (резкое повышение уровня атерогенных и снижение уровня антиатерогенных липопротеидов). Поэтому применение этих производных тестостерона в клинической практике было прекращено.
В настоящее время из пероральных препаратов предпочтение отдается тестостерону ундеканоату (Андриол). Указанный эфир тестостерона не подвергается первичному печеночному метаболизму, так как всасывается в лимфатическую систему, минуя печень. После гидролиза тестостерона ундеканоата в лимфатической системе в системный кровоток поступает тестостерон, который оказывает лечебное действие как сам по себе, так и через свои основные метаболиты – дигидротестостерон (ДГТ) и эстрадиол, обусловливающие полный спектр андрогенной активности тестостерона. Таким образом, тестостерона ундеканоат сохраняет свою активность при пероральном применении. Вместе с этим, минуя систему воротной вены и прохождение через печень, тестостерона ундеканоат не оказывает гепатотоксического и гепатоканцерогенного действия. Период полувыведения препарата из плазмы составляет 3–4 часа. В связи с этим режимом дозировки тестостерона ундеканоата является 2-кратный прием в течение суток, это не всегда удобно для пациентов. Исходя из собственного опыта, мы считаем, что Андриол является достаточно мягким препаратом и помогает только в случаях начальных и минимальных проявлений возрастного андрогенного дефицита.
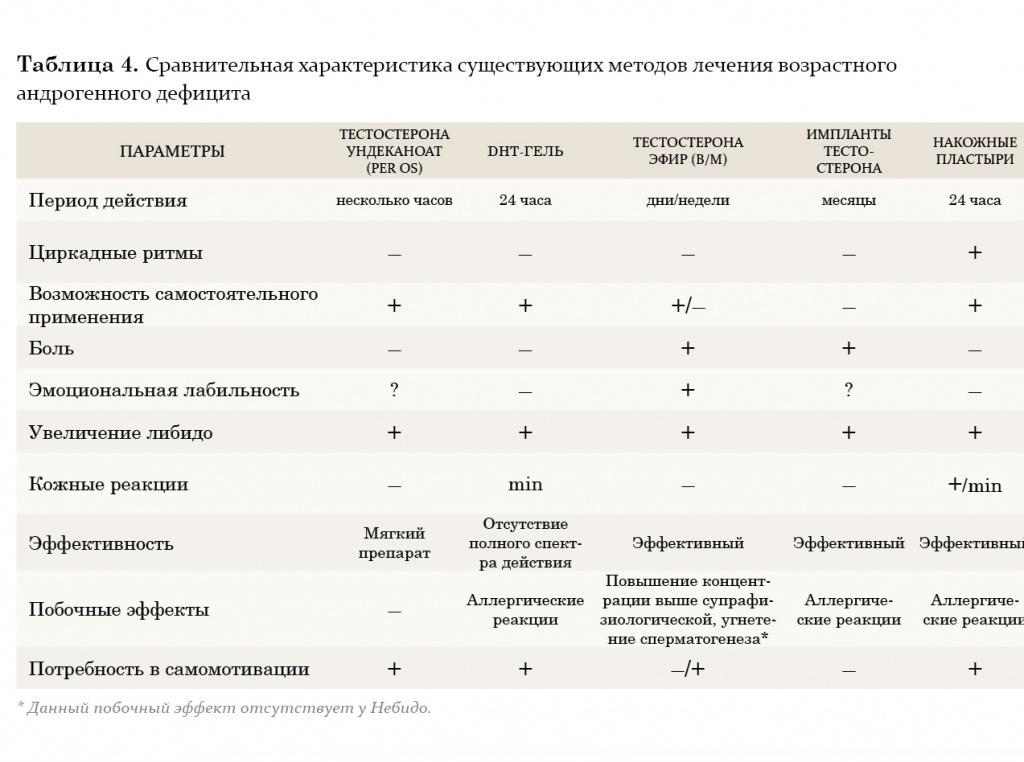
Внутримышечные инъекции пролонгированных эфиров тестостерона также являются широко применяемым методом заместительной терапии у мужчин с гипогонадизмом. Два наиболее известных эфира тестостерона – тестостерона ципионат и тестостерона энантат, имеют похожую фармакокинетику. При внутримышечном введении этих препаратов создается депо, из которого препарат высвобождается в кровеносное русло. В течение первых 2–3 дней после введения уровень тестостерона повышается до супрафизиологических цифр, а затем медленно снижается на протяжении последующих 2 недель до субнормальных значений. Положительной стороной этих препаратов является длительность терапевтического действия. Тем не менее резкие изменения в уровне тестостерона, зачастую ощущаемые самим пациентом в виде подъемов и снижения либидо, общего самочувствия, эмоционального статуса, являются нежелательными качествами данных препаратов. В связи с этим большие надежды возлагаются на новый препарат Небидо (Шеринг), фармакокинетика которого значительно отличается от других эфиров тестостерона. Небидо представляет собой тестостерона ундеканоат и является препаратом, не обладающим пиком повышения концентрации.
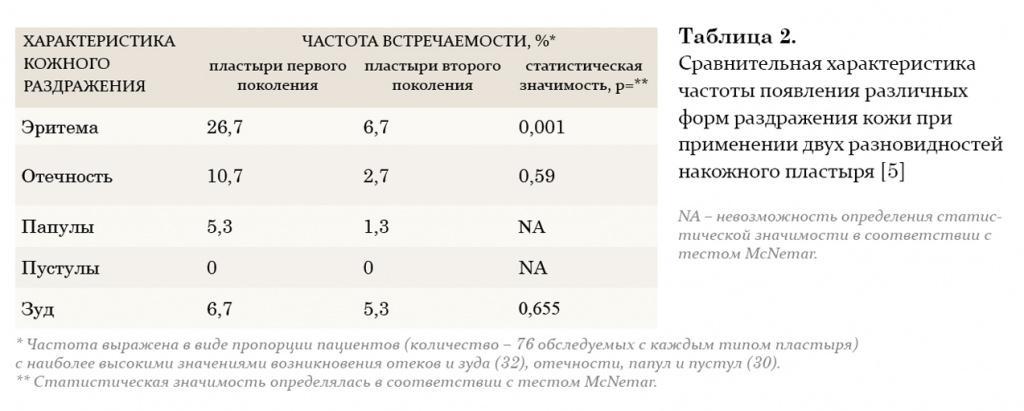
На протяжении двух последних десятилетий большое внимание уделяется исследованию преимуществ трансдермального применения препаратов тестостерона. Мошоночные пластыри обладают эффективным действием, и некоторые пациенты считают их наиболее удобным методом лечения. Накожные пластыри наиболее хорошо воспринимаются пациентами и дают эффективный уровень тестостерона в сыворотке крови. Тем не менее существуют некоторые различия между этими двумя разновидностями пластырей относительно их аллергогенного потенциала: при применении накожных пластырей отмечается гораздо большая частота возникновения аллергических реакций и раздражения кожи, чем при применении мошоночных пластырей.
Гель тестостерона обладает всеми преимуществами пластырей и не вызывает развития кожных реакций. Единственный его недостаток заключается в наличии возможности контакта геля с партнершей и недостаточном количестве долговременных исследований по его применению.
Трансдермальный путь введения тестостерона позволяет избежать его первичного метаболизма в печени и инактивации, как это происходит при применении пероральных андрогенных препаратов, а также позволяет имитировать циркадные ритмы высвобождения физиологического немодифицированного тестостерона и его естественных метаболитов, эстрадиола и ДГТ. К тому же терапию с использованием пластырей и геля в случае необходимости можно легко прервать. К положительным моментам этого метода лечения также относится низкий риск возникновения лекарственной зависимости.
Европейский препарат 5-α-дигидротестостерон-гель (ДГТ) хотя и признан эффективным, однако неизвестно, оказывает ли изолированное применение неароматизированного андрогена, каким является ДГТ, такое же действие, как тестостерон, в связи с тем, что метаболиты тестостерона включают эстрадиол. По мнению многих авторов, применение препарата не рекомендуется, так как ДГТ вследствие невозможности превращения в эстрадиол не обладает полным спектром терапевтических свойств тестостерона (например, влиянием на костную ткань и сердечно-сосудистую систему).
Некоторые из препаратов заместительной терапии, такие как тестостерона ундеканоат, ДГТ-гель и мошоночные пластыри, вызывают существенное увеличение концентрации ДГТ в сыворотке крови. ДГТ известен как главный андроген простаты, и в связи с этим проводилось много дискуссий по поводу способности его вызывать заболевания предстательной железы. Однако, несмотря на эти предположения, в последнее 10-летие не зафиксировано данных в пользу увеличения частоты возникновения патологии простаты при назначении препаратов ДГТ.
Таким образом, существует множество препаратов заместительной андрогенотерапии, однако все они имеют те или иные побочные эффекты, а также обладают угнетающим действием на сперматогенез. В последнее время появляется все больше работ, демонстрирующих вторичный характер возрастного андрогенного дефицита. Согласно материалам ВОЗ, получены данные о сохранении секретирующей функции клетками Лейдига у пожилых мужчин, что позволило ученым предложить принципиально новый подход в лечении возрастного андрогенного дефицита, основанный на стимуляции синтеза эндогенного тестостерона.
Однако не стоит забывать, что наряду с абсолютными противопоказаниями для заместительной терапии андрогенами (рак грудной и предстательной желез) существуют и дополнительные (доброкачественная гиперплазия предстательной железы с выраженной обструкцией, пролактинома, полицитемия). К относительным противопоказаниям относятся нарушения сна в виде апноэ, обструктивные заболевания легких, интенсивное курение.
К побочным эффектам андрогенов относятся усиление ночного апноэ, полицитемия, гинекомастия, приапизм, задержка жидкости, повышение АД, отеки, увеличение размеров простаты, торможение сперматогенеза.
То есть сегодня существуют методы лечения возрастного андрогенного дефицита, которые можно разделить на две группы, принципиально различающиеся по механизму действия:
заместительная терапия экзогенными андрогенными препаратами; терапия, стимулирующая синтез эндогенного тестостерона.
Таким образом, можно сказать, что оптимального для всех средства для лечения возрастного андрогенного дефицита у мужчин не существует. И к выбору препарата следует подходить строго индивидуально, учитывая возраст пациента, индекс массы тела, необходимость сохранения сперматогенеза, показатели гематокрита и сопутствующие заболевания.
Дюфастон®
Инструкция
Торговое название
Международное непатентованное название
Лекарственная форма
Таблетки, покрытые пленочной оболочкой, 10 мг
Состав
Одна таблетка содержит
активное вещество: дидрогестерон 10 мг,
вспомогательные вещества: лактозы моногидрат, метилоксипропилцеллюлоза, крахмал кукурузный, кремния диоксид безводный коллоидный, магния стеарат,
оболочка: Opadry белый Y-1-7000 (титана диоксид (Е-171), метилгидроксипропилцеллюлоза, полиэтиленгликоль).
Описание
Круглые, двояковыпуклые таблетки, покрытые пленочной оболочкой белого цвета, со скошенными краями на одной стороне, с надписью «155» слева и справа от риски на другой стороне таблетки.
Фармакотерапевтическая группа
Половые гормоны. Прогестагены. Производные прегнадиена. Дидрогестерон.
Фармакологические свойства
Фармакокинетика
Абсорбция. После приема внутрь дидрогестерон быстро всасывается из желудочно-кишечного тракта. Время достижения максимальной концентрации (Tmax) от 0.5 до 2.5 часов. Абсолютная биодоступность дидрогестерона при дозе 20 мг внутрь (при сравнении с 7.8 мг внутривенно) составляет 28%.
В таблице приведены средние значения фармакокинетических параметров дидрогестерона (Д) и дигидродидрогестерона (ДГД) после многократного приема дидрогестерона внутрь в дозе 10 мг.
Дидрогестерон 10 мг
*: из расчета AUC (0-tau)/24
Распределение. При стабильной концентрации дидрогестерона при внутривенном введении объем распределения около 1400 л. Дидрогестерон и ДГД связываются с протеинами плазмы крови более чем на 90%.
Метаболизм. После приема внутрь дидрогестерон быстро метаболизируется в ДГД. Концентрация основного метаболита 20-α-дигидродидрогестерона (ДГД) достигает пика примерно через 1.5 часа после приема дозы. Концентрация ДГД в плазме крови значительно выше, чем дидрогестерона. Отношения AUC (площади под кривой) и Cmax (максимальной концентрации) ДГД и дидрогестерона составляют примерно 40 и 25, соответственно. Периоды полувыведения дидрогестерона и ДГД в среднем 5–7 часов и 14–17 часов, соответственно. Основной особенностью всех метаболитов дидрогестерона является присутствие 4,6-диен-3-1 конфигурации исходного соединения и отсутствие 17-α-гидроксилирования. Это объясняет отсутствие эстрогенного и андрогенного эффектов дидрогестерона.
Выведение. После приема внутрь меченого дидрогестерона в среднем 63% дозы выводится с мочой. Общий клиренс плазмы 6,4 л/мин. Полное выведение дидрогестерона происходит через 72 часа. ДГД выводится с мочой преимущественно в форме конъюгата глюкуроновой кислоты.
Зависимость от дозы и времени. Фармакокинетика линейна как при однократном, так и многократном дозировании в интервале от 2.5 до 10 мг. Сравнение кинетики однократной и многократных доз показывает, что параметры фармакокинетики Д и ДГД не изменяются в результате повторного приема дозы. Стабильная концентрация достигается после 3 дней лечения.
Фармакодинамика
Дюфастон® не подавляет овуляцию. Вследствие этого остается возможность зачатия у женщин репродуктивного возраста, принимающих Дюфастон®.
У женщин в постменопаузе с не удаленной маткой ЗГТ эстрогенами повышает риск гиперплазии и рака эндометрия. Добавление прогестагена предупреждает повышение этого риска.
Показания к применению
— нарушение менструального цикла
— бесплодие вследствие лютеиновой недостаточности
— угрожающий аборт по причине недостаточности прогестерона
— привычное невынашивание беременности по причине недостаточности прогестерона
При терапии эстрогенами у женщин с интактной маткой может быть использован в циклическом режиме при следующих состояниях:
— для предотвращения гиперплазии эндометрия в период постменопаузы
— дисфункциональные маточные кровотечения
Способ применения и дозы
Предлагаемые режимы приема можно корректировать в зависимости от тяжести состояния и индивидуальной реакции на лечение.
Нерегулярные менструации – по 1 таблетке (10 мг) в день с 11-го по 25-й день. Возможно достижение регулярного 28-дневного цикла.
Дисменорея – по 1-2 таблетке (10-20 мг) в день с 5-го по 25-й день цикла. Дозу свыше 1 таблетки в день разделить на несколько приемов в течение дня. Лечение следует начинать с наивысшей дозы. Лечение продолжать на протяжении 6 месяцев непрерывно.
Бесплодие вследствие лютеиновой недостаточности – по 1 таблетке (10 мг) в день с 14-го по 25-й день цикла. Лечение продолжать непрерывно, в течение минимум 6 последовательных циклов. При наступлении беременности лечение рекомендуется продолжать в течение первых месяцев по схеме, рекомендованной при привычном аборте.
Угрожающий аборт по причине недостаточности прогестерона – начальная доза: 4 таблетки (40 мг) однократно, затем по 1 таблетке (10 мг) через каждые 8 часов до исчезновения симптомов. Лечение следует начинать с наивысшей дозы. При продолжении или рецидиве симптомов во время лечения дозу следует повышать на 1 таблетку (10 мг) каждые 8 часов. Лечение продолжать в эффективной дозе в течение 1 недели после исчезновения симптомов; затем постепенно снижать. При последующем рецидиве симптомов лечение продолжить приемом эффективной дозы, достигнутой ранее.
Привычное невынашивание беременности по причине недостаточности прогестерона – по 1 таблетке (10 мг) в день до 20-й недели беременности; затем дозу можно постепенно снизить. Лечение следует начать до зачатия. При возникновении симптомов угрожающего аборта лечение продолжить соответственно данному показанию.
Дисфункциональные маточные кровотечения
Последующее интенсивное кровотечение можно предупредить посредством назначения с профилактической целью 1 таблетки (10 мг) в день с 11-го по 25-й дни цикла, при необходимости в комбинации с эстрогенами, на протяжении 2-3 циклов. После этого лечение можно прекратить, чтобы убедиться в восстановлении регулярности циклов.
Вторичная аменорея – по 1-2 таблетки (10-20 мг) в день с 11-го по 25-й день цикла для достижения секреторной трансформации эндометрия в результате адекватной стимуляции эндогенными или экзогенными эстрогенами.
Комбинированная терапия эстрогенами и прогестагенами следует проводить при использовании минимальной эффективной дозы гормонов и на протяжении наиболее краткого курса, сопоставимого с целями лечения и рисками для каждой женщины, при регулярной переоценке рисков и преимуществ.
Предменструальный синдром – по 1 таблетке (10 мг) 2 раза в день с 11-го по 25-й день цикла.
Дети и подростки младше 18 лет: Нет соответствующих данных по использованию дидрогестерона до менархе.
Безопасность и эффективность дидрогестерона у подростков в возрасте 12-18 лет не установлена.
Для перорального применения. При назначении более высоких доз таблетки следует принимать в несколько приемов в течение дня.
Побочные действия
Нежелательные побочные реакции, о которых сообщалось наиболее часто во время клинических испытаний у пациенток при использовании дидрогестерона по показаниям без применения эстрогена, были следующими: метроррагия, болезненность/чувствительность молочных желез, мигрень/головная боль.
Следующие нежелательные побочные реакции (с указанием их частоты) наблюдались во время клинических испытаний при использовании дидрогестерона (n=3483) по показаниям без применения эстрогена и были сообщены спонтанно.
Румянцева, md
Предлагаю разобраться с двумя препаратами, которые назначаются в акушерской и гинекологической практике невероятно часто: Дюфастон и Утрожестан. Что это за препараты? Кто-то считает их неэффективными (и безобидными), другие боятся, как огня, а третьи считают их спасением практически от любой болезни в женском организме.
Итак, по сути, Дюфастон и Утрожестан – это препараты прогестерона:
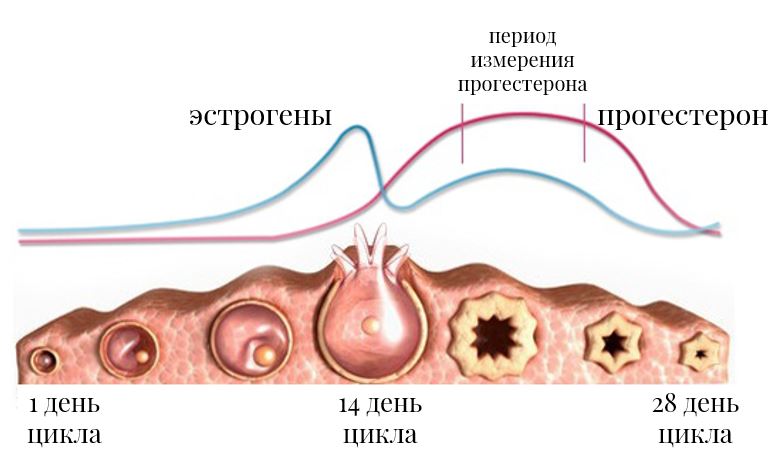
Прогестерон – это гормон второй фазы цикла и гормон беременности. Он вырабатывается желтым телом в яичнике после овуляции (подготавливая организм женщины к принятию оплодотворенной яйцеклетки в случае беременности), а также плацентой далее во время беременности.
Показания к применению Дюфастона и Утрожестана
В показаниях (из инструкции) к приему этих препаратов указано, что приниматься они должны при недостаточной выработке собственного прогестерона (а это обязательно доказать во время обследования женщины!) у женщин в следующих ситуациях:
Подчеркну еще раз, что даже в инструкциях к Дюфастону и Утрожестану указано, что назначаться они могут/ должны при прогестероновой недостаточности в вышеперечисленных случаях, а не всем подряд женщинам с бесплодием/ нерегулярным циклом/ выкидышем.
Давайте попробуем разобраться, что же известно о применении препаратов прогестерона при различных заболеваниях/состояниях/вмешательствах.
Синдром предменструального напряжения (ПМС)
Применение препаратов прогестерона при ПМС (от которого страдают, кстати, 5% женщин, а не каждая первая дама) обсуждается, так как симптомы ПМС возникают перед менструацией, когда в организме женщины «главенствует» именно этот гормон.
Справедливости ради стоит отметить, что до конца не ясно, являются ли тяжелые проявления ПМС результатом высокого уровня прогестерона в организме или, наоборот, снижения уровня прогестерона, предшествующего наступлению менструации. Несмотря на множество спорных моментов как в определении самого ПМС, так и в понимании его механизмов, попытки применения препаратов прогестерона предпринимались неоднократно, а их результаты неплохо освещены в научной литературе.
Что же мы имеем на сегодняшний день? Только в одном исследовании был показан положительный эффект от применения препаратов прогестерона во вторую фазу цикла у женщин с ПМС, однако эффект оценивали исключительно по субъективным ощущениям участниц. Остальные исследования, посвященные этой теме, либо недостаточно хороши, чтобы учитывать их результаты, либо не показали никакого эффекта от применения препаратов прогестерона в разных формах (внутрь или вагинально) при ПМС.
Вывод: На сегодняшний день применение препаратов прогестерона при ПМС не может считаться научно обоснованным.
Маточные кровотечения
Маточные кровотечения – нередкая проблема для женщин репродуктивного возраста. Существуют разнообразные подходы к лечению данной проблемы, причиной которой могут быть разнообразные заболевания. Для остановки маточного кровотечения могут применяться схемы от таблеток до операции по удалению матки. Применение препаратов прогестерона в данном случае имеет логичное обоснование: прогестерон является гормоном второй фазы цикла, он отвечает за изменения, происходящие в это время в эндометрии (внутренней выстилке матки), и за «удерживание» эндометрия на своем месте (перед менструацией уровень прогестерона падает, запускается механизм кровотечения). Таким образом, попытка поддержани высоких уровней прогестерона у женщин с маточными кровотечениями выглядит вполне оправданной. Что же говорят исследования? Действительно, есть эффект от применения препаратов прогестерона в таблетках, однако другие методы лечения (в частности, спираль с левонргестрелом) обладают гораздо более выраженным эффектом и значительно в большей мере улучшают качество жизни данных пациенток. Как это ни печально, но наиболее эффективным методом лечения остается операция по удалению матки. И все же спирали, содержащие левоноргестрел, должны быть испробованы до принятия решения о хирургическом лечении.
Вывод: Препараты прогестерона в таблетках могут давать положительный эффект у пациенток с маточными кровотечениями, однако существуют гораздо более эффективные способы лечения, которым и должно отдаваться предпочтение.
Нарушения менструального цикла
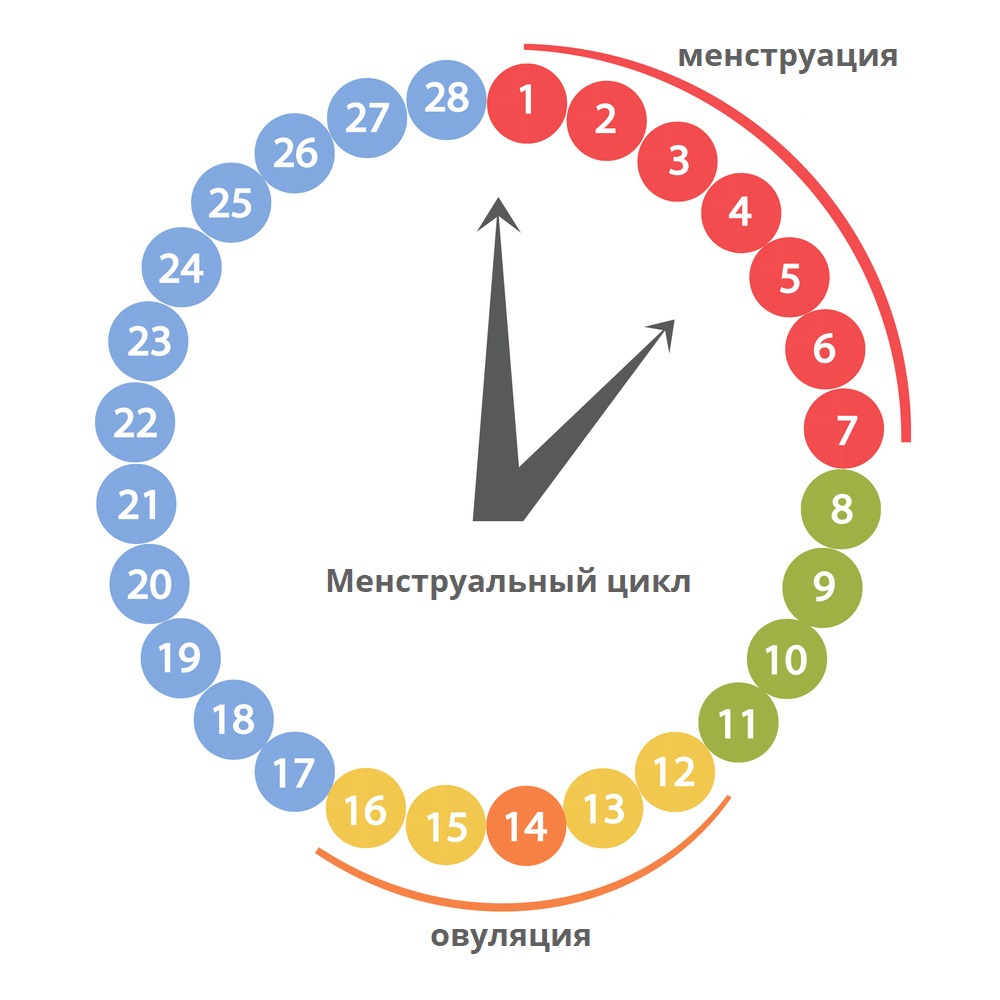
1. Если у женщины идеально работает первая фаза цикла
Если у женщины идеально работает первая фаза цикла (растет доминантный фолликул, утолщается эндометрий, и т.д.), далее происходит овуляция, а желтое тело работает недостаточно эффективно и не вырабатывает адекватного уровня прогестерона, вторая фаза оказывается неполноценной, а менструация наступает в разное время (так как важнейшим сигналом к наступлению менструации служит снижение уровня прогестерона после его пика во вторую фазу).
Самое подходящее решение проблемы в такой ситуации – назначение препаратов прогестерона на вторую фазу цикла (с 16го по 25ый день цикла). Перед назначением препаратов прогестерона следует оценить гормоны первой фазы, сделать УЗИ (чаще всего в динамике несколько раз), чтобы увидеть, что имеется доминантный фолликул, а затем желтое тело (признак прошедшей овуляции), а затем сдать кровь для определения уровня прогестерона.
И если с гормонами первой фазы все хорошо, по УЗИ отклонений не выявлено, а прогестерон после овуляции низкий, тогда имеет смысл назначать препараты прогестерона. Все логично и правильно, но надо учитывать один фактор: именно такая проблема встречается казуистически редко.
2. Если проблемы в цикле связаны с нарушением в первую фазу
Если проблемы в цикле связаны с нарушением в первую фазу и требуется стимуляция овуляции, препараты прогестерона тоже могут пригодиться (сначала принимаются препараты для стимуляции овуляции, потом по УЗИ отслеживается наступление овуляции, и только потом могут назначаться препараты прогестерона).
В такой ситуации при грамотной и эффективной стимуляции овуляции уровень прогестерона может быть и нормальным, т.е. препараты прогестерона могут не потребоваться. Однако чаще всего они назначаются профилактически, чтобы не перепроверять уровень прогестерона в каждом цикле после стимуляции овуляции и не «упускать» ни одного цикла для попыток зачатия в процессе стимуляции.
А что происходит, если назначать прогестерон, не установив причину нарушения цикла?
Чаще всего к низкому уровню прогестерона приводит именно отсутствие овуляции и проблемы в первой фазе цикла (причин для которых множество), а не изолированные нарушения второй фазы. Что же будет происходить у таких пациенток, если препараты прогестерона им назначать неправильно?
Классическая ситуация: имеем пациентку с нарушением цикла, сдаем анализ на прогестерон во вторую фазу, видим низкий прогестерон, назначаем прогестерон извне, чтобы его повысить! Логично? Нет. У такой пациентки чаще всего нет овуляции, нет желтого тела, не сформирован эндометрий! Что же мы делаем, назначая прогестерон? «Обманываем» организм, показывая ему, что все в порядке, желтое тело есть, прогестерон вырабатывается. Организм даже не пытается бросить все свои ресурсы на то, чтобы добиться овуляции: есть прогестерон – овуляция уже прошла, можно расслабиться. То есть назначая прогестерон по стандартной схеме (с 16го по 25ый день цикла) женщине с нерегулярным циклом, мы с определенной вероятностью мешаем наступлению у нее овуляции (без прогестерона организм «борется за овуляцию» до последнего; овуляция могла бы произойти и на 20-ый, и на 30-ый день цикла, если бы мы не вмешались прогестероном).
Что же происходит с циклом? Женщина принимает прогестерон до 25го дня цикла, далее препарат отменяется, организм улавливает сигнал о снижении уровня прогестерона в крови и запускает механизм начала менструации. Из женщины с нерегулярным циклом мы получаем женщину с регулярным циклом. Если цель лечения – предсказуемость жизни женщины и регулярный цикл, такой подход может применяться. Если цель лечения – нормализация работы яичников и зачатие ребенка, препараты прогестерона могут назначаться только после подтверждения наличия овуляции в каждом цикле.
Чтобы не совершать таких ошибок, необходимо внимательно отследить, что происходит с циклом у женщины с нерегулярными менструациями (гормоны первой фазы, УЗИ в динамике, прогестерон во вторую фазу, если есть овуляция), и только после постановки диагноза принимать решение о назначении/неназначении любых гормональных препаратов.
Вывод: Препараты прогестерона нужны либо женщинам с полностью сохранной первой фазой цикла и овуляцией, но низким уровнем прогестерона после овуляции (что наблюдается крайне редко), либо женщинам с нарушениями первой фазы после стимуляции овуляции (под строгим контролем овуляции по УЗИ).
Поддержка второй фазы цикла при ЭКО
Как уже неоднократно упоминалось, прогестерон – гормон второй фазы цикла. После овуляции в яичнике формируется желтое тело, которое и вырабатывает прогестерон, который, в свою очередь, готовит эндометрий (внутреннюю выстилку матки) к имплантации оплодотворенной яйцеклетки.
Женщинам, идущим на ЭКО, требуется медикаментозная поддержка второй фазы цикла либо из-за исходно имеющихся проблем с циклом, либо из-за неадекватной выработки собственного прогестерона после стимуляции первой фазы цикла. В этой ситуации препараты прогестерона нужны и важны, но есть принципиальные моменты в их назначении:
Назначение препаратов прогестерона для поддержания второй фазы цикла в рамках программы ЭКО действительно увеличивает вероятность наступления и прогрессирования беременности и рождения здорового малыша, однако даже в этой ситуации есть нерешенные моменты, и исследования, посвященные другим способам поддержки второй фазы цикла, продолжаются.
Вывод: Препараты прогестерона в таблетках могут применяться для поддержания второй фазы цикла в рамках программ ЭКО, но только после установления факта овуляции.
Заместительная гормональная терапия
Заместительная гормональная терапия (ЗГТ) проводится в тех случаях, когда у женщины не вырабатываются достаточные уровни собственных гормонов (в менопаузе (менопаузальная гормональная терапия) или после хирургического вмешательства). В таких ситуациях логично «воссоздание» собственного цикла путем введения соответствующих гормонов в первую и вторую фазу цикла.
Препараты прогестерона (в комбинации с препаратами эстрогенов, имитирующих первую фазу цикла) могут рассматриваться для этих целей, однако в современном мире есть множество комбинированных препаратов для ЗГТ (содержащих и эстрогеновый, и прогестиновый компонент), которым и отдается предпочтение в подобных ситуациях.
Вывод: Дюфастон/ Утрожестан могут применяться в сочетании с эстрогенами для заместительной гормональной терапии, однако они не являются препаратами выбора.
Эндометриоз
С эндометриозом все просто и сложно одновременно. Сложность в том, что причины и механизмы его возникновения изучены недостаточно, есть много теорий и дискуссий на этот счет. Простота в том, что мы рассматриваем это заболевание в контексте применения двух препаратов (Дюфастон и Утрожестан), эффективность которых в лечении данного заболевания не доказана.
Гормональная терапия может применяться для лечения эндометриоза, однако должны рассматриваться другие препараты, подробнее об этом можно прочитать здесь.
Вывод: Препараты прогестерона не должны применяться для лечения эндометриоза.
Профилактика выкидыша
Опять же, учитывая, что прогестерон – гормон беременности, совершенно логично попытаться сохранить беременность у женщины, по той или иной причине отнесенной в группу риска (в России в группу риска (чаще всего незаслуженно) попадают женщины с предыдущей потерей беременности, тянущими болями внизу живота на ранних сроках, «тонусом» по УЗИ в первом триместре, и т.д.).
А теперь сюрприз для многих: препараты прогестерона не способствуют профилактике самопроизвольного прерывания беременности в первом и втором триместре!
Другими словами, если беременность сохранилась на фоне Дюфастона, она сохранилась бы и без него, и наоборот (если беременность прервалась без Дюфастона, она прервалась бы и с этим препаратом)! Причем нет разницы, в каком виде принимается прогестерон: внутрь в виде таблеток, вагинально в свечах или внутримышечно.
Хочу сразу оговориться: в некоторых случаях при привычном невынашивании беременности препараты прогестерона снижают вероятность выкидыша, но это относится только к тем женщинам, которые ранее перенесли 3 и более потерь беременности подряд.
Вывод: Препараты прогестерона в таблетках, свечах и уколах не должны назначаться с целью профилактики выкидыша на ранних сроках беременности.
Лечение угрожающего выкидыша
Угрозой выкидыша считается наличие кровянистых выделений при закрытой шейке матки в сроке беременности до 20 недель. При начавшемся раскрытии шейки матки в этом сроке сохранение беременности любыми препаратами крайне маловероятно. Подчеркну, что тянущие боли внизу живота, а также «тонус» матки по УЗИ не являются признаками угрожающего выкидыша.
Лечение угрозы прерывания беременности возможно только после проведения УЗИ, которое подтвердит, что плод:
Лечение должно проводиться в стационаре под наблюдением врача.
В этой ситуации препараты прогестерона оказываются эффективными и помогают снизить частоту самопроизвольного прерывания беременности, однако большинство исследований в этой области оценивали эффективность прогестерона, вводимого внутримышечно, а не в виде таблеток или свечей (так как женщина находится в стационаре).
Вывод: Препараты прогестерона снижают вероятность выкидыша при наличии угрозы выкидыша (кровянистые выделения – основной признак. ), однако данных об эффективности этих препаратов в виде таблеток или свечей недостаточно.
Лечение преждевременных родов
Преждевременные роды – это роды, произошедшие до 37 недель беременности. Преждевременные роды могу приводить к тяжелейшим последствиям, в частности, смерти ребенка или тяжелым отдаленным последствиям для здоровья малыша. Именно поэтому вопросу изучения способов лечения (или остановки начавшихся) преждевременных родов посвящено огромное количество исследований.
Прогестерон – ключевой «гормон беременности», а потому логичными выглядят попытки его применения у женщины, роды которой начались слишком рано.
Стандартным вариантом лечения преждевременных родов считается применение токолитиков (препаратов, расслабляющих мускулатуру матки и останавливающих/ослабляющих начавшиеся схватки). В ряде исследований были осуществлены попытки применения препаратов прогестерона для лечения преждевременных родов совместно с токолитиками или без них. Несмотря на то, что в отдельных исследованиях был обнаружен эффект от применения прогестерона у женщин с начавшимися преждевременными родами (ослабление схваток, замедление процесса укорочения шейки матки), для включения этой группы препаратов в стандартные протоколы ведения женщин с преждевременными родами, данных все еще недостаточно. И тем более нельзя говорить о том, что препараты данной группы могут заменить стандартную токолитическую терапию при преждевременных родах.
Вывод: Препараты прогестерона могут добавлять положительный эффект у женщин с начавшимися преждевременными родами, однако они не могут заменять стандартного лечения, а также не должны применяться в виде таблеток или свечей (то есть тех форм, которые обсуждаются в данной статье).
Профилактика преждевременных родов при одноплодной беременности у женщин групп риска
Могут ли препараты прогестерона предотвратить наступление преждевременных родов у женщин, относящихся к группе риска (т.е. у женщин, уже перенесших преждевременные роды ранее или у женщин с укорочением шейки матки по УЗИ).
Опять же, прогестерон, будучи гормоном беременности, должен помогать пролонгированию беременности и препятствовать началу схваток.
Результаты многих исследований подтверждают эту гипотезу и демонстрируют, что профилактическое назначение прогестерона на поздних сроках беременности женщинам группы риска действительно снижает вероятность преждевременных родов, мертворождений и других негативных последствий для плода. Справедливости ради стоит отметить, что все эти данные получены для инъекций прогестерона или пессариев, содержащих прогестерон (устройство, вводимое во влагалище женщины, и выделяющее нужный препарат). Таблетки и свечи в этом разрезе изучены недостаточно.
Вывод: Препараты прогестерона действительно помогают снизить вероятность преждевременных родов у женщин группы риска, но доказанной эффективностью обладают инъекции и пессарии. Таблетки и свечи изучены недостаточно.
Профилактика преждевременных родов при многоплодной беременности
Примерно половина женщин, вынашивающих двойню, родит своих малышей раньше срока (т.е. ранее 37 недель беременности). При тройнях и большем количестве плодов этот риск еще выше. Преждевременные роды несут в себе опасность для жизни и здоровья ребенка, а потому вопросам их профилактики, в том числе, при многоплодных беременностях, посвящены многие исследования.
Учитывая, что прогестерон – основной гормон беременности, логично предположить, что его применение позволит продлить беременность и улучшить исходы для ребенка. Однако имеющиеся исследования, посвященные применению прогестерона в виде уколов или свечей (таблетки в этом аспекте изучены плохо), не выявили каких-либо плюсов для мамы и ребенка. Другими словами, на сегодняшний день нет оснований назначать профилактически препараты прогестерона женщинам с многоплодной беременностью.
Вывод: Препараты прогестерона в свечах и уколах не помогают в профилактике преждевременных родов у женщин с многоплодной беременностью. Таблетки в этом аспекте изучены плохо.
Преэклампсия
Преэклампсия – это серьезное осложнение беременности, характеризующееся высоким уровнем артериального давления, протеинурией (белок в моче) и отеками. Преэклампсия встречается у 2 — 8% беременных женщин. При этом состоянии поражаются кровеносные сосуды в различных органах, в том числе, в плаценте, что, в свою очередь, может приводить к задержке роста плода и преждевременным родам. У самой женщины страдают чаще всего почки, печень, головной мозг, а также система свертывания крови.
Как и в случае со многими другими осложнениями беременности, точного понимания механизмов и причин возникновения преэклампсии нет, поэтому недостаток прогестерона рассматривается как одна из (впрочем, не самая вероятная) причина развития перечисленных нарушений.
Исследований, посвященных применению препаратов прогестерона для профилактики и лечения преэклампсии, немного (суммарно они включают около 1500 женщин), но ни в одном из них не продемонстрировано убедительных данных в пользу применения прогестерона. В международные рекомендации по профилактике и лечению преэклампсии эти препараты также не входят.
Вывод: На сегодняшний день применение препаратов прогестерона для лечения и профилактики преэклампсии не может считаться оправданным.
Подводим итоги
Когда же могут назначаться препараты прогестерона, которые обсуждаются в этой статье (Дюфастон, Утрожестан)?
Препараты прогестерона могут применяться для профилактики и лечения преждевременных родов, а также для лечения угрозы выкидыша, но не в форме свечей и таблеток.
И еще пара замечаний.
Препараты прогестерона нельзя назвать безвредными и безобидными. У них довольно много побочных эффектов, к наиболее частым из которых относятся:
И последний крайне важный аспект!
Ни в коем случае нельзя назначать и отменять препараты прогестерона самостоятельно.
Это может привести к серьезным последствиям для организма, в частности, во время беременности. Если после прочтения этой статьи у вас возникли сомнения, насколько оправдано применение указанных препаратов в вашей ситуации, обязательно обсудите ваши сомнения с лечащим врачом и отменяйте препараты только под контролем врача.