Глюкоза в моче у ребенка что это
Глюкоза в моче у ребенка что это
Исследование мочи с помощью тест-полосок. Тест-полоски с реагентами, окраска которых зависит от концентрации определяемого вещества, ныне повсеместно применяются при анализе мочи. Есть тест-полоски для определения рН, удельного веса, присутствия крови, концентрации белка, кетоновых тел, глюкозы, нитритов, лейкоцитарной эстеразы и уробилиногена.
Точность определения у них разная, а результаты могут искажаться даже под действием часто присутствующих в моче веществ и других факторов. Тест-полоски широко используют благодаря их дешевизне и быстроте анализа, однако результаты следует истолковывать осторожно.
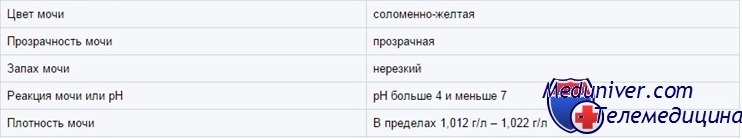
Цвет мочи у ребенка
В зависимости от концентрации моча может быть от почти прозрачной до темно-янтарной. Желтым цветом нормальная моча обязана главным образом урохрому. Другие пигменты — каротин, уробилин и билирубин — могут придать ей оранжевую окраску. Белая, похожая на молоко моча бывает у здоровых детей из-за выпадающего в осадок фосфата кальция (особенно если ее охлаждают); в редких случаях белая моча указывает на хилурию.
В моче грудных детей встречается розоватый осадок из уратов. Выпавшие в осадок ураты могут также давать «кирпичную пыль» на пеленках. Необычный цвет мочи часто вызывается пищевыми красителями, лекарственными средствами или некоторыми натуральными пищевыми продуктами, но может быть обусловлен пигментами, которые выделяются при разных болезнях. Для острого гломерулонефрита характерна коричневая моча (цвета крепкого чая или кока-колы, «ржавая» моча).
При гематурии моча может быть от бледно-розовой до ярко-красной. В таблице перечислены некоторые причины необычной окраски мочи.
Концентрация мочи у ребенка
У детей старше 6 мес осмолярность мочи (показатель числа осмотически активных частиц) составляет от 50 до 1200 мосм/л. Осмолярность — самый точный показатель концентрации мочи, но ее сложно измерять. Удельный вес (вес одного миллилитра мочи по отношению к весу одного миллилитра Н2О) легко измерить, и он в целом коррелирует с осмолярностью. Однако при глюкозурии и сильно выраженной протеинурии осмолярность, определенная по удельному весу, будет завышенной.
Глюкоза и рентгеноконтрастные вещества не влияют на определение удельного веса при помощи тест-полосок, но белки влияют. Удельный вес мочи колеблется от 1,001 до 1,030 и выше. Удельный вес выше 1,030, возможно, означает присутствие экзогенного вещества (например, рентгеноконтрастного).
pH мочи у ребенка
рН мочи колеблется от 4,5 до 8 и зависит от питания (чем больше белка, тем ниже рН), состояния КЩР и длительности хранения. Кислая (рН
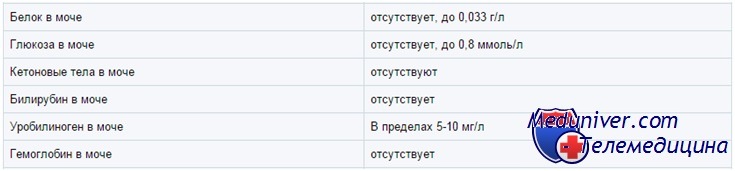
Белок в моче у ребенка
В норме моча содержит следовые количества белка (
Глюкоза в моче у ребенка
В норме глюкоза в моче не определяется (исключение — недоношенные дети). В тест-полосках обычно используется глюкозооксидазная реакция, специфичная по отношению к глюкозе. Другой метод — проба Бенедикта — основан на восстановлении ионов меди. Проба Бенедикта определяет все восстановители, включая глюкозу, и с ее помощью выявляют врожденные нарушения метаболизма Сахаров, например галактоземию.
Глюкозурия чаще всего возникает вследствие гипергликемии (избыток глюкозы попадает в мочу), но иногда отражает наследственное нарушение почечного транспорта глюкозы или же является частью общего нарушения функции проксимальных канальцев (синдрома Фанкони). У сильно недоношенных детей глюкозурия может быть вызвана незрелостью почечных канальцев.
Нитриты в моче у ребенка
Анализ на нитриты (с реактивом Грисса) используют, чтобы выявить бактериурию. Обычно в моче нитритов нет, но есть нитраты. Грамотрицательные бактерии восстанавливают нитраты до нитритов, но это занимает несколько часов. Поэтому положительная реакция возможна только при наличии в моче нитратов, выраженной бактериурии и достаточном для образования нитритов времени. Отрицательный результат еще не исключает бактериурию; при высоком уровне аскорбиновой кислоты возможен ложноотрицательный результат.
Лейкоцитарная эстераза в моче у ребенка
По лейкоцитарной эстеразе определяют лейкоцитурию. Если моча загрязнена влагалищными выделениями, результат будет положительным и в отсутствие инфекции мочевых путей или лейкоцитурии. Положительный результат нужно подтверждать исследованием осадка мочи под микроскопом.
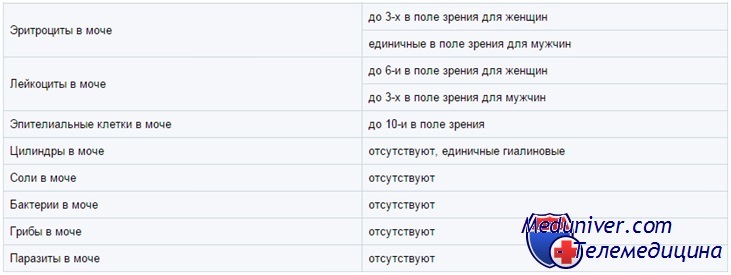
Гемоглобин, миоглобин, эритроциты в моче у ребенка
Гемоглобин и миоглобин дают с реагентами на тест-полоске в зависимости от концентрации зеленое либо синее окрашивание. Кроме того, эти реагенты лизируют эритроциты, так что внутриклеточный гемоглобин тоже вступает в реакцию. Ее чувствительность оценивают как 5—20 эритроцитов в поле зрения при большом увеличении микроскопа, или 0,015 мг% гемоглобина.
В моче часто встречаются следы гемоглобина; обычно это не говорит о болезни. Положительные результаты нужно сопоставить с микроскопией мочевого осадка. Отсутствие эритроцитов при микроскопии может означать, что реакцию дает свободный гемоглобин или миоглобин, но чаще — что эритроциты просто успели лизироваться.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Сахарный диабет у ребенка
Содержание статьи
Сахарный диабет у детей и подростков широко распространен. Патология характеризуется постоянно высоким уровнем глюкозы в крови. Заболевание сопровождается похуданием при хорошем аппетите, сильной жаждой и обильным мочеотделением.
При отсутствии адекватного лечения болезнь быстро прогрессирует по причине активного роста и повышенного обмена веществ у детей.
Виды диабета
Первый тип наиболее часто встречается у детей. Заболевание характеризуется очень низким уровнем инсулина, ребенку необходимо постоянное наблюдение.
При диабете 1 типа в организме недостаточно вырабатывается инсулин, необходимо постоянно контролировать его уровень и вводить дополнительно при необходимости. Причина неизвестна, заболевание нельзя предотвратить. Симптоматика проявляется в жажде, постоянном чувстве голода, чрезмерном мочеиспускании, усталости, снижении остроты зрения и потере веса. Симптомы могут возникнуть внезапно.
Диабет 2-го типа раньше наблюдался только у взрослых, теперь появляется и у детей. Патология является следствием неэффективного усвоения инсулина организмом. Развивается на фоне гиподинамии и лишнего веса. Симптомы менее выражены, чем при 1-м типе. Источник:
А.Б. Ресненко
Сахарный диабет 2-го типа у детей и подростков: от патогенеза к лечению // Педиатрическая фармакология, 2011, т.8, №4, с.125-129
Таблица сравнения типов СД
Признаки и симптомы
Суть протекания обменных процессов
Снижена выработка инсулина
Люди старше 40 лет
Выработка инсулина организмом
Поражены β-клетки, выработка прекращена
Инсулин вырабатывается, но клетки не используют его для проведения сахара
Введение инсулина, диета
Диета, увеличение физической активности, прием таблеток для снижения сахара
Откуда берется заболевание у детей?
Каждый тип диабета имеет свои причины. Существуют факторы риска, которые провоцируют болезнь:
Многих волнует, передается ли заболевание. Главной причиной возникновения сахарного диабета 1 типа у детей является наследственность. Это подтверждает большое количество семейных случаев, когда болезнь возникает у ребенка при наличии патологии у родителей, бабушек, дедушек.
Инициирует аутоиммунный процесс внешний фактор – вирусы. К хроническому инсулиту и инсулиновой недостаточности приводит воздействие вируса ECHO, Коксаки В, герпеса, краснухи, Эпштейна-Барр. Заболевание может вызвать энтеровирус, ротавирус, корь и другие. Источник:
П.Ф. Литвицкий, Л.Д. Мальцева
Расстройства углеводного обмена у детей: сахарный диабет // Вопросы современной педиатрии, 2017, т.16, №6, с.468-480
У детей с генетической предрасположенностью болезнь может запустить интоксикация, искусственное вскармливание, однообразное углеводистое питание, а также стрессы и перенесенные операции.
Диабет 2-го типа у детей развивается на фоне нарушения функции поджелудочной железы – когда b-клетки не вырабатывают и не выделяют инсулин. В результате чувствительность рецепторов снижается.
Порядок развития патологии
Инсулин – гормон, вырабатываемый поджелудочной железой, которая у ребенка маленькая. К 10-летнему возрасту железа весит 50 грамм и длина ее 12 см. Основная функция – выработка инсулина. Железа должна справляться с задачей уже к 5 годам.
Наибольший риск заболевания сахарным диабетом наблюдается в возрасте с 5 до 11 лет. В это время обмен веществ быстрый, хорошо усваивается сахар. Ежедневно ребенку необходимо 10 грамм углеводов. Обмен контролируется не до конца сформированной нервной системой, могут происходить сбои.
В группу риска входят подростки в период полового созревания, недоношенные младенцы и дети, которые испытывают большие нагрузки.
Особенности протекания болезни зависят от возраста, в котором проявились патология. У малышей диабет протекает тяжело, приводит к осложнениям. Родители должны понимать, что при сахарном диабете у детей требуется уход и пожизненное лечение.
Симптомы и первые признаки
Болезнь у ребенка может развиться в любом возрасте. Существует два пиковых периода – 5-8 лет и половое созревание, когда усиленный рост и обмен веществ.
Заболевание первого типа проявляется остро. Признаками сахарного диабета 1-го типа у детей являются: резкая слабость и головокружение при голоде и насыщении. От проявления первых симптомов до диабетической комы может пройти от 1 до 3 месяцев. Источник:
ISPAD Clinical Practice Consensus Guidelines 2009 Compendium. Pediatric Diabetes. 2009; 10 (Suppl. 12): 210
Первые признаки развития сахарного диабета у детей:
Родители могут заметить, что моча стала липкой, на нижнем белье остаются словно накрахмаленные пятна. Может наблюдаться сухость слизистых и эпидермиса – шелушение кожи на подошвах, ладонях. Среди симптомов сахарного диабета у детей раздражение в уголках рта («заеды»), стоматит. Появляются гнойнички, фурункулы, опрелости. У девочек развитие заболевания сопровождается вульвитами, у мальчиков – баланопоститами. Если заболевание впервые проявляется в период полового созревания девушки, это может спровоцировать нарушение менструального цикла.
У малышей сложно выявить симптоматику, поэтому обращают внимание на сопутствующие проявления. Для маленьких детей характерен ночной энурез, зуд, беспокойство, проблемы с пищеварением. При заболевании грудной ребенок жадно пьет молоко и воду. По причине сладкой липкой мочи пеленки жесткие. Такие признаки указывают на среднетяжелую и тяжелую форму развития патологии. При легкой форме заболевание диагностируют по анализу крови и мочи.
Диагностика сахарного диабета
Первым, кто выявляет симптомы заболевания, является педиатр, который наблюдает ребенка. Врач обращает внимание на классические признаки: повышенное мочеиспускание, ощущение жажды, голода и похудение.
Во время осмотра доктор может заметить диабетический румянец, пониженный тургор кожи и малиновый язык. При обнаружении симптомов сахарного диабета, педиатр передает пациента для лечения и наблюдения эндокринологу.
Для постановки точного диагноза ребенка направляют на лабораторное исследование. Необходимо сдать анализ крови на уровень сахара, применяют суточный мониторинг. Также проверяют инсулин, проинсулин, толерантность в глюкозе, уровень гликозилированного гемоглобина, КОС крови.
Таблица результатов анализа крови
Глюкоза капиллярной крови (ммоль/л)
Гипогликемическое состояние у детей
Редкий случай органического гиперинсулинизма у ребенка 3 месяцев Уровень глюкозы в крови натощак у практически здорового человека колеблется от 3,3 до 5,5 ммоль/л при определении глюкозооксидазным методом.
Редкий случай органического гиперинсулинизма у ребенка 3 месяцев
Уровень глюкозы в крови натощак у практически здорового человека колеблется от 3,3 до 5,5 ммоль/л при определении глюкозооксидазным методом. На протяжении суток глюкоза в плазме крови в норме может колебаться от 2,8 до 8,8 ммоль/л. Содержание глюкозы в крови ниже 2,7 ммоль/л принято называть гипогликемией.
Основная причина гипогликемического симптомокомплекса — гиперинсулинизм.
Гиперинсулинизм — патологическое состояние организма, обусловленное абсолютным или относительным избытком инсулина, вызывающим значительное снижение содержания сахара в крови; как следствие возникают дефицит глюкозы и кислородное голодание мозга, что ведет к нарушению в первую очередь высшей нервной деятельности.
Абсолютный гиперинсулинизм — это состояние, связанное с патологией инсулярного аппарата (первичный органический гиперинсулинизм). Наиболее частыми причинами органического гиперинсулинизма являются инсулинома — опухоль b-клеток островков Лангерганса, секретирующая избыточное количество инсулина (у взрослых и детей старшего возраста) и незидиобластоз — гиперплазия островков поджелудочной железы (у детей первого года жизни). Еще одна нередкая причина гиперинсулинизма у детей младшего возраста — функциональный гиперинсулинизм новорожденных от матерей с сахарным диабетом.
Доброкачественную аденому островков Лангерганса впервые обнаружил в 1902 году во время вскрытия Николлс. В 1904 году Л. В. Соболев описал «струму островков Лангерганса». В 1924 году Гаррис и отечественный хирург В. А. Оппель независимо друг от друга описали симптомокомплекс гиперинсулинизма. В этом же году Г. Ф. Ланг наблюдал множественный аденоматоз панкреатических островков. В России успешная операция удаления инсулиномы была выполнена в 1949 году А. Д. Очкиным, а в 1950 году — О. В. Николаевым. Инсулин-секретирующая опухоль описана во всех возрастных группах, от новорожденных до престарелых, однако чаще она поражает людей трудоспособного возраста — от 30 до 55 лет. Среди общего числа больных дети составляют всего около 5%. 90% инсулином — доброкачественные. Около 80% из них — солитарные. В 10% случаев гипогликемия обусловлена множественными опухолями, 5% из них — злокачественные, а 5% составляет незидиобластоз (Антонов А. В. Клиническая эндокринология, 1991).
Термин незидиобластоз введен Г. Лейдло в 1938 году. Незидиобластоз — это тотальная трансформация протокового эпителия поджелудочной железы в b-клетки, продуцирующие инсулин. У детей первого года жизни это наиболее частая причина органического гиперинсулинизма (лишь 30% гиперинсулинизма у детей обусловлено инсулиномой, 70% — незидиобластозом). Это генетически обусловленное заболевание.
Диагноз устанавливается только морфологически после исключения инсулиномы. Клинически он проявляется тяжелыми, трудно поддающимися коррекции гипогликемиями, вследствие чего при отсутствии положительного эффекта от консервативного лечения придется прибегать к уменьшению массы ткани поджелудочной железы. Общепринятый объем операции — 80 — 95% резекции железы.
Инсулиномы у детей встречаются исключительно редко и располагаются либо в хвосте, либо в теле поджелудочной железы. Их диаметр колеблется от 0,5 до 3 см. Малые размеры инсулином создают сложности для диагностики (информативность УЗИ-метода — не более 30%). Для определения локализации инсулиномы применяют селективную ангиографию, КТ и МРТ или сканирование с изотопом октреотида (аналог соматостатина). Наиболее информативной является ангиография с селективным забором крови из вен поджелудочной железы (60 — 90%).
Инсулинома проявляется более или менее резким падением уровня сахара крови, что обусловлено повышенной секрецией инсулина в кровь. Радикальным методом лечения инсулиномы является хирургический (инсулиномэктомия ), прогноз в большинстве случаев благоприятный (88 — 90%) при своевременном оперативном вмешательстве.
Органический гиперинсулинизм (инсулинома, незидиобластоз) является причиной тяжелых панкреатических гипогликемий с падением сахара крови до 1,67 ммоль/л и ниже (во время приступа). Эти гипогликемии всегда некетотические (ацетон в моче отрицательный за счет подавления процессов липолиза).
Наиболее часто в клинической практике встречаются кетотические гипогликемии (с ацетонурией). Кетотические гипогликемии являются внепанкреатическими и могут быть эндокринно- и неэндокриннозависимыми. Они сопровождаются относительным гиперинсулинизмом, то есть не связанным с патологией инсулярного аппарата поджелудочной железы (вторичный, функциональный, симптоматический гиперинсулинизм). Относительный гиперинсулинизм обусловлен повышением чувствительности организма к нормально выделяемому b-клетками панкреатических островков инсулину или нарушением компенсаторных механизмов, участвующих в регуляции углеводного обмена и в инактивации инсулина.
Эндокриннозависимые кетотические гипогликемии (без повышения уровня инсулина в крови) выявляются при недостаточности контринсулиновых гормонов у больных с гипофункцией передней доли гипофиза (церебрально-гипофизарный нанизм, изолированный дефицит СТГ, гипопитуитаризм), щитовидной железы (гипотиреоз), коры надпочечников (болезнь Аддисона).
Без повышения уровня инсулина могут протекать внепанкреатические гипогликемии, встречающиеся при экстрапанкреатических опухолях (грудной клетки, брюшной полости, ретроперитонеальные и т. д.), гипогликемии, сопровождающие диффузные заболевания печени, хроническую почечную недостаточность. У детей первого года жизни причиной кетотических неэндокринозависимых гипогликемий (без гиперинсулинизма) являются врожденные энзимопатии (гликогенозы).
В клинической практике часто встречаются реактивные гипогликемии — функциональный гиперинсулинизм при вегетососудистой дистонии. Они наблюдаются у лиц с ожирением, у детей-невротиков дошкольного возраста на фоне ацетонемических рвот из-за нарушения процессов глюконеогенеза и т. д.
Нередки также гипогликемии экзогенной природы (вызванные введением инсулина, сахароснижающих средств, салицилатов, сульфаниламидов и других лекарственных средств).
При функциональном гиперинсулинизме гипогликемии клинически менее выражены, содержание сахара крови не падает ниже 2,2 ммоль/л.
Обнаружить гипогликемию можно по клиническим признакам, чаще же сниженный уровень сахара в крови является лабораторной находкой. Достоверным считается выявление гипогликемии в ранние утренние часы или натощак перед завтраком в капиллярной крови не менее 2 — 3 раз (при отсутствии четких клинических данных). Показанием для обследования в стационаре является классическая клиника гиперинсулинизма или трижды подтвержденная утренняя гипогликемия (без клинических проявлений) ниже возрастных показателей (снижение гликемии натощак для новорожденных — менее 1,67 ммоль/л, 2 месяца — 18 лет — менее 2,2 ммоль/л, старше 18 лет — менее 2,7 ммоль/л).
Для гипогликемической болезни патогномоничной является триада Уиппла:
Большинство симптомов гипогликемии обусловлено недостаточным снабжением центральной нервной системы глюкозой. При снижении уровня глюкозы до гипогликемии включаются механизмы, направленные на гликогенолиз, глюконеогенез, мобилизацию свободных жирных кислот, кетогенез. В этих процессах участвуют в основном 4 гормона: норадреналин, глюкагон, кортизол, гормон роста. Первая группа симптомов связана с повышением в крови содержания катехоламинов, что вызывает слабость, тремор, тахикардию, потливость, беспокойство, чувство голода, побледнение кожных покровов. Симптомы со стороны ЦНС (симптомы нейрогликопении) включают головную боль, двоение в глазах, нарушение поведения (психическое возбуждение, агрессивность, негативизм), в дальнейшем наступает потеря сознания, появляются судороги, может развиться кома с гипорефлексией, поверхностным дыханием, мышечной атонией. Глубокая кома ведет к смерти или необратимым повреждениям ЦНС. Частые приступы гипогликемии приводят к изменению личности у взрослых, снижению интеллекта у детей. Отличие симптомов гипогликемии от настоящих неврологических состояний — положительный эффект приема пищи, обилие симптомов, не укладывающихся в клинику.
Наличие выраженных нервно-психических нарушений и недостаточная осведомленность врачей о гипогликемических состояниях часто приводят к тому, что вследствие диагностических ошибок больные с органическим гиперинсулинизмом длительно и безуспешно лечатся под самыми разными диагнозами. Ошибочные диагнозы ставятся у 3/4 больных с инсулиномой (эпилепсия диагностируется в 34% случаев, опухоль головного мозга — в 15%, вегетососудистая дистония — в 11%, диэнцефальный синдром — в 9%, психозы, неврастения — 3% (Dizon A. М., 1999).
Период острой гипогликемии — это результат срыва контринсулярных факторов и адаптационных свойств ЦНС.
Чаще всего приступ развивается в ранние утренние часы, что связано с продолжительным ночным перерывом в приеме пищи. Обычно больные не могут «проснуться» из-за различного рода расстройств сознания. Может быть вялость, апатия по утрам. Наблюдаемые у этих больных эпилептиформные припадки отличаются от истинных большей продолжительностью, хориоформными судорожными подергиваниями, гиперкинезами, обильной нейровегетативной симптоматикой. Распознавание заболевания требует тщательного изучения анамнеза и внимательного наблюдения за больными. Это особенно важно для диагностики органического гиперинсулинизма как причины гипогликемии у детей.
У детей первого года жизни клинически выявить гипогликемию сложно, так как симптомы нечетки и нетипичны. Это может быть цианоз, бледность кожных покровов, снижение мышечного тонуса, остановка дыхания (апноэ), тремор, судороги, «закатывание» глазных яблок (нистагм), беспокойство. При врожденной форме (незидиобластоз) наблюдается большая масса тела (крупный плод), отечность, круглое лицо.
У детей дошкольного и школьного возраста с органическим гиперинсулинизмом чаще регистрируется доброкачественная инсулинома. Для этих детей характерны утренняя неработоспособность, трудности утреннего пробуждения, нарушение концентрации внимания, выраженные чувство голода, тяга к сладкому, негативизм, сердцебиения. Гиперинсулинизм приводит к повышению аппетита и ожирению. Чем моложе ребенок, тем больше выражена склонность к низкому сахару крови в ответ на более продолжительные перерывы между приемами пищи.
Среди лабораторных показателей при подозрении на органический гиперинсулинизм (инсулиному или незидиобластоз) особое место занимает исследование иммунореактивного инсулина (ИРИ). Но, как показала практика, далеко не всегда при доказанной инсулиноме имеются повышенные его значения. ИРИ принято оценивать одновременно с уровнем гликемии. Важным является индекс отношения инсулина к глюкозе — ИРИ мкед/мл/глюкоза венозная ммоль/л. У здоровых людей и на фоне гипогликемии без гиперинсулинизма этот индекс составляет менее 5,4.
Среди функциональных проб, используемых для диагностики органического гиперинсулинизма, наиболее распространена проба с голоданием.
Проба основана на развитии гипогликемии у людей с гиперфункцией инсулярного аппарата поджелудочной железы при прекращении поступления углеводов с пищей. Во время проведения пробы больному разрешается пить только воду или чай без сахара. Чем младше ребенок и чем чаще приступы гипогликемии, тем проба короче.
Длительность пробы:
дети до 3 лет — 8 ч;
2 — 10 лет — 12-16 ч;
10 — 18 лет — 20 ч;
старше 18 лет — 72 ч.
(рекомендации кафедры детской эндокринологии РМАПО, Москва).
У детей 2 лет и старше последний прием пищи должен быть накануне вечером; детям до 2 лет пробу начинают в ранние утренние часы.
У здорового человека ночное, а также более продолжительное по времени голодание умеренно снижает уровень гликемии и, что характерно, уменьшает содержание инсулина в крови. При наличии опухоли, постоянно продуцирующей избыточное количество инсулина, в условиях голодания создаются предпосылки для развития гипогликемии, поскольку поступления глюкозы из кишечника нет, а печеночный гликогенолиз блокирован опухолевым инсулином.
Перед началом пробы определяют содержание глюкозы в плазме крови. Далее гликемия в капиллярной крови (глюкометром) исследуется у детей до 2 лет 1 раз в час, у детей в возрасте 2 лет и старше — 1 раз в 2 часа. При снижении сахара в крови до 3,3 ммоль/л и меньше интервалы исследования сокращаются в 2 — 3 раза. Порог допустимой гликемии, при котором голодание прекращают и проводят исследования, — 1,7 ммоль/л у ребенка до 2 лет, 2,2 ммоль/л у детей старше 2 лет. После регистрации глюкометром пороговой гипогликемии исследуется сыворотка крови на содержание ИРИ и контринсулиновых гормонов, глюкоза крови исследуется биохимическим методом (поскольку после снижения уровня глюкозы до 3,3 ммоль/л и ниже глюкометр дает неточный результат), исследуется уровень липидов крови.
Купируется приступ гипогликемии введением в/в струйно 40% глюкозы; сразу после введения глюкозы и через 3 часа после окончания пробы исследуется моча на содержание кетоновых тел.
Интерпретация результатов пробы
В случае подтверждения гиперинсулинизма как причины гипогликемии необходимо дообследование и лечение в специализированном эндокринологическом отделении.
Во всех случаях инсулином показано хирургическое лечение. При незидиобластозе терапия может быть консервативной и радикальной. Наибольшее признание в настоящее время получил препарат диазоксид (прогликем, зароксолин). Гипергликемизирующий эффект этого недиуретического бензотиазида основан на торможении секреции инсулина из опухолевых клеток. Рекомендуемая доза для детей — 10 — 12 мг на кг массы тела в сутки в 2 — 3 приема. При отсутствии выраженной положительной динамики показано оперативное лечение — субтотальная или тотальная резекция поджелудочной железы (с возможным переходом в сахарный диабет).
С. А. Столярова, Т. Н. Дубовая, Р. Г. Гарипов
С. А. Мальмберг, доктор медицинских наук
В. И. Широкова, кандидат медицинских наук
ДКБ №38 ФУ «Медбиоэкстрем» при МЗ РФ, Москва
Больной Захар З., 3 мес., поступил в отделение психоневрологии ДКБ № 38 ФУ «Медбиоэкстрем» Москвы 01.11.02 с направляющим диагнозом эпилепсия.
Ребенок с умеренно отягощенным перинатальным анамнезом. Беременность у матери первая, протекала с токсикозом в первой половине, анемией. Роды на 40-й неделе, крупный плод (вес при рождении 4050 г, длина 54 см). Оценка по шкале Апгар — 8/9 баллов. С периода новорожденности до 2 мес. периодически отмечался тремор подбородка, с 2-месячного возраста появились приступообразные состояния в виде остановки взора, снижения двигательной активности, подергивания правой половины лица, правой руки (приступы фокальных судорог) — по несколько секунд 3 — 4 раза в сутки. Лечился амбулаторно у невропатолога, получал противосудорожную терапию без выраженного положительного эффекта. Накануне госпитализации появились хореиформные подергивания в утренние часы на фоне нарушенного сознания. Госпитализирован в отделение психоневрологии с направляющим диагнозом эпилепсия.
При поступлении состояние ребенка средней тяжести. В соматическом статусе — кожные покровы с проявлениями атопического дерматита, зев чистый, в легких хрипов нет, тоны сердца звучные, тахикардия до 140 — 160 уд. в мин. Живот мягкий, печень +2 см, селезенка +1 см. Мочеиспускание не нарушено. В неврологическом статусе — вялый, взгляд фиксирует, голову удерживает плохо. ЧН — интактны, мышечный тонус снижен, больше в руках, симметричный. Сухожильные рефлексы невысокие, Д=С, безусловные рефлексы н/р — по возрасту. Вес — 7 кг, рост — 61 см (отмечается избыток веса на фоне средневозрастного показателя роста).
В стационаре при исследовании биохимического анализа крови натощак впервые выявлено снижение сахара в крови до 1,6 ммоль/л при отсутствии кетоновых тел в моче.
Результаты лабораторного и инструментального обследования:
Динамический контроль уровня глюкозы позволил выявить стойкую гипогликемию в капиллярной и венозной крови. Натощак и через 2 часа после кормления грудным молоком в течение суток гликемия колебалась от 0,96 до 3,2 ммоль/л. Клинически гипогликемия проявлялась повышенным аппетитом, вялостью, тахикардией, эпизодами «закатывания» правого глазного яблока, генерализованными эпилептиформными судорогами. В межприступный период самочувствие удовлетворительное. Гипогликемические состояния купировались приемом глюкозы внутрь, а также внутривенным введением 10%-ной глюкозы.
С диагностической целью для подтверждения гиперинсулинизма ребенку проведена проба с голоданием: последнее ночное кормление в 6 часов утра, перед кормлением гликемия — 2,8 ммоль/л, через 3,5 часа после кормления глюкометром отмечено снижение уровня гликемии до 1,5 ммоль/л (ниже допустимого порогового значения). На фоне гипогликемии взята сыворотка крови для гормонального исследования (ИРИ, с-пептид. кортизол, СТГ). Сделан забор венозной крови для биохимического исследования уровня глюкозы и липидов. После купирования гипогликемии в/в струйным введением глюкозы собрана трехчасовая порция мочи на содержание кетоновых тел.
Результаты пробы: ацетонурии нет. Уровень контринсулиновых гормонов не снижен (кортизол — 363,6 при норме 171 — 536 нмоль/л, СТГ — 2,2 при норме 2,6 — 24,9 мкЕ/мл). С-пептид — 0,53 при норме — 0,36 — 1,7 пмоль/л. ИРИ — 19,64 при норме — 2,6 — 24,9 ммкЕ/мл. Глюкоза венозная — 0,96 ммоль/л. Уровень липидов крови на нижней границе нормы (триглицериды — 0,4 ммоль/л, холестерин общ. — 2,91 ммоль/л, холестерин липопр. выс. плотн. — 1,06 ммоль/л, холест. липопр. низк. плотн. — 1,67 ммоль/л. Индекс ИРИ/глюкоза (19,64 /0,96) составил 20,45 при норме менее 5,4.
Данные анамнеза, динамического наблюдения, клинико-лабораторного обследования позволили поставить диагноз: некетотическая гипогликемия. Гиперинсулинизм. Незидиобластоз?
Для уточнения генеза заболевания и тактики лечения ребенок переведен в эндокринологическое отделение РДКБ Москвы, где инсулинома у мальчика исключена. Подтвержден диагноз незидиобластоз. Назначено пробное консервативное лечение прогликемом в дозе 10 мг на кг массы тела. Отмечена тенденция к нормализации показателей углеводного обмена. Планируется дальнейшее динамическое наблюдение для коррекции тактики лечения.
Рассмотренный клинический случай диктует необходимость исследования показателей углеводного обмена у всех детей раннего возраста с судорожным синдромом, ввиду стертости клинических симптомов гипогликемии у детей грудного и раннего детского возраста, для исключения диагностических ошибок.