Госсипол и кагоцел что общего
Ученые-химики: Если «Кагоцел» безопасен, значит, как лекарство он бесполезен
«Кагоцел» не может оказывать заявленного в инструкции противовирусного действия. А возможно, противозачаточного и токсического. Такой вывод сделали ученые Российского химико-технологического университета им. Менделеева. И сообщили о нем Комиссии РАН по борьбе с лженаукой.
Однако ученые давно не верят в препарат со сложным активным веществом. Поэтому Комиссия РАН по борьбе с лженаукой обратилась в Российский химико-технологический университет им. Менделеева с просьбой разъяснить, что представляет собой препарат «Кагоцел»: «В СМИ, в первую очередь на телевидении, идет масштабная рекламная кампания препарата для лечения гриппа и ОРВИ под названием «Кагоцел». Задекларированный производителем состав действующего вещества препарата, вызывает серьезное недоумение, в связи с чем прошу Вас дать профессиональную консультацию по возникшим вопросам:
2. Может ли в принципе существовать вещество с подобным химическим названием или химической формулой?»
Председатель комиссии РАН по борьбе с лженаукой, академик РАН Евгений Александров получил ответ от Анны Щербины, проректора по науке Российского химико-технологического университета им. Менделеева, в котором объясняется происхождение столь сложного названия. Его получило химическое вещество, образующееся при взаимодействии карбоксиметилцеллюлозы с госсиполом, от авторов патента РФ за № 2270708 («Натриевая соль сополимера карбоксиметилцеллюлозы и госсипола, фармацевтическая композиция и способ профилактики или лечения вирусных заболеваний»).
Кагоцел: противозачаточное под видом противовирусного?
Демографическая таблетка
Китай и Бразилия образца 1970-го года не могли допустить дальнейшего роста численности населения, которое и без того было нечем кормить, поэтому изобретение препарата, нарушающего сперматогенез, казалось отличным решением проблемы. Тот факт, что у каждого пятого из принимавших госсипол развивалось необратимое бесплодие, поначалу никого особо не смущал. Просто в инструкцию внесли пункт о том, что принимать его рекомендуется лишь после того, как мужчина произвел на свет запланированное потомство. Тем не менее до применения препарата в США и Европе дело так и не дошло. В 1998 году экспертная комиссия Всемирной организации здравоохранения по проблемам мужской фертильности приняла решение о запрете госсипола, потому что вреда от его приема оказалось больше, чем пользы. Ведь что такое госсипол? Один из пигментов хлопчатника, относящегося к классу полифенолов, который сам по себе достаточно токсичен.
Уровень небезопасности
Препарат может вызывать гипокалиемию – снижение уровня калия в крови, приводя к общей и мышечной слабости и нарушениям сердечной деятельности. Конечно, дефицит калия можно восполнить с помощью содержащих его лекарств – панангина или аспаркама. Их обычно назначают, чтобы компенсировать потерю этого минерала при приеме мочегонных средств (диуретиков), выводящих его из организма. А вот способность госсипола вызывать необратимое бесплодие намного серьезнее негативных эффектов гипокалиемии.
А ведь после без малого 20 лет повсеместного применения «инновационного нанопрепарата» для профилактики герпеса, гриппа, ОРВИ, а теперь уже и коронавирусной инфекции эти 9% грозят превратиться в куда больший показатель в ближайшем будущем, когда подросшие мальчики захотят обзавестись собственными семьями.
Иммунная индукция
Так ли уж хороши противовирусные свойства препарата, чтобы можно было пренебречь репродуктивными рисками? Кагоцел относится к так называемым индукторам интерферонов – белков, которые блокируют воспроизведение вирусов. Но делают они это не целенаправленно, как антитела, «заточенные» против определенного возбудителя. И не как лекарства вроде ацикловира, который уничтожает конкретно вирус герпеса, или осельтамивира, уничтожающего вирус гриппа. У интерферонов нет такой спецификации, они бьют из пушки по воробьям, то есть по всем вирусам сразу, но ни по одному не попадают прицельно.
Да и начать прием кагоцела нужно успеть до 4-го дня заболевания, иначе эффект будет не таким заметным. Получается, что ради повышения неспецифического иммунитета, который а) можно укрепить зарядкой перед открытой форточкой и обливанием холодной водой и б) от вируса на сто и даже на пятьдесят процентов не защищает, мы готовы пожертвовать репродуктивным здоровьем нации.
Клубок противоречий
«Но позвольте, – возражают сторонники лечения кагоцелом, – риск бесплодия и возможные токсические эффекты несет в себе госсипол в свободном виде. А в нашем нанопрепарате он соединен с сополимером – карбоксиметилцеллюлозой. В результате получается довольно крупная молекула, неспособная проникать через ограничительные барьеры организма в головной мозг и ткань яичек, а значит, отравлять первый и нарушать образование сперматозоидов во вторых».
Все это верно, но ведь связь госсипола с сополимером может разрушаться под действием ферментов желудочно-кишечного тракта и ряда других факторов. И тогда, если верить предупреждению ВОЗ, вред начинает преобладать над пользой.
Может ли прием кагоцела вызвать бесплодие?
Какое лекарство от «простуды» вызывает бесплодие у мужчин? Подобных вопросов и отзывов в интернете предостаточно. С чем связаны страхи, что кагоцел влияет на мужскую фертильность? Например, существует мнение, что госсипол — пигмент хлопка и активный компонент кагоцела снижает шансы на зачатие у мужчин. Так ли это на самом деле?
Считается, что противовирусные препараты, такие как кагоцел, в состав которого входит госсипол — вещество, выделяемое из вегетативных частей хлопка, может подавлять сперматогенез и в некоторых случаях «работать» как мужской контрацептив. По своей химической природе госсипол — это алкалоид токсического действия, необходимый растению для защиты от вредных насекомых-вредителей.
Известно, что госсипол снижает подвижность зрелых сперматозоидов и приводит к угнетению развивающихся форм сперматозоидов, особенно на стадии сперматид. Он также способен ингибировать ряд белков и ферментов, содержащихся в сперматозоидах и клетках сперматогенного эпителия. Получается, что кагоцел также может спровоцировать бесплодие?
Противопростудные средства и бесплодие, как открыли госсипол
В первой трети XX века мужчины северных провинций Китая, среди которых этнические киргизы, уйгуры и китайцы столкнулись с проблемой бесплодия. Проанализировав возможные факторы, ученые обнаружили, что на фертильность оказало влияние употребление в пищу хлопкового масла, которое является традиционным для этой области. Одним из токсичных веществ в масле оказался тот самый госсипол.
С госсиполом история вообще странная. В 70-е гг XX века китайские ученые пытались создать на его основе мужской контрацептив, — необходимо было контролировать рождаемость в стране. Однако из разработки его вывели из-за токсичности.
Среди наиболее неблагоприятных эффектов при приеме чистого госсипола были:
К концу 90-х годов XX века исследования госсипола были прекращены по рекомендации ВОЗ. Но не везде.
Принимать или нет лекарства от «простуды», если хочешь ребенка?
Многих мужчин волнует риск стать бесплодными, в том числе и из-за употребления кагоцела. Масла в огонь подливают публикации в Интернете и медицинской литературе, ведь именно госсипол используется в производстве кагоцела. Есть данные, что госсипол, как и его производные, обладает определенным противовирусным, иммуномодулирующим действием.
При изготовлении кагоцела госсипол используется в сочетании с карбоксиметилцеллюлозой, которая, по словам производителей, нивелирует отрицательные свойства, присущие свободной форме вещества. Однако есть информация и о том, что с целлюлозой соединяется минимальный процент госсипола, другая часть остается в несвязанном виде. В любом случае научных исследований на эту тему пока существует не так много. То есть потенциальная опасность все же существует?
На вопросы о том, правда ли что кагоцел вызывает бесплодие, на официальном сайте легко найти ответы медиков консультантов. Пишут, что «средство в ходе доклинических и клинических исследований показало высокий профиль безопасности (разрешен даже детям с 3-х лет), в инструкции написано, что применять можно с 6-ти лет и все исследования, включая изучение влияния на сперматогенез у животных, были проведены»*. У животных, но не у человека.
Как говорится, есть над чем подумать, особенно, если с зачатием у мужчины возникают трудности.
ОЦЕНКА ВОЗМОЖНОСТИ ВЫСВОБОЖДЕНИЯ СВОБОДНОГО ГОССИПОЛА ИЗ ПРЕПАРАТА «КАГОЦЕЛ» ПОД ВОЗДЕЙСТВИЕМ ИМИТАТОРОВ ПИЩЕВАРИТЕЛЬНЫХ СОКОВ ЧЕЛОВЕКА
Введение. Лекарственный препарат «Кагоцел» (таблетки 12 мг) создан на основе полимера окисленной целлюлозы с привитыми химически модифицированными молекулами природного полифенола – госсипола. В связанном состоянии этот природный полифенол с высокой биологической активностью утрачивает свою токсичность, при этом сохраняя полезные фармакологические свойства. При производстве субстанции «Кагоцел» обеспечивается тщательное удаление и контроль остаточного количества не связавшихся остатков свободного госсипола. Отсутствие токсических эффектов препарата «Кагоцел» подтверждено в ходе доклинических исследований. Дополнительным подтверждением безопасности препарата может служить отсутствие высвобождения молекул свободного госсипола в организме человека из активной субстанции препарата под воздействием пищеварительных соков.
Цель работы – оценка содержания свободного госсипола в препарате «Кагоцел» после воздействия на него стандартных модельных сред – имитаторов желудочного и кишечного сока человека, а также после инкубации препарата в среде, содержащей активную микробную целлюлазу.
Материал и методы. Объект исследования – лекарственный препарат «Кагоцел, таблетки 12 мг». Для контроля и количественного определения свободного госсипола в составе модельных сред использован высокочувствительный метод высокоэффективной жидкостной хроматографии с масс-спектрометрическим детектированием (ВЭЖХ-МС).
Результаты. Разработана и валидирована высокочувствительная и высокоспецифичная ВЭЖХ-МС методика определения свободного госсипола в препарате «Кагоцел, таблетки 12 мг». Методика позволяет надежно детектировать свободный госсипол в жидкой среде при его концентрации в растворах в диапазоне от 0,005 до 2,500 мкг/мл. Содержание микропримесей в виде свободного госсипола в среде после 24-часового инкубирования препарата в стандартных имитаторах желудочного и кишечного соков, а также после воздействия микробной целлюлазы не возрастает.
Заключение. Высвобождения и накопления свободного госсипола после длительного инкубирования таблеток «Кагоцел» как в имитационных средах, так и в среде, содержащей микробную целлюлазу, не происходит.
Ключевые слова: кагоцел, госсипол, модельные среды, ВЭЖХ, валидация.
Introduction. Kagocel (12-mg tablets) has been designed on the basis of an oxidized cellulose polymer with grafted chemically modified molecules of the natural polyphenol gossypol. When this natural highly biologically active polyphenol is in a bound state, it loses its toxicity, by maintaining its beneficial pharmacological properties. The manufacture of Kagocel ensures thorough removal of unbounded free gossypol residues and control of the presence of the latter. Lack of toxic effects of Kagocel has been confirmed by preclinical studies. In addition, the safety of the drug can be proved by the fact that free gossypol cannot be released from the active substance of the drug in the human body under the influence of digestive juices.
Objective: to estimate the content of free gossypol in Kagocel after exposure to standard model environments, such as human gastric and intestinal juice simulants, as well as after incubation of the drug in the medium containing active microbial cellulase.
Material and methods. The investigation object was 12-mg tablets of Kagocel. The highly sensitive method, namely: high-performance liquid chromatography with mass spectrometric detection (HPLC-MS) was used to monitor and quantify free gossypol as part in the model media.
Results. The highly sensitive and highly specific HPLC-MS procedure was developed and validated to determine minimal quantities of residual free gossypol in Kagocel (12-mg tablets). The procedure allows reliable detection of free gossypol at solution concentrations in the range of 0.005 to 2.500 µg/ml. The content of traces as free gossypol in the medium after 24-hour incubation in standard gastric and intestinal juice simulants, as well as after exposure to microbial cellulase did not increase.
Conclusion. The release and accumulation of free gossypol do not occur after prolonged incubation of Kagocel in both simulation and microbial cellulase-containing environments.
Key words: Kagocel, gossypol, model media, high-performance liquid chromatography, validation.
Введение
Тем не менее, на основе госсипола созданы и используются в клинической практике различные лекарственные средства (ЛС), среди которых наиболее широко применяемый в настоящее время противовирусный препарат «Кагоцел». Активным веществом этого препарата является уникальное соединение, представляющее собой полимерную матрицу диальдегид-карбоксиметилцеллюлозы (ДАКМЦ) с прочно присоединенными молекулами госсипола. Контроль полноты удаления исходно добавляемого в реакцию синтеза госсипола и подтверждение его отсутствия в конечном лекарственном препарате – обязательный элемент системы контроля качества субстанции и препарата «Кагоцел».
Цель работы — отработать и валидировать в соответствии с современными требованиями высокочувствительную и специфичную методику ВЭЖХ-анализа, пригодную для обнаружения минимальных примесей свободного госсипола, в том числе в составе модельных сред. Оценить содержание свободного госсипола в препарате «Кагоцел» до и после воздействия на него стандартных сред — имитаторов желудочного и кишечного сока человека, а также после инкубации препарата в среде, содержащей активную микробную целлюлазу.
Материалы и методы
Объектом исследования служили образцы таблеток препарата «Кагоцел, таблетки 12 мг» (производственная серия 0250216).
В качестве стандартного образца госсипола в работе использовали коммерческий реактив госсипола «Sigma Aldrich» (кат. № G8761) с содержанием основного вещества не менее 95%.
Реактивы для ВЭЖХ. Для приготовления подвижной фазы при проведении хроматографического исследования применяли ацетонитрил (900667 SigmaAldrich), муравьиную кислоту (17186 Sigma-Aldrich), этанол (ГОСТ 5962-2013), ацетон (650501 SigmaAldrich), ледяную уксусную кислоту (64-19-7 SigmaAldrich), воду деионизированную (Milli-Q). Все растворы перед введением в хроматограф фильтровали через мембранный фильтр PTFE (политетрафторэтилен) с размером пор 0,45 мкм.
Приготовление испытуемых растворов. Для проведения исследований на содержание свободного госсипола таблетки препарата «Кагоцел» истирали в ступке до состояния пудры. В пластиковую пробирку объемом 15 мл помещали точную навеску образца массой 0,350–0,450 г, добавляли 2 мл воды, вносили 2 мл смеси ацетонитрил/CH3COOHлед (99,2/0,8 об./об.), перемешивали 30 с на высокоскоростном шейкере-вортексе, инкубировали в течение 10 мин на орбитальном шейкере при комнатной температуре (20—25°С) в скоростном режиме 260 об/мин. Образец инкубировали 2 ч при температуре −15—-18°С, с помощью шприца (вместимостью 5 мл) с длинной иглой отбирали жидкую фазу, фильтровали через одноразовый мембранный PTFE-фильтр с диаметром пор 0,45 мкм. Анализируемый раствор хранили во флаконе из темного стекла при температуре не выше 10°C не более 3 ч.
Приготовление раствора сравнения. Навеску стандартного образца госсипола массой 0,0010 г помещали в мерную колбу, растворяли в 2–4 мл смеси ацетонитрил/CH3COOHлед (99,2/0,8 об./об.), перемешивали, доводили объем до 10 мл той же смесью (раствор А, 100 мкг/мл). Раствор Б представлял собой разбавленный в 10 раз ацетонитрилом раствор А. Растворы хранили в темноте при температуре −10—-18°С не более 1 сут.
Состав имитатора желудочного сока (ИЖС) (pH среды – 1,2):
• пепсин очищенный «Carl Roth» (2000 ед/г) – 0,32г;
• NaCl – 0,20 г;
• HCl конц. – 0,7 мл;
• вода очищенная до 100 мл.
Состав имитатора кишечного сока (ИКС)(pH среды – 6,8):
• панкреатин «PanReac» (35000 ед/г) – 1,0 г;
• KH2PO4 – 0,68 г;
• NaOH, 0,2М – 7,7 мл.
Испытание влияния инкубации в модельных средах на препарат «Кагоцел». Для каждой модельной среды готовили 2 параллельные пробы: в мерную колбу объемом 25 мл, изолированную от света фольгой, вносили точную навеску диспергированного исследуемого образца порошка растертых таблеток «Кагоцел» массой 4,5–5,5 г, добавляли 15 мл среды, перемешивали (не взбалтывая) до состояния однородной суспензии, объем доводили до метки, интенсивно перемешивали в течение 1 мин, избегая образования пены (суспензия МС). Колбы устанавливали в термостатированный орбитальный шейкер, и непрерывно перемешивали (скорость 260 об/мин) при температуре 37°С.
Пробы объемом 4 мл каждая отбирали через заданные промежутки времени (0, 3 и 24 ч). Для проведения хроматографического исследования отобранных образцов к ним добавляли 4 мл смеси ацетонитрил/CH3COOHлед (99,2/0,8 об./об.), и далее обрабатывали, согласно описанию приготовления испытуемых растворов применительно к таблеткам (см. выше). Образцы хранили при температуре не выше 10°C не более 3 ч.
ВЭЖХ-анализ проб выполняли на жидкостном хроматографе Agilent 1290, оборудованном двухканальным насосом Agilent Technologies 1290 Infinity Binary Pump; блоком для термостатирования; хроматографической колонкой Agilent Technologies 1290 Infinity TCC; автосамплером Agilent Technologies 1290 Infinity Sampler; тройным квадрупольным масс-спектрометрическим детектором Agilent Technologies 6460 Triple Quad LC/MS c источником ионов типа электроспрей Jet Stream ESI.
Разделение выполняли на хроматографической колонке Agilent С18 SB-Aq 2,1×50 мм, заполненной октадецилсилильным эндокепированным силикагелем для хроматографии (C18) с размером частиц 1,8 мкм. В ходе исследования колонку поддерживали при постоянной температуре 40°С. Объем пробы для анализа — 5 мкл; скорость элюирования — 0,4 мл/мин.
Результаты и обсуждение
Разработка и валидация методики количественного определения примесей свободного госсипола
Для определения свободного госсипола в составе лекарственного препарата «Кагоцел», в том числе и после его помещения в модельные среды, выбрали вариант ВЭЖХ с масс-спектрометрическим детектированием (ВЭЖХ-МС), как наиболее чувствительный и специфичный биоаналитический метод.
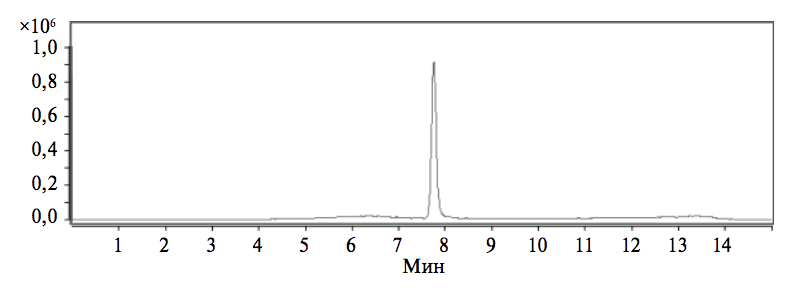
На 1-м этапе исследований отрабатывали условия испытаний лекарственного препарата «Кагоцел» на наличие свободного госсипола. В ходе отработки и валидации методики в качестве стандартного образца (СО) использовали коммерческий препарат очищенного госсипола. При этом анализ методом ВЭЖХ-МС выполняли в условиях детектирования специфического для госсипола иона размером 517.2 а.е.м. (рис. 1).
Результаты предварительных экспериментов подтвердили высокую чувствительность метода и его пригодность для количественной оценки содержания госсипола в средах.
С учетом данных литературы о значительной нестабильности растворов госсипола в ряде органических растворителей 14 в ходе отработки условий выполнения методики также осуществляли выбор оптимального состава подвижной фазы для хроматографии. При этом предварительно были получены данные, подтвердившие стабильность на уровне не менее 97–98% от исходной концентрации растворов госсипола (0,2 мкг/мл) в ацетоне, ацетонитриле и в смеси ацетонитрил–уксусная кислота (99,2/0,8 об./об.) в течение 3 ч.
Кроме того, выбор оптимальной для проведения исследований системы растворителей в составе подвижной фазы был обусловлен полученными в ходе отработки методики результатами оценки эффективности экстракции примесей свободного госсипола из порошка растертых таблеток препарата (табл. 1).
| Экстрагент | Среднее значение содержания свободного госсипола, нг/мг препарата |
|---|---|
| Ацетонитрил | 0,01 |
| Ацетонитрил/уксусная кислота (99,2/0,8 об./об.) | 0,01 |
| Вода | 0,19 |
| Ацетонитрил/вода (50/50 об./об.) | 1,09 |
| Ацетонитрил/уксусная кислота (99,2/0,8 об./об.) + равный объем воды | 1,17 |
Таким образом, максимальный эффект извлечения из таблеток препарата имеют системы растворителей (ацетонитрил/уксусная кислота (99,2/0,8 об./ об.) – вода (50/50 об./об.) или ацетонитрил–вода (50/50 об./об.).
Для дальнейших экспериментов в качестве подвижной фазы для хроматографии использовали систему растворителей (ацетонитрил/уксусная кислота (99,2/0,8 об./об.) – вода (50/50 об./об.).
На следующем этапе определяли оптимальные условия пробоподготовки и проведения ВЭЖХ-МС-анализа наличия примесей свободного госсипола в таблетках лекарственного препарата «Кагоцел». В ходе этих исследований были отработаны условия для отделения нерастворимых компонентов из состава вспомогательных веществ, содержащихся в таблетках препарата. При этом с использованием модельных смесей было подтверждено сохранение количественного характера извлечения из таблеток добавляемых примесей госсипола.
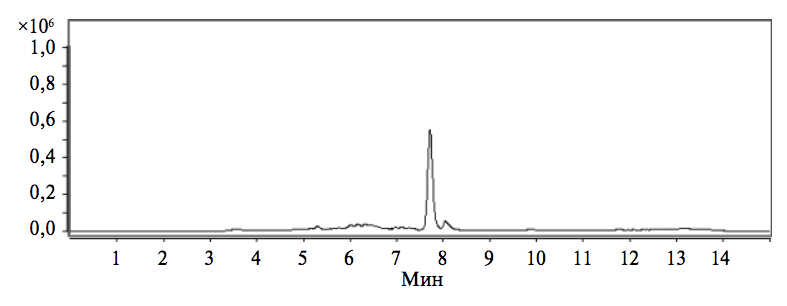
В условиях эксперимента сохранялись высокая чувствительность и специфичность анализа, при котором содержащиеся в препарате вспомогательные вещества не оказывали существенного влияния на результаты исследования (рис. 2).
После отработки условий выполнения анализа осуществляли валидацию методики хроматографического определения содержания свободного госсипола в лекарственном препарате «Кагоцел». При этом, согласно рекомендациям ГФ XIII, методика оценивалась по следующим параметрам: специфичность, предел обнаружения и количественного определения, линейность и аналитический диапазон, правильность, прецизионность.
Специфичность методики обнаружения анализируемого вещества (госсипол) в исследуемых образцах подтвердили путем сопоставления результатов исследования проб, приготовленных отработанным способом из порошка растертых таблеток, с результатами исследования СО госсипола (см. рис. 1 и 2). Эти данные не выявили негативного влияния вспомогательных веществ в таблетках «Кагоцела» на результаты количественного определения содержания свободного госсипола.
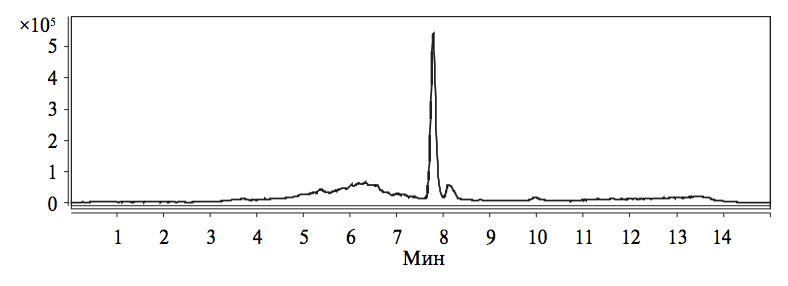
Аналогичным образом было подтверждено отсутствие мешающего действия компонентов модельных сред на результаты обнаружения госсипола (рис. 3).
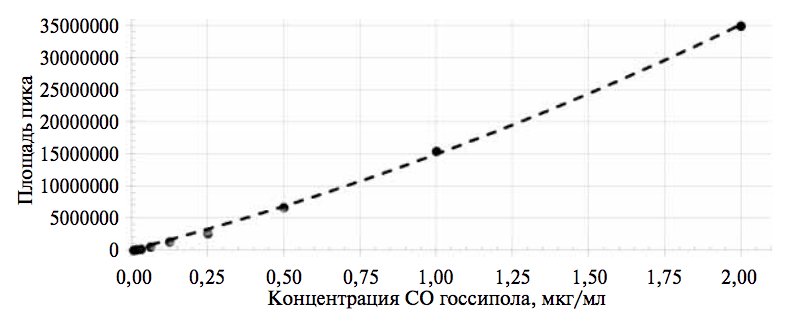
Линейность отработанной методики рассчитывали вычислением площадей пиков определяемого вещества на хроматограммах, полученных для серии из 9 растворов СО с содержанием госсипола в диапазоне концентраций от 0,0050 до 2,500 мкг/мл.
Установлено, что зависимость площади пика СО госсипола от его концентрации имеет линейную зависимость во всем диапазоне исследуемых концентраций госсипола (рис.4).
На основании этих данных показатель предела обнаружения был принят равным 0,003 мкг/мл, а нижний предел количественного определения (ПКО) свободного госсипола составил 0,01 мкг/мл.
Правильность методики устанавливали методом добавок с использованием 3 испытуемых модельных растворов смеси растертых таблеток «Кагоцел» с добавлением к ним в соотношении 1:1 об. возрастающих количеств СО госсипола. При этом использовали модельные смеси с концентрациями специфической примеси 50, 100, 150% от установленного верхнего значения максимально зарегистрированного содержания госсипола в таблетках «Кагоцел» (0,12 мкг в одной таблетке). Всего было приготовлено и проанализировано 9 образцов. Согласно полученным данным (табл. 2), открываемость находится в пределах установленной для валидационных испытаний нормы.
| Концентрация госсипола в испытуемом растворе, мкг/мл | Добавлено раствора СО с концентрацией, мкг/мл | Ожидаемое значение (В), мкг/мл | Полученное значение (А), мкг/мл | Абсолютная ошибка, мкг/мл | R, % |
|---|---|---|---|---|---|
| 0,254 | 0,100 | 0,177 | 0,178 | 0,001 | 100,7 |
| 0,254 | 0,300 | 0,277 | 0,295 | 0,018 | 106,5 |
| 0,311 | 0,400 | 0,355 | 0,388 | 0,032 | 109,1 |
| 0,311 | 0,100 | 0,205 | 0,217 | 0,012 | 105,7 |
| 0,291 | 0,300 | 0,296 | 0,285 | -0,011 | 96,4 |
| 0,291 | 0,400 | 0,346 | 0,365 | 0,020 | 105,7 |
| 0,291 | 0,100 | 0,196 | 0,190 | -0,006 | 96,9 |
| 0,291 | 0,300 | 0,296 | 0,269 | -0,027 | 90,9 |
| 0,338 | 0,400 | 0,369 | 0,370 | 0,001 | 100,1 |
| Среднее значение выхода, % | 101,3 | ||||
Аналогичным образом оценка показателя правильности применительно к анализу искусственных смесей модельных сред с добавленными количествами (от 0,2 до 0,5 мкг/мл) раствора СО госсипола показала достаточный уровень открываемости (табл 3).
| Название | № | Среда | Среда с добавкой СО госсипола (процент восстановления, R%) |
|---|---|---|---|
| Имитатор желудочного сока | 1 | Не обнаружено | 92,3 |
| 2 | То же | 93,8 | |
| Среднее | –»– | 93,1 | |
| Имитатор кишечного сока | 1 | –»– | 109,8 |
| 2 | –»– | 106,8 | |
| Среднее | –»– | 108,3 | |
| Среда с целлюлазой | 1 | –»– | 99,1 |
Прецизионность методики оценивали по показателям сходимости и воспроизводимости метода, коэффициенты вариации которых по 6 измерениям составили 4,32 и 5,05% соответственно, что удовлетворяет установленным критериям для этих показателей.
Как показали результаты проведенных исследований, предлагаемая методика признана удовлетворяющей установленным ГФ XIII валидационным критериям (табл. 4).
| Параметр | Оценка | Пояснение |
|---|---|---|
| Специфичность | Положительно | Время удерживания (tr): 7,759±0,015 |
| Линейность | То же | Коэффициент корреляции (R2): 0,99918. Степень аппроксимации: хорошая |
| Правильность (точность) | –»– | Диапазон процента восстановления (R%): 90,9–109,1 |
| Сходимость (повторяемость) | –»– | Коэффициент вариации (СV, %): 4,32 |
| Воспроизводимость | –»– | Коэффициент вариации (CV, %): 5,05 |
Анализ возможности высвобождения свободного госсипола из препарата «Кагоцел» при инкубации в модельных средах
В соответствии с описанными условиями (см. раздел «Материал и методы») в ходе испытания отбор проб осуществляли сразу после добавления испытуемого образца порошка таблеток «Кагоцел» в модельные среды, а также через 3 и 24 ч инкубации. Количество госсипола в препарате «Кагоцел» после воздействия модельных сред рассчитывали валидированным методом ВЭЖХ-МС. Результаты количественной оценки содержания свободного госсипола в составе всех испытанных модельных сред приведены в табл. 5.
| Модельная среда | Проба | Время инкубации, ч | ||
|---|---|---|---|---|
| 0 | 3 | 24 | ||
| Имитатор желудочного сока | 1 | 0,69 | 0,44 | 0,29 |
| Линейность | 2 | 0,54 | 0,29 | 0,17 |
| Правильность (точность) | Среднее | 0,62 | 0,36 | 0,23 |
| Имитатор кишечного сока | 1 | 1,21 | 0,61 | 0,47 |
| 2 | 1,04 | 0,57 | 0,22 | |
| Среднее | 1,13 | 0,59 | 0,34 | |
| Среда с целлюлазой | 1 | 0,82 | 0,66 | 0,42 |
| 2 | 0,88 | 0,67 | 0,43 | |
| Среднее | 0,85 | 0,67 | 0,42 | |
Результаты экспериментов с применением стандартных, рекомендованных ведущими фармакопеями модельных сред, имитирующих пищеварительные соки человека (ИЖС, ИКС), подтвердили, что при длительном (до 24 ч) воздействии на препарат модельных сред количество госсипола в растворе не возрастало. Воздействие на препарат «Кагоцел» (активное вещество — субстанция на основе окисленного производного КМЦ) модельной среды с добавлением комплекса микробных ферментов — целлюлазы, β-глюканазы и ксиланазы — также не сопровождалось увеличением в среде количества свободного госсипола.
Заключение
Отработана и валидирована в соответствии с современными фармакопейными требованиями ВЭЖХ-МС методика определения примесей свободного госсипола в препарате таблеток «Кагоцел». Методика характеризуется высокой чувствительностью (порог количественного определения – 0,01 мкг/мл) и специфичностью. Подтверждены условия выполнения методики для выявления госсипола в сложных по составу модельных (имитационных) средах.
В процессе длительной (до 24 ч) инкубации препарата «Кагоцел» в модельных средах, имитирующих пищеварительные соки человека, а также в среде, содержащей активную микробную целлюлазу, не выявлено увеличения содержания примесей свободного госсипола.
Работа выполнена с использованием научного оборудования Центра коллективного пользования «Промышленные биотехнологии» и АЦКП «Биоинженерия» Федерального исследовательского центра Биотехнологии РАН.