Гозерелин или золадекс что лучше
Золадекс : инструкция по применению
Состав
Одна капсула содержит:
Активное вещество: гозерелина ацетат 3.6 мг (в пересчете на гозерелин- основание) Вспомогательные вещества: молочной и гликолевой кислот сополимер (50:50) до общей массы 18,0 мг.
Описание
Белого или почти белого со светло-коричневым оттенком цвета капсула из твердого полимерного материала, свободного или практически свободного от видимых включений.
Гозерелина ацетат диспергирован в подвергающейся биологической деградации матрице, состоящей из лактидо-гликолидного сополимера. Поставляется со шприцем- аппликатором разовой дозы с защитным механизмом (Система безопасного введения Safety Glide).
Фармакологическое действие
Золадекс является синтетическим аналогом природного ЛГРГ (рилизинг гормон лютеинизирующего гормона). При постоянном применении Золадекс ингибирует выделение гипофизом ЛГ, что ведет к снижению концентрации тестостерона в сыворотке крови у мужчин и концентрации эстрадиола в сыворотке крови у женщин. Данный эффект обратим после отмены терапии. На первоначальной стадии Золадекс, подобно другим агонистам ЛГРГ, может вызывать временное увеличение концентрации тестостерона в сыворотке крови у мужчин и концентрации эстрадиола в сыворотке крови у женщин. На ранних стадиях терапии Золадексом у некоторых женщин могут отмечаться вагинальные кровотечения различной продолжительности и интенсивности.
У мужчин примерно к 23 дню после введения первой капсулы концентрация тестостерона снижается до кастрационных уровней и продолжает оставаться лечении, проводимом каждые 28 дней.
Остается сниженной до уровня сравнимого с тем, что наблюдается у женщин в менопаузе. Данное снижение приводит к положительному эффекту при гормонально-зависимых формах рака молочной железы, эндометриозе, фибромах матки и подавлении развития фолликулов в яичниках. Это также вызывает истончение эндометрия и является причиной возникновения аменореи у большинства пациенток.
Показано, что Золадекс в комбинации с препаратами железа вызывает аменорею и повышение уровня гемоглобина и соответствующих гематологических параметров у женщин с фибромами матки и сопутствующей анемией.
На фоне приёма агонистов ЛГРГ у женщин может иметь место наступление менопаузы. Редко, у некоторых женщин не происходит восстановления менструаций после окончания терапии.
Фармакокинетика
Введение капсулы каждые четыре недели обеспечивает поддержание эффективных концентраций. Кумуляции в тканях при этом не происходит. Золадекс плохо связывается с белком, и период полувыведения его из сыворотки крови составляет 2-4 часа у больных с нормальной функцией почек. Период полувыведения увеличивается у больных с нарушениями почечной функции. При ежемесячном введении препарата данное изменение не будет иметь значительных последствий, поэтому изменять дозу для данных пациентов не требуется. У больных с печеночной недостаточностью значительных изменений в фармакокинетике не наблюдается.
Показания к применению
(I) Лечение рака предстательной железы в следующих условиях:
• При лечении метастатического рака предстательной железы, при котором Золадекс продемонстрировал преимущество для выживаемости, сравнимое с хирургической кастрацией.
• При лечении локального рака предстательной железы, в качестве альтернативы хирургической кастрации, при котором Золадекс продемонстрировал преимущество для выживаемости, сравнимое с антиандрогенами.
• Как адъювантная терапия при лучевой терапии у пациентов с локализованным высокого риска или локальным раком предстательной железы, при которой Золадекс продемонстрировал увеличение выживаемости без болезни и общей выживаемости.
• Как неоадъювантная терапия, предшествующая лучевой терапии у пациентов с локализованным высокого риска или локальным раком предстательной железы, при которой Золадекс продемонстрировал увеличение выживаемости без болезни.
(II) Рак груди на поздних стадиях у женщин в пре- и перименопаузе, подходящий для гормонального воздействия.
(III) Золадекс 3,6 мг показан как альтернатива химиотерапии в стандарте лечения женщин в пре- и перименопаузе с чувствительным к эстрогену раку груди на ранних стадиях.
Эндометриоз: при ведении эндометриоза Золадекс облегчает симптомы, включая боль, и сокращает размер и количество эндометриальных пор
Истончение эндометрия: Золадекс показан для предварительной матки перед его хирургической абляцией.
(I) Фибромы матки: в сочетании с лечением препаратами железа для улучшения гематологического состояния пациентов с анемией до хирургического вмешательства.
(II) Вспомогательная репродукция: низкоуровневая регуляция гипофиза в подготовке к гиперовуляции.
Противопоказания
— Повышенная чувствительность к гозерелину или другим аналогам ЛГРГ
— Беременность и лактация
Беременность и период лактации
Способ применения и дозы
Одну капсулу (3,6 мг) препарата Золадекс вводят подкожно в переднюю брюшную стенку каждые 28 дней. Для пациентов с почечной или печеночной недостаточностью, а также для пациентов пожилого возраста нет необходимости корректировать дозу.
Эндометриоз можно лечить не более 6 месяцев, поскольку отсутствуют клинические данные относительно более длительных периодов применения. Повторные курсы терапии проводить не следует в связи с опасностью потери части минеральных компонентов и уменьшения плотности костной ткани. Было продемонстрировано, что у пациенток, получавших Золадекс для лечения эндометриоза, дополнительная заместительная гормонотерапия (ежедневный прием эстрогенных и прогестагенных препаратов) уменьшила потерю минеральной плотности костной ткани и выраженность вазомоторных симптомов.
Для истончения эндометрия курс лечения длится четыре или восемь недель. Может потребоваться введение второй капсулы пациенткам с большой маткой или для обеспечения гибкого графика подготовки хирургической операции.
Для женщин с анемией в результате фибромы матки может вводиться капсула Золадекс 3,6 мг с добавлением железа в течение до 3 месяцев до проведения хирургической операции. Экстракорпоральное оплодотворение: Золадекс 3,6 мг назначают для десенсибилизации гипофиза, которая определяется по концентрации эстрадиола в сыворотке крови и должна отвечать такой, какая существует на ранней фолликулярной фазе (приблизительно 150 пмоль/л). Это, как правило, происходит между 7-м и 21-м днем менструального цикла.
Суперовуляцию (контролируемую стимуляцию яичников) с помощью гонадотропина начинают, когда уже достигнута десенсибилизация. Десенсибилизация, вызванная введением агониста ЛГ-РГ (Золадекс), является более стойкой, поэтому в некоторых случаях может возникнуть потребность повысить дозу гонадотропина. На соответствующей стадии развития фолликулы введение гонадотропина прекращают, а в дальнейшем вводят хорионический гонадотропин человека для индукции овуляции. Контроль лечения, процедуры получения ооцита и оплодотворения проводят в соответствии с обычной практикой каждого отдельного клинического учреждения.
Побочное действие
Следующие категории по частоте возникновения неблагоприятных побочных реакций основаны на данных клинических исследований, анализа постмаркетингового периода и информации из спонтанных отчётов. Наиболее часто встречающимися побочными реакциями являются приливы крови, повышенное выделение пота и состояние мест введения лекарственного средства.
Для классификации побочных реакций по частоте используется следующая шкала: Очень част (>1 /10), Часто (>1/100 до 1/1000 до 1/10000 до
Передозировка
Опыт передозировки препарата у людей ограничен. В случае непреднамеренного введения Золадекса прежде срока или в более высокой дозе не отмечалось клинически значимых нежелательных явлений. Данных относительно передозировки у людей не имеется. В случае передозировки больному следует назначить симптоматическое лечение.
Взаимодействие с другими лекарственными средствами
Особенности применения
Меры предосторожности
Золадекс не показан для лечения детей, поскольку безопасность и эффективность препарата у этой группы пациентов не установлены.
Золадекс следует назначать с осторожностью мужчинам, у которых существует риск развития непроходимости мочеточников или сдавливания спинного мозга. Необходимо проводить систематическое наблюдение этой категории больных в течение первого месяца терапии. В случае возникновения компрессии спинного мозга или непроходимости мочеточников назначают обычное для данных осложнений лечение.
Следует рассмотреть необходимость начального применения анти-андрогенов (например, ципротерона ацетата 300 мг в день в течение трёх дней до и трёх недель после начала терапии Золадексом) в начале терапии аналогами ЛГ-РГ, поскольку имеются сообщения, что это препятствует возможным осложнениям в связи с первоначальным повышением сывороточной концентрации тестостерона.
Применение агонистов ЛГ-РГ может вызвать снижение минеральной плотности костной ткани. По имеющимся предварительным данным у мужчин, которые применяют бифосфонат в сочетании с агонистами ЛГ-РГ, снижение минеральной плотности костной ткани может замедляться. Особую осторожность следует проявлять пациентам с дополнительным фактором риска в виде остеопороза (например, у лиц, хронически злоупотребляющих алкоголем, курильщиков, проходящих длительный курс терапии противосудорожными средствами или кортикостероидами, с остеопорозом в семейном анамнезе).
Имеются сообщения о случаях резкой перемены настроения и депрессии. Необходимо вести постоянное наблюдение за пациентами с известным депрессивным состоянием и гипертензией.
У мужчин, применявших агонисты ЛГ-РГ, наблюдались случаи снижения толерантности к глюкозе. Это может свидетельствовать о диабете или потере гликемического контроля у пациентов, у которых до этого уже был сахарный диабет. В этих случаях-необходимо контролировать уровень глюкозы в крови.
При раке молочной железы
Предварительные данные указывают на то, что сочетание Золадекса с тамоксифеном у пациентов с раком молочной железы может замедлить снижение минеральной плотности костной ткани.
Снижение минеральной плотности костной ткани:
Применение агонистов ЛГ-РГ может стать причиной снижения минеральной плотности костной ткани в среднем на 1% в месяц в течение шестимесячного курса лечения. Каждые 10% снижения минеральной плотности костной ткани примерно в 2-3 раза повышают риск перелома костей. У большинства женщин, по имеющимся на сегодняшний день данным, после прекращения курса терапии наблюдается восстановление минеральной плотности костной ткани.
У пациентов, получающих Золадекс для лечения эндометриоза, добавление гормонозамещающей терапии замедляет снижение минеральной плотности костной ткани и уменьшает вазомоторные симптомы.
Отсутствуют какие-либо конкретные данные о пациентах с установленным остеопорозом или факторами риска возникновения остеопороза (например, злоупотребление спиртными напитками, курение, длительная терапия лекарственными средствами, вызывающими снижение минеральной плотности костной ткани, например, противосудорожными кортикостероидами, наличие остеопороза в семейном анамнезе, расстройство пищеварения, например, анорексия нервоза).
Поскольку снижение минеральной плотности костной ткани у этих пациентов носит более неблагоприятный характер, решение о назначении лечения Золадексом должно приниматься в индивидуальном порядке, и само лечение должно начинаться только после тщательной оценки возможного соотношения пользы и риска. Следует предусматривать дополнительные меры противодействия снижению минеральной плотности костной ткани.
На ранних стадиях лечения Золадексом у некоторых женщин наблюдались вагинальные кровотечения различной продолжительности.
Для выведения эстрогена. Ожидается, что кровотечение должно прекратиться самопроизвольно. Если кровотечение продолжается, необходимо установить его причины.
Клинические данные об эффектах лечения гинекологических состояний Золадексом в течение периода времени свыше 6-ти месяцев отсутствуют.
Применение Золадекса может приводить к повышению цервикальной резистентности, необходимо соблюдать осторожность при дилатации шейки матки.
Золадекс должен применяться при экстракорпоральном оплодотворении только под наблюдением специалиста, имеющего опыт в этой области.
Как и в случае других аналогов ЛГРГ, при применении Золадекса 3,6 мг в комбинации с гонадотропином сообщалось о случаях развития синдрома гиперстимуляции яичников (СГСЯ). Необходимо тщательно следить за циклом стимуляции, чтобы выявить пациенток с риском развития СГСЯ. Если такой риск существует введение хорионического гонадотропина человека необходимо прекратить, если это требуется.
Рекомендуется с осторожностью применять Золадекс при экстракорпоральном оплодотворении у пациенток с синдромом поликистозных яичников, так как возможна активация большого количества фолликулов.
Фертильные женщины во время лечения Золадексом и до возобновления менструаций после прекращения курса терапии Золадексом должны использовать негормональные методы контрацепции.
Необходимо внимательно следить за состоянием пациентов с известной депрессией или гипертензией. Лечение Золадексом может давать положительный результат тестов на допинг.
Форма выпуска
Капсула по 3.6 мг для подкожного введения пролонгированного аппликаторе с защитным механизмом (Система безопасного введение Один шприц-аппликатор помещается в ламинированный алюмиш помещается в картонную пачку с инструкцией по применению.
Лечение первично выявленного распространенного рака предстательной железы
Глава 9. Лечение первично выявленного распространенного рака предстательной железы
Тестостерон. Яички продуцируют около 95% всех андрогенов в виде тестостерона. В яичках он продуцируется клетками Лейдига в ответ на стимуляцию лютеинизирующим гормоном (ЛГ), который секретирует аденогипофиз в ответ на высвобождение рилизинг гормона лютеинизирующего гормона гипоталамуса. Соотношение гормонов определяется состоянием гипоталамо-гипофизарно-тестикулярной системы (рис. 20).
Рис. 20. Продукция тестостерона. Гипоталамо-гипофизарно-тестикулярная ось.
Механизм отрицательной обратной связи заключается в том, что при снижении уровней тестостерона гипоталамус высвобождает ЛГРГ, который в свою очередь стимулирует секрецию ЛГ, и, в конце концов, повышается секреция тестостерона. Механизм обратной связи приводит к возрастанию концентрации тестостерона, при этом уменьшаются выбросы ЛГРГ гипоталамусом.
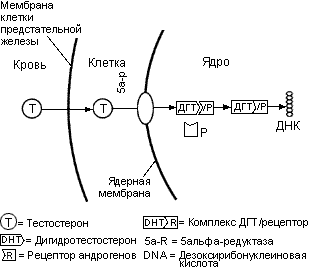
Большая доля циркулирующего тестостерона в крови связана глобулином, связывающим половые гормоны (ГСПГ), и альбумином. Небольшая часть (2-3%) циркулирующего тестостерона не связана и, как считается, является функционально-активной формой тестостерона, который проникает в ткани предстательной железы. Свободный тестостерон пересекает мембрану клетки предстательной железы, а затем в цитозоле ферментом 5альфа-редуктазой превращается в ДГТ (рис. 21).
Рисунок 21. Механизм стимуляции функции клеток предстательной железы андрогенами.
Современные концепции лечения распространенного рака предстательной железы. Вопросы лечения гормонально-зависимых опухолей предстательной железы не могут решаться однозначно в связи со значительными изменениями, происходящими в организме больного. Это выдвигает необходимость всестороннего подхода к проблеме лечения рака предстательной железы, которая содержит еще целый ряд противоречивых вопросов.
Несмотря на то, что с тех пор, как Huggins и Hodges показали гормональную зависимость рака предстательной железы, прошло уже более 50 лет, гормонотерапия остается ведущим методом лечения распространенных форм этой опухоли. Однако эффект лечения в этих случаях временный. При наличии отдаленных метастазов рецидив заболевания возникает обычно в течение первых двух лет, а продолжительность жизни после появления рецидива обычно исчисляется месяцами. Сразу после внедрения гормонотерапии в клиническую практику начались споры об оптимальном времени ее проведения. В настоящее время гормонотерапию при распространенном раке предстательной железы стараются назначать как можно раньше в надежде на более позднее появление болевого симптома и увеличение продолжительности жизни. Однако правильность такого подхода ставится под сомнение некоторыми исследователями (Lepor Н., et al., 1982).
В 1985 году было начато исследование по сравнению немедленной и отсроченной гормонотерапии у больных с бессимптомным течением диссеминированного и местно-распространенного рака предстательной железы (Рабочая группа по изучению рака предстательной железы Совета по исследованиям в медицине, Англия). Набор больных был прекращен в конце 1993 года. Предварительные результаты этой работы были опубликованы в 1997 году. Авторы исследования получили данные о 934 больных. В группе больных, которым гормонотерапия проводилась отсрочено, 51 больной умер от сопутствующих заболеваний еще до начала лечения (только пять из этих больных были моложе 70 лет), еще 29 больных умерли до начала лечения от основного заболевания. Показанием для начала лечения одинаково часто служили как рост первичной опухоли, так и отдаленные метастазы. Появление отдаленных метастазов и боли в костях чаще наблюдались у больных, которым гормонотерапия проводилась отсрочено (р 0.033).
Гозерелин ацетат (Золадекс) в сочетании с заместительной
| Несмотря на данные преимущества, широкое применение а-ГнРГ ограничено такими гипоэстрогенными эффектами, как вазомоторная симптоматика, сухость влагалища, эмоциональная нестабильность, бессонница и снижение минеральной плотности костей. Выраженность побочных эффектов, в частности снижение плотности костной ткани, накладывает определенные ограничения на продолжительность назначения а-ГнРГ при лечении многих гинекологических заболеваний. Для уменьшения побочных эффектов рекомендуется дополнять лечение препаратами а-ГнРГ назначением заместительной гормональной терапии (ЗГТ). Обоснованием данного подхода служит гипотеза “пороговой концентрации эстрогенов”, согласно которой концентрация эстрогенов в пределах определенного диапазона может частично предотвращать снижение плотности костной ткани и в тоже время не оказывать стимулирующего эффекта на рост эндометриоидных имплантатов. |
Комбинация медроксипрогестерон-ацетата (МПА) или норэтинодрона с а-ГнРГ устраняет вазомоторную симптоматику и уменьшает выраженность деминерализации костной ткани, но непрерывное введение МПA ослабляет положительные эффекты терапии а-ГнРГ, а норэтинодрон оказывает еще и неблагоприятное влияние на липидный профиль.
Недавно были проведены два исследования для оценки фоновой (add-back) терапии эстрогенами и прогестагенами при лечении а-ГнРГ пациенток с эндометриозом. В одном из них авторы не обнаружили различий в эффективности лечения гозерелином (Золадексом) и сочетанием гозерелина и ЗГТ (подкожное введение низкодозированного 17b-эстрадиола по 25 мкг два раза в неделю и 5 мг МПА), в то время как, использование фоновой ЗГТ привело к значительному снижению числа пациенток с такими побочными явлениями, как приливы и снижение либидо. Аналогично в другом исследовании с плацебо-контролем оказалось, что сочетание гозерелина с ЗГТ (прием внутрь 2 мг Е2 и 1 мг норэтистерона ацетата) не снижает его эффективности и одновременно уменьшает выраженность побочных эффектов терапии а-ГнРГ. Хотя ЗГТ эстрогенами и прогестагенами остается многообещающей терапевтической стратегией, для определения наиболее оптимальных комбинированных режимов лечения пациенток с эндометриозом необходимы дополнительные исследования.
Мы провели подобное исследование для оценки эффективности и переносимости лечения гозерелином в сочетании с двумя режимами ЗГТ. В качестве эстрогенного компонента ЗГТ использовались две различных дозы конъюгированных эстрогенов (0,3 и 0,625 мг в день); в качестве прогестагенного компонента в обоих режимах использовался МПА (5 мг в день). Исследование проводилось с целью определить, является ли сочетание гозерелина с ЗГТ столь же эффективным в отношении уменьшения тазовых симптомов эндометриоза, что и лечение одним гозерелином, и способствует ли комбинированная терапия сокращению количества побочных явлений, таких как снижение плотности костной ткани, вызванных использованием а-ГнРГ.
Проведено рандомизированное контролируемое многоцентровое исследование состояния пациенток во время 24-недельного курса лечения Золадексом и в течение 48 недель после его окончания. В исследовании участвовали 345 женщин из 42 центров.
Требования для участия в исследовании
Женщины в пременопаузе, в возрасте от 18 до 45 лет с подтвержденным диагнозом наружного генитального эндометриоза.
Диагноз наружного генитального эндометриоза I—IV степени был подтвержден с помощью лапароскопии до начала исследования.
Если лапароскопия включала в себя хирургическое вмешательство, пациентки должны были первоначально иметь клинический ответ, а затем рецидив и стабильную тяжесть тазовой симптоматики в течение более чем 3 месяца до начала исследования.
Исключение из наблюдения
-Положительный тест на беременность.
-Беременность и лактация.
-Использование гормональных препаратов, не входящих в данный курс, таких как эстрогены, прогестагены или кломифен в течение 60 дней до начала лечения и в течение всего периода наблюдения.
-Использование лекарственных препаратов в концентрациях, подавляющих функцию гипоталамо-гипофизаро-надпочечниковой системы.
-Серьезные сопутствующие заболевания.
-Длительное лечение (более 3-х месяцев) а-ГнРг за 12 месяцев до начала данного курса.
-Исходное значение минеральной плотности костной ткани более чем на 2 SD меньше среднего для женщин данного возраста.
-Гиперчувствительность к гормонотерапии или к заместительной гормональной терапии эстрогенами или прогестогенами.
-Любые условия, которые являются противопоказанием для получения данного курса лечения.
Все пациентки были разделены случайным образом на три группы. Пациентки группы HRT0 получали одну инъекцию (3,6 мг) гозерелина (Золадекса) каждые 28 дней и однократно суточную дозу плацебо конъюгированных эстрогенов (0,3 мг) и плацебо МПА. Пациентки группы HRT1 получали каждые 28 дней одну инъекцию (3,6 мг) гозерелина и однократную суточную дозу 0,3 мг конъюгированных эстрогенов (Premarin; Wyeth Ayerst, Philadelphia) и 5 мг МПА (Provera; Upjon, Kalamazoo, MI). Пациентки группы HRT2 получали каждые 28 дней одну инъекцию (3,6 мг) гозерелина и однократную суточную дозу 0,625 мг конъюгированных эстрогенов и 5 мг МПА.
Гозерелин вводили подкожно в переднюю брюшную стенку первый раз между 1 и 5 днем менструального цикла, а затем каждые 28 дней. Пациентки начинали прием конъюгированных эстрогенов и МПА или их плацебо на 15 день менструального цикла, затем продолжали принимать их ежедневно один раз в сутки в течение 24-недельного курса лечения.
Пациенток опрашивали до начала лечения о наличии субъективных тазовых симптомов эндометриоза (дисменорея, диспареуния и тазовые боли). Также проводили оценку объективного состояния органов малого таза (болезненность и наличие уплотнений в области малого таза). Тазовые симптомы оценивали по трехбалльной шкале в зависимости от их выраженности: 0= “отсутствие”; 1= “слабые”; 2 = “умеренные”; 3 = “сильные”. Результаты оценивали в соответствии с балльной шкалой, принятой в ранних исследованиях эффективности лечения гозерелином больных эндометриозом. Сумма баллов каждого из трех субъективных симптомов и двух объективных тазовых симптомов составила общий показатель для каждой обследуемой пациентки.
Предполагалось, что пациентка имеет признаки эндометриоза, если общий показатель тазовых симптомов составляет 3 и более, причем один из симптомов имеет степень выраженности 2 и более балла. Те же тазовые симптомы оценивались во время курса лечения (на 4-й, 8-й, 12-й, 16-й, 20-й и 24-й неделе) и после его окончания (на 36-й, 48-й и 72-й неделе). Кроме того, во время каждого визита в истории болезни делали запись о датах менструального кровотечения.
Первую (диагностическую) лапароскопию выполняли в течение 24 месяцев до начала лечения. Степень выраженности эндометриоза оценивали в баллах по шкале R-AFS (пересмотренная классификация Американского общества фертильности). Оценка производилась до и после проведения лапароскопии. При необходимости производили выскабливание.
С помощью рентгеновской абсорбциометрии определяли массу 2—4 поясничных позвонков, или, если этот метод был недоступен, использовали фотонную абсорбциометрию. Измерения проводили после первой лапароскопии, но до первой инъекции гозерелина. Определение минеральной плотности костной ткани повторяли в течение всего курса лечения (на 12-й и 24-й неделях) и после его окончания (на 48-й и 72-й неделях).
При каждом визите пациенток опрашивали о наличии или отсутствии пяти побочных эффектов применения а-ГнРГ (сухость влагалища, депрессия, смена настроений, головные боли и приливы). Также регистрировались все другие побочные эффекты, обнаруженные при опросе.
Инструментальное обследование проводили перед началом лечения, затем с периодичностью 1 раз в 4 недели первые 24 недели курса, и 1 раз в 12 недель после его окончания и до 72 недели. Образцы крови отбирались перед началом лечения, в первый день, на 4-й и 24-й неделях лечения, и на 36-й и 72-й неделях после окончания курса; проводили биохимический анализ (сывороточные трансаминазы, общий билирубин, лактатдегидрогеназа, щелочная фосфатаза, мочевина, глюкоза, кальций, креатинин, холестерин, липопротеины низкой и высокой плотности, триглицериды, фосфаты, натрий, калий и общий белок), клинический анализ (гемоглобин, гематокрит, лейкоциты, тромбоциты) и анализ крови и мочи на беременность.
Из 345 пациенток было сформировано три рандомизированные группы следующего численного состава: HRT0—119, HRT1—113, HRT2—113. Демографические характеристики были сбалансированы между группами. 306 пациенток завершили курс лечения (HRT0—109, HRT1—99, HRT2—98), 39 — были исключены из наблюдения (HRT0—10, HRT1—14, HRT2—15). Причинами исключения из исследования во время курса лечения были прерывание лечения (n=24), решение врача-исследователя (n=4), побочные эффекты (n=3), беременность (n=1), другие причины (n=7). Три пациентки (по одной из каждой группы) завершили курс лечения, но после его окончания не захотели продолжать наблюдение у врача. 144 пациентки наблюдались после окончания курса терапии гозерелином (HRT0—54, HRT1—46, HRT2—44), 159 пациенток были исключены из наблюдения после окончания курса (HRT0—54, HRT1—52, HRT2—53). Причинами исключения из исследования в этом случае были использование препаратов, запрещенных в данном клиническом исследовании (n=67), отказ от наблюдения (n=42), решение врача-исследователя (n=1), побочные эффекты (n=1), беременность (n=33), другие причины (n=15).
Суммарная доза гозерелина была одинаковой во всех трех группах. Среднее количество инъекций на пациентку составило 5,8 для группы HRT0, 5,6 для группы HRT1, 5,6 для группы HRT2.
Объективные и субъективные тазовые симптомы
На фоне лечения гозерелином во всех трех группах снизился общий показатель объективных тазовых симптомов эндометриоза. Значимые различия между режимами лечения в течение 72-недельного клинического наблюдения были обнаружены только на 12-й неделе, когда среднее значение показателя для группы HRT1 составляло 4,4 балла (P=0,027), а для HRT2 (P=0,03) — 3,5, и на 16-й неделе, среднее значение показателя для группы HRT2 было равно 3,4 балла, в отличие от 4,1 — для HRT0 (P=0,034) и 4,2 — для HRT1 (P=0,019).
Также наблюдалось снижение общего показателя субъективных симптомов эндометриоза во всех трех группах пациенток. Характер кривых для данного показателя сходен с таковым для объективных тазовых симптомов; однако, на протяжении всего периода наблюдения не было выявлено статистически значимых различий по данному показателю для разных режимов терапии.
Минеральная плотность костной ткани
Для всех трех групп пациенток средний процент снижения плотности костной ткани изменялся в диапазоне от 0,8% до 2,1% на 12-й неделе, от 1,6% до 4,1% на 24-й неделе, от 1,2% до 2,8 % на 48-й неделе и от 0,5% до 1,7% на 72-й неделе. Процент снижения плотности костной ткани был достоверно выше в группе HRT0 по сравнению с HRT1 и HRT2. Не выявлено статистически значимых различий между группами HRT1 и HRT2.
Во время курса лечения группы HRT1 и HRT2 имели меньшую, чем HRT0 интенсивность снижения средней плотности костной ткани. После окончания терапии гозерелином показатели плотности костной ткани во всех трех группах выходили на исходный уровень. Статистический анализ влияния возраста женщин на плотность костной ткани не выявил различий между группами пациенток старше и младше 30 лет.
Средний показатель выраженности побочных эффектов, таких как приливы, сухость влагалища, депрессия, смена настроений, головные боли, значительно увеличился по сравнению с исходным уровнем к 8-й неделе лечения, оставался устойчивым до 24-й недели и быстро снижался до исходного уровня после 24-й недели. Исключение составил средний показатель выраженности головных болей — он медленно снижался в течение всего периода наблюдения после прекращения лечения.
Во время курса лечения наблюдали различия в выраженности сухости влагалища и приливов. Статистически значимые различия были обнаружены для среднего показателя сухости влагалища на 24-й неделе (p=0,007) и для приливов на 12-й (p меньше 0,001) и 24-й неделях (p меньше 0,001). На 24-й неделе в группе HRT0 процент пациенток с сухостью влагалища (51,4%) был выше, чем в группах HRT1 (39,4%) или HRT2 (25,5%). На 12-й неделе в группе HRT0 процент пациенток с приливами (94,8%) был выше, чем в группах HRT1 (56,2%) или HRT2 (45,2%). Подобные результаты наблюдались в группах и на 24-й неделе.
Во время курса лечения две пациентки из группы HRT0 и одна — из группы HRT2 были исключены из дальнейшего наблюдения из-за побочных эффектов. Обе пациентки жаловались на выраженные приливы, а одна из них — на тошноту. Пациентка из группы HRT2 была исключена из наблюдения в связи с жалобами на учащенное сердцебиение и повышение давления. Трех пациенток исключили из-за приема запрещенных в данном клиническом исследовании препаратов. После окончания курса лечения одна пациентка была исключена в связи с депрессией и попыткой суицида, не имеющих отношения к лечению.
Результаты лабораторных исследований
Данные клинического и биохимического анализа крови, а также анализа липидов были сравнительно одинаковыми для всех трех групп пациенток в период лечения гозерелином и во время последующего наблюдения. Наиболее часто встречающимся отклонением было увеличение уровня холестерина (37,4%) и триглицеридов (28,1%). Средний уровень холестерина изменялся в пределах от 174,2 мг/дл до 194,9 мг/дл, триглицеридов — от 88,5 мг/дл до 111,6 мг/дл. Для пациенток с нормальным исходным уровнем уровень холестерина в течение лечения был выше в группе HRT0 по сравнению с группами HRT1 и HRT2.
Число дней с мажущими, средними и интенсивными кровянистыми выделениями в течение периода менструаций слабо менялось по сравнению с исходным до 4 недели лечения, значительно снижалось к 8-й—24-й неделям лечения и быстро восстанавливалось на исходный уровень после прекращения лечения. К 8-й неделе курса число дней с мажущими кровянистыми выделениями было значительно больше в группе HRT2 (4,5) по сравнению с группами HRT0 (0,8) и HRT1 (2,3). На среднее число дней мажущих кровянистых выделений в группе HRT2 оказывали сильное влияние несколько пациенток, у которых наблюдались кровянистые выделения на 8-й и 16-й неделях курса. За исключением 8-й недели, характер изменения менструаций был одинаковым во всех трех группах пациенток.
Проведенное клиническое исследование показало, что сочетание гозерелина с ЗГТ не изменяет эффективность препарата в отношении уменьшения объективных и субъективных признаков эндометриоза и уменьшает интенсивность снижения плотности костной ткани и выраженность связанных с лечением а-ГнРГ побочных эффектов, таких как приливы и сухость влагалища. В отличие от большинства работ по изучению фоновой заместительной гормонотерапии при лечении гозерелином, в данном исследовании пациентки получали ЗГТ с начала курса лечения а-ГнРГ, а не по прошествии нескольких месяцев. Согласно полученным данным, назначение ЗГТ в начале курса лечения а-ГнРГ не оказывает влияния на эффективность лечения.
Степень уменьшения субъективных и объективных тазовых симптомов эндометриоза не отличалась для разных доз эстрогенов (0,3 мг — HRT1 и 0,625 мг — HRT2), в то время как интенсивность снижения плотности костной ткани была меньше для группы пациенток, получавших эстрогены по 0,625 мг/сут. Однако, данное различие между двумя режимами дозирования эстрогенов не было статистически достоверным.
В заключение следует отметить, что сочетание ЗГТ с лечением гозерелином значительно уменьшает интенсивность снижения плотности костной ткани и выраженность некоторых побочных явлений, возникающих на фоне терапии а-ГнРГ. Подключение ЗГТ с начала курса лечения гозерелином не снижает его эффективности. Таким образом, представляется разумным использование ЗГТ с начала курса лечения а-ГнРГ больных, страдающих эндометриозом. Полученные данные подтверждают, что курс а-ГнРГ и ЗГТ продолжительностью 6 месяцев является эффективным, хорошо переносимым видом медикаментозного лечения эндометриоза. Для оценки отдаленных результатов лечения требуются дополнительные клинические исследования.