Группа риска гси что это
Группа риска гси что это
О частоте внутриутробного (эндогенного) инфицирования новорожденных возбудителями гнойно-септических инфекций в акушерском стационаре
А.А. Хозяшева, В.И. Сергевнин, О.В. Чайкина
Медико-санитарная часть № 7 г. Перми
Пермская государственная медицинская академия
Известно, что гнойно-септичсские инфекции (ГСИ) новорожденных могут развиваться в результате постнатального (экзогенного) и внутриутробного (эндогенного) инфицирования. Постанатальное инфицирование возникает вследствие контакта новорожденного с источником возбудителя инфекции в условиях акушерского стационара. Внутриутробное инфицирование происходит от матери до родов (антенатально) или во время родов (интранатально). Очевидно, что профилактические мероприятия в отношении постнатальных и внутриутробных ГСИ принципиально различны. Между тем до настоящего времени четких критериев диагностики внутриутробных ГСИ не предложено, а частота их возникновения фактически не известна.
Целью работы явилось изучение частоты внутриутробного инфицирования новорожденных возбудителями ГСИ в акушерском стационаре.
Работа выполнена на базе акушерского стационара медсанчасти № 7 г.Перми в течение 1997 – 1999 гг. Бактериологически обследовано 2780 беременных, 2534 родильниц и 3423 новорожденных. У беременных исследовали мочу и мазок с цервикального канала, у родильниц – задние околоплодные воды и мазки с цервикального канала и последа, у новорожденных – мазки из ушной раковины и с кожи (непосредственно при рождении). Бактериологический анализ проводили на весь спектр аэробных и факультативно-анаэробных бактерий в соответствии с действующими инструкциями. Каждый случай ГСИ у новорожденного анализировали с учетом результатов комплексных бактериологических исследований, состояния здоровья матери, характера беременности и родов, времени появления и клинической картины заболевания.
Результаты бактериологических исследований показали, что пейзаж микроорганизмов, выделяемых от беременных, родильниц и новорожденных, в значительной степени совпадает (табл.)
Пейзаж микроорганизмов, выделенных от беременных, родильниц
и новорожденных (в % от общего количества микроорганизмов)
| Микроорганизмы | Беременные | Родильницы | Новорожденные |
| Грибы рода Candida | 33,0 | 30,0 | 13,0 |
| E. coli | 24,0 | 20,0 | 50,0 |
| S. aureus | 3,0 | 8,0 | 4,0 |
| S. epidermidis | 11,0 | 18,0 | 6,0 |
| S. pyogenes | 1,0 | 0 | 1,0 |
| S. faecalis | 8,0 | 8,0 | 9,0 |
| S. faecium | 15,0 | 12,0 | 8,0 |
| Klebsiella | 1,0 | 2,0 | 3,0 |
| Прочие | 4,0 | 2,0 | 6,0 |
| Итого | 100,0 | 100,0 | 100,0 |
Следует отметить, что в 59,0% случаев у родильниц в анамнезе фигурировали хронический пиелонефрит, кольпит, хламидиоз, венерические болезни и другие инфекции.
Представленные материалы свидетельствуют о том, что ГСИ новорожденных наиболее часто являются следствием внутриутробного (эндогенного) инфицирования. Отсюда очевидно, что в профилактике ГСИ новорожденных приоритетное место должны занимать мероприятия, направленные на нейтрализацию эндогенных факторов риска, т.е. на выявление и санацию очагов хронической и латентной инфекции у каждой беременной женщины.
Группы риска новорождённых
Группы риска
Критерии распределения новорождённых детей по группам риска.
Дородовый патронаж.
•Выявление факторов риска (сбор и оценка данных генеалогического, биологического и социального анамнезов);
•Прогноз состояния здоровья и развития будущего ребенка (группы риска);
• Проведение прогноза и профилактики гипогалактии;
•Информирование беременной о выявленном у будущего ребенка риске;
•Подбор рекомендаций по профилактике реализации выявленного риска (санитарно-гигиенические условия, режим дня и питание беременной женщины);
•Гигиеническое обучение и воспитание будущих родителей (пропаганда здорового образа жизни, положительный психологический настрой на рождение ребенка, формирование мотивации на длительное грудное вскармливание, посещение занятий в “Школе будущих родителей”);
•Определение срока второго дородового патронажа беременной.
•Второй дородовый патронаж осуществляется участковым педиатром и медсестрой на 32-34-й неделе беременности в период начала декретного отпуска женщины.
•Цель второго патронажа – контроль выполнения назначений врача женской консультации и педиатра, переоценка факторов и направленности риска, коррекция рекомендаций.
•Особое внимание уделяется посещению беременной “Школы матерей” и занятиям по психопрофилактической подготовке к родам.
Задачи второго патронажа
•Переоценка факторов и направленности риска (получение информации о течении беременности, перенесенных заболеваниях, применении медикаментов, изменении условий труда, быта, уточнение предполагаемого срока родов);
•Контроль выполнения предшествующих назначений и их эффективности;
•Проведение повторного прогноза гипогалактии и ее профилактика;
•Коррекция рекомендаций в соответствии с выявленным риском;
•Гигиеническое обучение и воспитание будущих родителей (подготовка молочных желез к лактации, подготовка семьи к встрече новорожденного).
•Окончательно группы риска для ребенка выставляются после первого патронажа участкового педиатра к новорожденному.
•Патронаж новорожденного ребенка в течение первого месяца жизни проводится врачом-педиатром и медицинской сестрой педиатрического участка. Кратность посещений определяется региональными нормативами.
•Патронаж детей первого года жизни осуществляется медицинской сестрой не реже одного раза в месяц, второго года жизни – ежеквартально, третьего года жизни – два раза в год.
•Цель такого патронажа состоит в оказании помощи матери при организации и проведении ухода за новорожденным. Важно научить ее правильно выполнять манипуляции по уходу за ребенком. Во время проведения первичного патронажа новорожденного медицинская сестра получает от врача ряд конкретных указаний по особенностям наблюдения за данным ребенком
Распределение новорождённых детей по группам риска.
Новорождённые дети из групп риска дополнительно к стандартным обследованиям (проводящимся всем здоровым детям) проходят следующие обследования и профилактические мероприятия:
I Группа риска – дети с риском заболевания ОРВИ
•Осмотр невролога в 1; 3; 6; 9; 12 месяцев
•Массаж, гимнастика, плавание
III Группа риска – дети с риском метаболических нарушений: рахит, анемия, гипотрофия, паратрофия
•ОАК в 1; 3; 6; 12 месяцев (контроль уровня гемоглобина)
•Контроль массо-ростовых показателей
•Профилактика нутритивной недостаточности (рациональное вскармливание, своевременное введение прикорма, профилактика белковой – энергетической недостаточности, рахита и анемии)
IV Группа риска – дети с риском врождённых пороков органов и систем
V Группа риска – дети с риском гнойно – септических заболеваний в период новорождённости
•После выписки из род.дома до 10 дня жизни ежедневный осмотр педиатра, затем 1 раз в неделю до 1 мес.
•Наблюдение за пупочной ранкой, кожными высыпаниями, характером стула, активностью ребёнка, прибавкой в весе
•Ежедневно 3 р/д измеряется температура тела ребёнка
•Госпитализация при гнойничковых кожных высыпаниях
VI Группа риска – дети с риском аллергических заболеваний
•Аллерголог – иммунолог в 3 месяца, далее по показаниям
•ОАК в 3; 12 месяцев, для выявления эозинофилии
•Гипоаллергенная диета кормящей матери
•Лекарственные препараты, фитопрепараты (лекарственные средства, получаемые исключительно из растительного сырья), лечебное питание (специализированные смеси), введение прикорма – только по назначению врача
•Исключение бытовых аллергенов
•Срок наблюдения до – 3-х лет
VII Группа риска – дети с неблагополучными социальными условиями
•До 10 дня жизни ежедневный осмотр педиатра, затем в 20 дней и 1 месяц, далее 2 раза в месяц
•Контроль за вскармливанием, гигиеной, прибавкой в весе, физическим и нервно – психическим развитием
•Обеспечение бесплатными медикаментами и питанием
•При заболеваниях – госпитализация в стационар
•ОАК; ОАМ; Копрограмма – ежегодно
•С 7 лет контроль АД
•Медосмотры с участием специалистов ( педиатр, ЛОР, хирург, окулист, стоматолог) в 1; 3; 5; 7; 10; 12; 14 – 15; 17 – 18 лет.
•Флюорография с 14 лет
•Наблюдение бессрочное: до того момента, как обстановка в семье и условия жизни ребёнка улучшатся.
VIII Группа риска – дети с риском развития тугоухости и глухоты
•Осмотр ЛОРа в 1; 4; 6; 12 месяцев, проведение звукореактотеста, при необходимости консультация сурдолога
•Избегать назначение аминогликозидов, ототоксичных препаратов.
•Срок наблюдения – до 18 лет.
После истечения срока наблюдения:
•Если у ребёнка не обнаружились отклонения в состоянии здоровья, он снимается с наблюдения по этой группе риска
•Если патология проявилась определёнными симптомами, то после обследования ребёнку выставляется конкретный диагноз и назначается лечение.
Внутрибольничные инфекции в родовспомогательных учреждениях
Опубликовано в журнале:
Сестринское дело »» №5-6 1998 Ежегодно в Российской Федерации регистрируется от 50 до 60 тысяч случаев внутрибольничных инфекций. В истекшем году было зарегистрировано 48,6 тысячи заболевших.
Как и в предыдущие годы, в общей структуре гнойно-септические инфекции (ГСИ), возникающие в родовспомогательных учреждениях, занимают первое место и составляют до 45% от общего числа зарегистрированных случаев внутрибольничных инфекций. Официальной регистрации подлежат ГСИ, возникающие среди новорожденных и родильниц, к которым прежде всего относятся такие тяжелые инфекции бактериальной природы, как бактериальный менингит, сепсис, остеомиелит новорожденных, а также перитонит, сепсис, эндометрит у рожениц.
В условиях работы родовспомогательного учреждения следует учитывать, что большинство возбудителей ВБИ относятся к условно-патогенным микроорганизмам, проявляющим свои свойства на фоне снижения неспецифических защитных сил организма. На этом фоне важное значение приобретает определение групп риска среди новорожденных и рожениц.
Распространению внутрибольничных инфекций способствует многообразие возбудителей (более 300 видов), формирование госпитальных штаммов, обладающих высокой устойчивостью к неблагоприятным факторам окружающей среды, в том числе к ультрафиолетовому излучению, высушиванию, лекарственной устойчивостью.
К группам риска среди рожениц относятся прежде всего женщины с хроническими соматическими и инфекционными заболеваниями, болезнями мочеполовой системы, с отягощенным акушерско-гинекологическим анамнезом (инфекционные осложнения при предыдущих беременностях, привычное невынашивание и др.), с кровотечением в послеродовом периоде и т.д. Кроме того, в последнее время участились случаи поступления в роддом женщин, не обращавшихся ни разу в женскую консультацию, т.е. у которых отсутствуют данные акушерского анамнеза.
Несмотря на то, что на долю вспышечной заболеваемости приходится 0,2-0,3% от общего числа зарегистрированных в указанных учреждениях случаев, число вспышек на протяжении последних лет не уменьшается. Так, в родовспомогательных учреждениях в 1997 году было зарегистрировано 9 вспышек, при которых пострадало 93 новорожденных и рожениц, из них один случай закончился летальным исходом. С начала 1998 года уже зарегистрировано 5 вспышек гнойно-септических инфекций среди новорожденных в родовспомогательных учреждениях страны.
Анализ заболеваемости в родовспомогательных учреждениях свидетельствует о том, что причины возникновения групповой заболеваемости связаны прежде всего с нарушением персоналом санитарно-гигиенического и противоэпидемического режимов, несвоевременным переводом заболевших новорожденных с признаками инфекционного заболевания в стационары II этапа выхаживания, отсутствием обследований на сальмонеллез, особенно в неблагополучных по этой инфекции территориях, женщин перед поступлением на роды. Источником инфекции может служить и персонал, который работает с признаками, к примеру, острой респираторной инфекции, что чаще всего выявляется только при проведении эпидемиологического расследования вспышки. Значительно реже в настоящее время констатируются случаи нарушения правил обработки и стерилизации инструментов.
Работа родовспомогательных учреждений в условиях отключения горячего водоснабжения, в период аварий на канализационных и водопроводных сетях недопустима. Такие чрезвычайные ситуации создают условия для распространения инфекции как среди новорожденных и рожениц, так и среди персонала.
Профилактика ВБИ невозможна без слаженной работы всех подразделений роддома. Особое место в структурных подразделениях занимает комната сбора и хранения грудного молока, где от четкой работы персонала зависит жизнь новорожденных. Инфицирование грудного молока при неправильном режиме обработки, приготовление молочных смесей с нарушением технологии может привести к развитию тяжелой инфекции у детей, т.к. грудное молоко и смеси являются благоприятной средой для развития микроорганизмов, относящихся к группе условно-патогенных (стафилококки, энтеробактерии, клебсиеллы), и патогенных (шигиллы, сальмонеллы, ротавирусы), которые чаще всего выделяются от больных, с предметов окружающей среды и от персонала при возникновении групповой заболеваемости. Многие из этих микроорганизмов приобрели свойства госпитальных штаммов, т.е. таких возбудителей, которые приобретают свойства устойчивости ко множеству антибиотиков и дезрастворам и прекрасно адаптировались к выживанию в условиях стационаров.
Это требует совершенствования мероприятий по профилактике ВБИ, что нашло свое отражение в приказе Минздрава России №345 от 26.11.97 «О совершенствовании мероприятий по профилактике внутрибольничных инфекций в акушерских стационарах».
Положения Приказа ориентируют на внедрение в родовспомогательных учреждениях новых технологий, направленных прежде всего на совместное пребывание матери и ребенка, раннее прикладывание к груди со свободным вскармливанием, раннюю (на 2-4-й день) выписку из стационара, что позволит максимально предотвратить риск заражения ВБИ. В настоящее время мы можем говорить, что эта работа находится на начальных этапах внедрения. Кроме того, особое внимание в приказе уделяется вопросу обработки рук персонала. Казалось, вопрос обработки рук освещается практически во всех документах, относящихся к работе лечебно-профилактических учреждений любого профиля. Но эта мера не утеряла свой значимости и в настоящее время. Многочисленные наблюдения и исследования свидетельствуют о недостаточном внимании со стороны персонала к этой важнейшей процедуре. Мытье рук после манипуляций, ведущих к их загрязнению, обязательно. Неукоснительное выполнение этих несложных правил в значительной мере предотвращает развитие тех или иных осложнений у рожениц и новорожденных.
В последние годы в большинстве родовспомогательных учреждений страны из-за нехватки персонала сложилась практика совмещения обязанностей акушерки и санитарки. В этих условиях недопустимо осуществлять мытье палат и других помещений в часы, предназначенные для проведения тех или иных манипуляций, предусмотренных функциональными обязанностями акушерки.
Татьяна ФРОЛОЧКИНА, главный специалист отдела госэпиднадэора и целевых программ.
В Центре иммунологии и репродукции уже много лет успешно работает программа пренатального скрининга. Наших специалистов приглашают читать лекции на специализированных конференциях, в других клиниках. Наша лаборатория получает стабильно хорошие оценки в системе контроля качества. Специально обученные специалисты проводят расчет рисков.
Содержание
Что такое пренатальная диагностика?
Слово «пренатальный» означает «дородовый». Поэтому термин «пренатальная диагностика» означает любые исследования, позволяющие уточнить состояние внутриутробного плода. Поскольку жизнь человека начинается с момента зачатия, различные проблемы со здоровьем могут быть не только после рождения, но и до рождения. Проблемы могут быть разными:
Для выяснения состояния здоровья внутриутробного плода используются методы пренатальной диагностики, к которым относятся ультразвуковое исследование, кардиотокография, различные биохимические исследования и пр. Все эти методы имеют разные возможности и ограничения. Некоторые методы вполне безопасны, как, например, ультразвуковое исследование. Некоторые сопряжены с определенным риском для внутриутробного плода, например, амниоцентез (проба околоплодных вод) или биопсия ворсинок хориона.
Понятно, что методы пренатальной диагностики, сопряженные с риском осложнений беременности, должны применяться только в том случае, когда для их использования имеются веские показания. Для того, чтобы максимально сузить круг пациенток, нуждающихся в инвазивных (т. е. связанных с вмешательством в организм) методах пренатальной диагностики, используется выделение групп риска развития тех или иных проблем у внутриутробного плода.
Что такое группы риска?
Группами риска являются такие группы пациенток, среди которых вероятность обнаружения той или иной патологии беременности выше, чем во всей популяции (среди всех женщин данного региона). Существуют группы риска по развитию невынашивания беременности, гестоза (позднего токсикоза), различных осложнений в родах и т. д. Если женщина в результате обследования оказывается в группе риска по той или иной патологии, это не означает, что данная патология обязательно разовьется. Это означает только то, что у данной пациентки тот или иной вид патологии может возникнуть с большей вероятностью, чем у остальных женщин. Таким образом, группа риска не тождественна диагнозу. Женщина может находиться в группе риска, но никаких проблем в течение беременности может не быть. И необорот, женщина может не находиться в группе риска, но проблема у нее возникнуть может. Диагноз же означает то, что у данной пациентки уже обнаружено то или иное патологическое состояние.
Зачем нужны группы риска?
Знание того, что пациентка входит в ту или иную группу риска, помогает врачу правильно спланировать тактику ведения беременности и родов. Выделение групп риска позволяет оградить пациенток, не входящих в группы риска, от ненужных медицинских вмешательств, и наоборот, позволяет обосновать назначение тех или иных процедур или исследований пациенткам, входящим в группы риска.
Что такое скрининг?
Слово скрининг означает «просеивание». В медицине под скринингом понимают проведение простых и безопасных исследований большим группам населения с целью выделения групп риска развития той или иной патологии. Пренатальным скринингом называются исследования, проводимые беременным женщинам с целью выявления групп риска осложнений беременности. Частным случаем пренатального скрининга является скрининг по выявлению групп риска развития врожденных пороков у плода. Скрининг не позволяет выявить всех женщин, у которых может быть та или иная проблема, но дает возможность выделить относительно небольшую группу пациенток, внутри которой будет сосредоточена бо́льшая часть лиц с данным видом патологии.
Зачем нужен скрининг пороков развития плода?
Некоторые виды врожденных пороков у плода встречаются довольно часто, например, синдром Дауна (трисомия по 21-й паре хромосом или трисомия 21) – в одном случае на 600 – 800 новорожденных. Это заболевание, так же как и некоторые другие врожденные заболевания, возникает в момент зачатия или на самых ранних стадиях развития зародыша и с помощью инвазивных методов пренатальной диагностики (биопсии ворсин хориона и амниоцентеза) может быть диагностировано на достаточно ранних сроках беременности. Однако такие методы сопряжены с риском целого ряда осложнений беременности: выкидыша, развития конфликта по резус-фактору и группе крови, инфицирования плода, развития тугоухости у ребенка и т. д. В частности, риск развития выкидыша после таких исследований составляет 1:200. Поэтому эти исследования следует назначать только женщинам высоких групп риска. К группам риска относятся женщины старше 35 и особенно старше 40 лет, а также пациентки с рождением детей с пороками развития в прошлом. Однако дети с синдром Дауна могут родиться и у совсем молодых женщин. Методы скрининга – совершенно безопасные исследования, проводимые в определенные сроки беременности, – позволяют с очень большой степенью вероятности выявить группы женщин с риском синдрома Дауна, которым может быть показано проведение биопсии ворсин хориона или амниоцентеза. Женщины, не попавшие в группы риска, не нуждаются в проведении дополнительных инвазивных исследований. Обнаружение повышенного риска развития пороков развития плода с помощью методов скрининга не является диагнозом. Диагноз может быть поставлен или отвергнут с помощью дополнительных тестов.
На какие виды врожденных пороков проводится скрининг?
В настоящее время рекомендуется проведение скрининга на следующие виды врожденных пороков у плода:
Какие виды исследований проводятся в рамках скрининга риска пороков развития у плода?
По видам исследований выделяют:
Общей тенденцией в развиитии пренатального скрининга является желание получать достоверную информацию о риске развития тех или иных нарушений на как можно ранних сроках беременности. Оказалось, что комбинированный скрининг в конце первого триместра беременности (сроки 10–13 недель) позволяет приблизиться к эффективности классического биохимического скрининга второго триместра беременности.
Ультразвуковой скрининг, используемый для математической обработки рисков аномалий плода, проводится только 1 раз: в конце первого триместра беременности.
Что касается биохимического скрининга, то набор показателей будет различным в разные сроки беременности. В сроки беременности 10-13 недель проверяются следующие показатели:
Расчет риска измерения аномалий плода, проведенный на основании измерения этих показателей, называется двойным биохимическим тестом первого триместра беременности.
С помощью двойного теста в I триместре рассчитываются риск обнаружения у плода синдрома Дауна (T21) и синдрома Эдвардса (T18), трисомии по 13 хромосоме (синдром Патау), триплоидии материнского происхождения, синдрома Шерешевского-Тернера без водянки. Риск дефектов нервной трубки с помощью двойного теста посчитать нельзя, поскольку ключевым показателем для определения этого риска является α-фетопротеин, который начинают определять только со второго триместра беременности.
Специальные компьютерные программы позволяют рассчитать комбинированный риск аномалий развития плода с учетом биохимических показателей, определяемых в двойном тесте первого триместра и результатов УЗИ, сделанного в сроки 10-13 недель беременности. Такой тест называется комбинированным с ТВП двойным тестом первого триместра беременности или тройным тестом первого триместра беременности. Результаты расчета рисков, полученные с помощью комбинированного двойного теста, гораздо точнее, чем расчеты риска только на основании биохимических показателей или только на основании УЗИ.
Если результаты теста в первом триместре указывают на группу риска хромосомных аномалий плода, для исключения диагноза хромосомных аномалий пациентке может быть проведена биопсия ворсин хориона.
По этим показателям рассчитываются следующие риски:
Такой тест называется четверным тестом второго триместра беременности или четверным биохимическим скринингом во втором триместре беременности. Усеченным вариантом теста является так называемый тройной или двойной тесты второго триместра, включающий в себя 2 или показателя: ХГЧ или свободная β-субъединица ХГЧ, АФП, свободный эстриол. Понятно, что точность двойного или двойного тестов II триместра ниже, чем точность четверного теста II триместра.
Еще одним вариантом биохимического пренатального скрининга является биохимический скрининг риска только дефектов нервной трубки во втором триместре беременности. При этом производится определение только одного биохимического маркера: α-фетопротеин
В какие сроки беременности проводится скрининг второго триместра?
В 14 – 20 недель беременности. Оптимальным сроком является 16 – 18 недель беременности.
Что такое четверной тест второго триместра беременности?
Основным вариантом биохимического скрининга второго триместра в ЦИР является так называемый четверной или квадрупл-тест, когда к определению трех вышеперечисленных показателей добавляется определение ингибина А.
Ультразвуковой скрининг в первом триместре беременности.
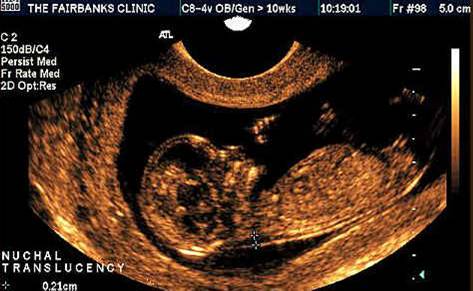
В первом триместре беременности главным размером, используемым при расчете рисков является ширина шейной прозрачности (англ. «nuchal translucency» (NT) », франц. «clarté nuchale»). В русском медицинском обиходе данный термин часто переводится как «воротниковое пространство» (ТВП) или «шейная складка». Шейная прозрачность, воротниковое пространство и шейная складка – полные синонимы, с которыми можно встретиться в разных медицинских текстах и обозначающие одно и то же.
Шейная прозрачность – определение
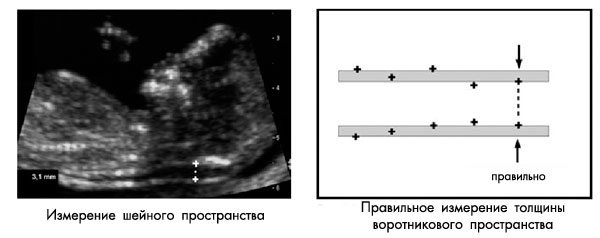
Измерение шейной прозрачности
Сроки беременности и копчико-теменной размер
Оптимальным сроком беременности для измерения ШП является срок от 11 недель до 13 недель 6 дней. Минимальный размер КТР – 45 мм, максимальный – 84 мм.
Имеются две причины для выбора срока в 11 недель в качестве самого раннего срока для измерения ШП:
Изображение и измерение
Для измерении ШП ультразвуковой аппарат должен иметь высокое разрешение с функцией видео-петли и калибраторами, которые могут измерять размер с точностью до десятых долей миллиметра. ШП можно измерить с помощью абдоминального датчика в 95% случаев, в случаях, когда это невозможно выполнить, следует использовать влагалищный датчик.
При измерении ШП в картинку должны попадать только голова и верхняя часть грудной клетки плода. Увеличение должно быть максимальным, так что небольшое смещение маркеров дает изменение в измерении не более чем на 0,1 мм. При увеличении картинки, до или после фиксации изображения, важно уменьшить гейн. Это позволяет избежать ошибки измерения, когда маркер попадает в размытую область и тем самым размер ШП будет недооценен.
Должен быть получен хороший саггитальный срез, такого же качества, как при измерении КТР. Измерение должно производиться в нейтральном положении головки плода: разгибание головки может увеличивать значение ТВП на 0,6 мм, сгибание головки – уменьшать показатель на 0,4 мм.
Важно не спутать кожу плода и амнион, поскольку в эти сроки беременности оба образования выглядят как тонкие мембраны. При сомнении следует дождаться момента, когда плод сделает движение и отойдет от амниона. Альтернативным способом является попросить беременную покашлять или легонько постучать по брюшной стенке беременной.
Замеряется наибольшее перпендикулярное расстояние между внутренними контурами шейной прозрачности (см. рисунок ниже). Замеры проводятся трижды, для расчета используется наибольшее значение размера. В 5-10% случаев обнаруживается обвитие пуповины вокруг шейки плода, что может значительно затруднить измерение. В таких случаях используется 2 измерения: выше и ниже места обвития пуповины, для расчета рисков используется среднее значение этих двух измерений.
Стандарты ультразвукового сканирования в конце первого триместра беременности разрабатываются базирующейся в Англии организацией Fetal Medicine Foundation (FMF). В группе компаний ЦИР УЗИ проводится по протоколу FMF.
Дополнительные ультразвуковые признаки риска синдрома Дауна
В последнее время дополнительно к измерению ШП для диагностики синдрома Дауна в конце первого триместра беременности использутся следующие ультразвуковые признаки:
Форма кровотока в аранциевом протоке при допплерометрии. Вверху: норма; внизу: при трисомии 21.
Не только синдром Дауна!
Во время УЗИ в конце первого триместра оценка контура плода поставляет выявить также следующие аномалии плода:
Каким образом рассчитываются риски?
Для вычисления рисков используется специальное программное обеспечение. Простое определение уровня показателей в крови недостаточно для того, чтобы решить, повышен риск аномалий развития, или нет. Программное обеспечение должно быть сертифицировано для использования с целью пренатального скрининга. На первом этапе компьютерного обсчета цифры показателей, полученные при лабораторной диагностике, переводятся в так называемые MoM (multiple of median, кратное медианы), характеризующие степень отклонения того или иного показателя от медианы. На следующем этапе расчета производится поправка MoM на различные факторы (масса тела женщины, расовая принадлежность, наличие некоторых заболеваний, курение, многоплодная беременность и т. д.). В результате получаются так называемые скорректированные MoM. На третьем этапе расчета скорректированные MoM используются для расчета рисков. Программное обеспечение специальным образом настраивается под используемые в лаборатории методы определения показателей и реактивы. Недопустимо рассчитывать риски с использованием анализов, сделанных в другой лаборатории. Наиболее точным расчет рисков аномалий плода бывает при использовании данных ультразвукового исследования, выполненного в 10-13 недель беременности.
Что такое MoM?
MoM – английская аббревиатура термина “multiple of median”, что в переводе означает “кратное медианы”. Это коэффициент, показывающий степень отклонения значения того или иного показателя пренатального скрининга от среднего значения для срока беременности (медианы). MoM расчитывается по следующей формуле:
MoM = [Значение показателя в сыворотке крови пациентки] / [Значение медианы показателя для срока беременности]
Поскольку значение показателя и медиана имеют одни и те же единицы измерения, значение MoM не имеет единиц измерения. Если значение MoM у пациентки близко к единице, то значение показателя близко к среднему в популяции, если выше единицы – выше среднего в популяции, если ниже единицы – ниже среднего в популяции. При врожденных пороках плода могут быть статистически значимые отклонения MoM маркеров. Однако в чистом виде MoM почти никогда не используются в расчете рисков аномалий плода. Дело в том, что при наличии целого ряда факторов, средние значения MoM отклоняются от средних в популяции. К таким факторам относятся масса тела пациентки, курение, расовая принадлежность, наступление беременности в результате ЭКО и др. Поэтому после получения значений MoM программа расчета рисков делает поправку на все эти факторы, в результате чего получается так называемое “скорригированное значение MoM”, которое и используется в формулах расчета рисков. Поэтому в бланках заключения по результатам анализа рядом с абсолютными значениями показателей указываются скорригированные значения MoM для каждого показателя.
Типичные профили MoM при патологии беременности
При различных аномалиях плода значения MoM сочетанно отклонены от нормы. Такие сочетания отклонений MoM называются профилями MoM при той или иной патологии. В таблицах ниже приведены типичные профили MoM при разных сроках беременности.
| Аномалия | PAPP-A | Своб. β-ХГЧ |
|---|---|---|
| Тр.21 (синдром Дауна) | 0,41 | 1,98 |
| Тр.18 (Синдром Эдвардса) | 0,16 | 0,34 |
| Триплоидия типа I/II | 0,75/0,06 | |
| Синдром Шерешевского-Тернера | 0,49 | 1,11 |
| Синдром Клайнфельтера | 0,88 | 1,07 |
| Аномалия | АФП | Общ. ХГЧ | Св. эстриол | Ингибин A |
|---|---|---|---|---|
| Тр.21 (синдром Дауна) | 0,75 | 2,32 | 0,82 | 1,79 |
| Тр.18 (синдром Эдвардса) | 0,65 | 0,36 | 0,43 | 0,88 |
| Триплоидия типа I/II | 6,97 | 13 | 0,69 | |
| Синдром Шерешевского-Тернера | 0,99 | 1,98 | 0,68 | |
| Синдром Клайнфельтера | 1,19 | 2,11 | 0,60 | 0,64-3,91 |
Показания к пренатальному скринингу I и II триместра на риск аномалий плода
В настоящее время пренатальный скрининг рекомендуется проводить всем беременным женщинам. Приказ Минздрава РФ от 2000 г. обязывает женские консультации проводить биохимический пренатальный скрининг всем беременным пациенткам во втором триместре беременности по двум показателям (АФП и ХГЧ).
Приказ № 457 от 28.12.2000 г. «О совершенствовании пренатальной диагностики в профилактике наследственных и врожденных заболеваний у детей»:
«В 16-20 недель производить забор крови у всех беременных для проведения исследований не менее двух сывороточных маркеров(АФП,ХГЧ)»
Важность проводить мониторинг врожденных заболеваний на постоянной основе в г.Москве рассматривается также в постановлении правительства Москвы об учреждении городской программы «Здоровье детей» на 2003-2005 годы.
Постановление Правительства Москвы от 23 июля 2002 г. № 572-ПП
«Целесообразно начать в Москве проведение генетического мониторинга врожденных пороков развития новорожденных, пренатального скрининга на болезнь Дауна и дефектов невральной трубки»
С другой стороны, пренатальный скрининг должен быть сугубо добровольным делом. В большинстве западных стран обязанностью врача является информирование пациентки о возможности проведения таких исследований и о целях, возможностях и ограничениях пренатального скрининга. Сама пациентка решает, делать ей анализы, или нет. Такой же точки зрения придерживается и группа компаний ЦИР. Главной проблемой является то, что никакого лечения обнаруженных аномалий не существует. В случае подтверждения наличия аномалий супружеская пара становится перед выбором: прервать беременность или сохранить ее. Это нелегкий выбор.
Что такое синдром Эдвардса?
Это состояние, обусловленное наличием в кариотипе лишней 18-й хромосомы (трисомия 18). Синдром характеризуется грубыми физическими аномалиями и умственной отсталостью. Это летальное состояние: 50% больных детей умирают в первые 2 месяца жизни, 95% – в течение первого года жизни. Девочки поражаются в 3-4 раза чаще, чем мальчики. Частота в популяции колеблется от 1 случая на 6000 родов до 1 случая на 10000 родов (примерно в 10 раз реже, чем синдром Дауна).
Что такое свободная β-субъединица ХГЧ?
Молекулы ряда гормонов гипофиза и плаценты (тиреотропного гормона (ТТГ), фолликул-стимулирующего гормона (ФСГ), лютеинизирующего гормона (ЛГ) и хорионического гормона человека (ХГЧ)) имеют сходную структуру и состоят из α и β-субъединиц. Альфа-субъединицы этих гормонов очень сходны и основные различия между гормонами заключаются в строении β-субъединиц. ЛГ и ХГЧ являются очень сходными не только по строению α-субъединиц, но и по строению β-субъединиц. Вот почему они являются гормонами с одинаковым действием. Во время беременности выработка ЛГ гипофизом падает практически до нуля, а концентрации ХГЧ очень высоки. Плацента вырабатывает очень большие количества ХГЧ, и хотя в основном этот гормон поступает в кровь в собранном виде (димерная молекула, состоящая из обеих субъединиц), в небольшом количестве в кровь поступает также свободная (не связанная с α-субъединицей) β-субъединица ХГЧ. Концентрация ее в крови во много раз меньше, чем концентрация общего ХГЧ, но этот показатель гораздо надежнее может указывать на риск проблем у внутриутробного плода на ранних сроках беременности. Определение свободной β-субъединицы ХГЧ в крови имеет значение также для диагностики трофобластической болезни (пузырного заноса и хорионэпителиомы), некоторых опухолей яичка у мужчин, мониторинге успеха процедур экстракорпорального оплодотворения.
Какой показатель: общий ХГЧ или свободная β-субъединица ХГЧ – предпочтительнее использовать в тройном тесте второго триместра?
Использование определения свободной β-субъединицы ХГЧ по сравнению с определением общего ХГЧ дает более точный расчет риска синдрома Дауна, однако в классических статистических расчетах риска синдрома Эдвардса в популяции использовалось определение уровня общего ХГЧ в крови матери. Для β-субъединицы ХГЧ таких расчетов не проводилось. Поэтому нужно делать выбор между более точным вычислением риска синдрома Дауна (в случае β-субъединицы) и возможностью вычисления риска синдрома Эдвардса (в случае общего ХГЧ). Напомним, что в первом триместре для вычисления риска синдрома Эдвардса используется толко свободная β-субъединицы ХГЧ, но не общий ХГЧ. Синдром Эдвардса характеризуется низкими цифрами всех 3-х показателей тройного теста, поэтому в подобных случаях можно сделать оба варианта тройного теста (с общим ХГЧ и со свободной β-субъединицей).
Что такое PAPP-A?
Ассоциированный с беременностью плазменный протеин A (pregnancy-associated plasma protein-A, PAPP-A) впервые был описан в 1974 г. в виде высокомолекулярной белковой фракции в сыворотке крови женщин на поздних сроках беременности. Оказалось, что это большой цинк-содержащий металогликопротеин с молекулярной массой около 800 кДа. Во время беременности PAPP-A вырабатывается синцитиотрофобластом (тканью, являющейся наружным слоем плаценты) и экстраворсинным цитотрофобластом (островками клеток плода в толще слизистой оболочки матки) и поступает в кровоток матери
Биологическое значение этого белка не до конца изучено. Было показано, что он связывает гепарин и является ингибитором эластазы гранулоцитов (фермента, индуцируемого при воспалении), поэтому предполагается, что PAPP-A модулирует иммунный ответ материнского организма и является одним из факторов, который обеспечивает развитие и выживание плаценты. Кроме того, было установлено, что он является протеазой, расщепляющей протеин 4, связывающий инсулиноподобный фактор роста. Существуют серьезные основания полагать, что PAPP-A является одним из факторов паракринной регуляции не только в плаценте, но и в некоторых других тканях, в частности в атеросклеротических бляшках. Предлагается использовать данный маркер как один из факторов риска ишемической болезни сердца.
Концентрации PAPP-A в крови матери постоянно увеличиваются с увеличением срока беременности. Наибольший рост этого показателя отмечается в конце беременности.
В течение последних 15 лет PAPP-A изучался в качестве одного из трех маркеров риска трисомии 21 (синдром Дауна) (вместе со свободной β-субъединицей ХГЧ и толщиной воротникового пространства). Оказалось, что уровень этого маркера в конце первого триместра беременности (8-14 недель) значительно снижен при наличии у плода трисомии 21 или трисомии 18 (синдром Эдвардса). Уникальностью этого показателя является то, что значимость его как маркера синдрома Дауна исчезает после 14 недель беременности. Во втором триместре уровни его в материнской крови при наличии у плода трисомии 21 не отличаются от таковых у беременных со здоровым плодом. Если рассматривать PAPP-A в качестве изолированного маркера риска синдрома Дауна в первом триместре беременности, наиболее значимым было бы его определение в сроки 8–9 недель. Однако свободная β-субъединица ХГЧ является стабильным маркером риска синдрома Дауна в сроки 10–18 недель, т. е. позже PAPP-A. Поэтому оптимальным сроком сдачи крови для двойного теста первого триместра беременности – 10–12 недель.
Комбинация измерения уровня PAPP-A с определением концентрации свободной β-субъединицы ХГЧ в крови и определением ТВП с помощью УЗИ в конце первого триместра беременности позволяет выявить до 90% женщин с риском развития синдрома Дауна в старшей возрастной группе (после 35 лет). Вероятность ложноположительных результатов при этом составляет около 5%.
Кроме пренатального скрининга риска синдрома Дауна и синдрома Эдвардса, в акушерстве определение PAPP-A используется также при следующих видах патологии:
Диагностика риска остановки развития плода на малых сроках беременности явилось исторически первым клиническим приложением определения PAPP-A в сыворотке крови, предложенным в начале 1980-х годов. Было показано, что женщины с низкими уровнями PAPP-A на ранних сроках беременности попадают в группы риска последующей остановки развития беременности и тяжелых форм позднего токсикоза. Поэтому рекомендуется определение этого показателя в сроки 7–8 недель женщинам с тяжелыми осложнениями беременности в анамнезе.
Синдром Корнелии де Ланж – это редкая форма врожденных пороков развития плода, обнаруживаемая в 1 случае на 40 000 родов. Синдром характеризуется отставанием умственного и физического развития, пороками сердца и конечностей и характерными особенностями черт лица. Было показано, что при данном состоянии уровни PAPP-A в крови в сроки 20–35 недель значимо ниже нормы. Исследование группы Эйткена в 1999 г. показало, что данный маркер может использоваться для скрининга на синдром Корнелии де Ланж и во втором триместре беременности, поскольку уровни показателя у таких беременных в среднем были в 5 раз ниже нормы.
Реактивы, используемые для определения PAPP-A и свободной β-субъединицы ХГЧ, на порядок дороже реактивов, используемых для большинства гормональных показателей, что делает данный тест более дорогим исследованием по сравнению с определением большинства гормонов репродуктивной системы.
Что такое α-фетопротеин?
Это гликопротеин плода, вырабатываемый вначале в желточном мешке, а потом в печени и желудочно-кишечном тракте плода. Это транспортный белок в крови плода, связывающий целый ряд различных факторов (билирубин, жирные кислоты, стероидные гормоны). Это двойной регулятор роста внутриутробного плода. У взрослого человека никаких известных функций АФП не выполняет, хотя может повышаться в крови при заболеваниях печени (цирроз, гепатит) и при некоторых опухолях (гепатоклеточная карцинома и герминативная карцинома). В крови матери уровень АФП постепенно повышается с увеличением срока беременности и достигает максимума к 30 неделям. Уровень АФП в крови матери повышается при дефектах нервной трубки у плода и при многоплодной беременности, понижается – при синдроме Дауна и при синдроме Эдвардса.
Что такое свободный эстриол?
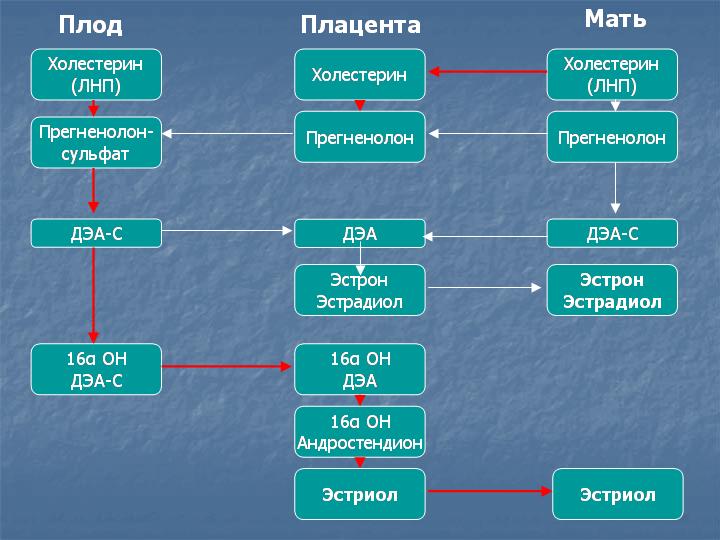
Эстриол синтезируется в плаценте из 16α-гидрокси-дегидроэпиантростерон-сульфата, поступающего со стороны плода. Главный источник предшественников эстриола – надпочечники плода. Эстриол является главным эстрогенным гормоном беременности и обеспечивает рост матки и подготовку молочных желез к лактации.
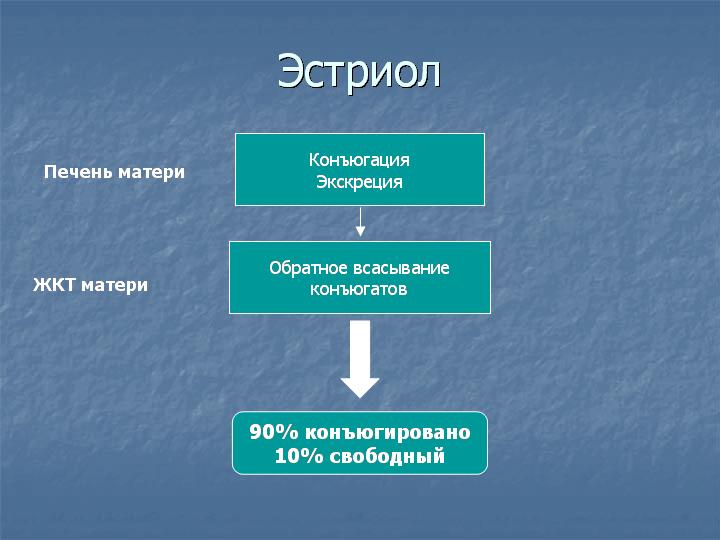
90% эстриола после 20 недель беременности образуются из ДЭА-С плода. Большой выход ДЭА-С из надпочечника плода связан с низкой активностью 3β-гидроксистероид-дегидрогеназы у плода. Протективным механизмом, защищающим плод от избытка андрогенной активности, является быстрая конъюгация стероидов с сульфатом. В сутки плод вырабатывает более 200 мг ДЭА-С в день, в 10 раз больше матери. В печени матери эстриол быстро подвергается конъюгации с кислотами, в основном с гиалуроновой кислотой, и таким образом инактивируется. Наиболее точным методом определения активности надпочечников плода является определение уровня свободного (неконъюгированного) эстриола.
Уровень свободного эстриола постепенно повышается по мере развития беременности и в третьем триместре беременности может использоваться для диагностики благополучия плода. При ухудшении состояния плода в третьем триместре беременности может наблюдаться резкое падение уровня свободного эстриола. Уровень свободного эстриола часто понижен при синдроме Дауна и при синдроме Эдвардса. Прием дексаметазона, преднизолона или метипреда при беременности подавляет функцию надпочечников плода, поэтому уровень свободного эстриола у таких пациенток часто снижается (снижение поступления эстриола со стороны плода). При приеме антибиотиков усиливается скорость конъюгации эстриола в печени матери и снижается обратное всасывание конъюгатов из кишечника, поэтому уровень эстриола тоже снижается, но уже за счет ускорения его инактивации в организме матери. Для точной интерпретации данных тройного теста очень важно, чтобы пациентка указала полный список лекарств, принимавшихся или принимаемых во время беременности с дозами и сроками приема.
Алгоритм проведения пренатального скрининга I и II триместра беременности.
1. Рассчитываем срок беременности, лучше после консультации с врачом или с помощью консультанта.
Скрининг I триместра имеет свои особенности. Он проводится в сроки 10 – 13 недель беременности и достаточно жестко ограничен по срокам. Если сдать кровь слишком рано или слишком поздно, если ошибиться в расчете сроков беременности на момент сдачи крови, точность расчета резко уменьшится. Сроки беременности в акушерстве обычно рассчитываются по первому дню последней менструации, хотя зачатие происходит в день овуляции, т. е. при 28-дневном цикле – через 2 недели после первого дня менструации. Поэтому сроки 10 – 13 недель по дню менструации соответствуют 8 – 11 неделям по зачатию.
Для вычисления срока беременности мы рекомендуем воспользоваться акушерским календарем, размещенном на нашем сайте. Сложности в расчете сроков беременности могут быть при нерегулярном менструальном цикле, при беременности, наступившей вскоре после родов, при цикле, более чем на неделю отклоняющегося от 28 дней. Поэтому лучше всего довериться профессионалам, и для расчета сроков беременности, проведения УЗИ и сдачи крови обратиться к врачу.
2. Делаем УЗИ.
Следующим этапом должно быть проведение УЗИ в сроки 10 – 13 недель беременности. Данные этого исследования будут использованы программой расчета рисков как в первом, так и во втором триместре. Начинать обследование нужно именно с УЗИ, поскольку в процессе исследования могут выявиться проблемы с развитием беременности (например, остановка или отставание в развитии), многоплодная беременность, будут достаточно точно рассчитаны сроки зачатия. Врач, проводящий УЗИ, поможет пациентке расчитать сроки сдачи крови для биохимического скрининга. Если УЗИ окажется сделанным слишком рано по срокам беременности, то, возможно, врач рекомендует повторить исследование спустя какое-то время.
Для расчета рисков будут использоваться следующие данные из заключения УЗИ: дата УЗИ, копчико-теменной размер (КТР) и толщина воротникового пространства (ТВП) (английские сокращения соответственно CRL и NT), а также визуализация носовых костей.
3. Сдаем кровь.
Имея результаты УЗИ и зная точный срок беременности можно приходить для сдачи крови. Взятие крови для анализа на пренатальный скрининг в группе компаний ЦИР проводится ежедневно, включая выходные дни. В будние дни взятие крови проводится с 7:45 до 21:00, в выходные и праздничные дни: с 8:45 до 17:00. Взятие крови проводится через 3-4 часа после последнего приема пищи.
4. Получаем результат.
Теперь нужно получить результаты анализа. Сроки готовности результатов анализа пренатального скрининга в группе компаний ЦИР составляют один рабочий день (кроме четверного теста). Это означает, что анализы, сданные с понедельника по пятницу будут готовы в тот же день, а сданные с субботы по воскресенье – в понедельник.
Заключения по результатам исследования выдаются пациентке на русском языке.
Тиблица. Объяснения терминов и сокращений
| Дата отчета | Дата компьютерной обработки результатов |
| Срок беременности | Недели + дни |
| Дата УЗИ |  Дата проведения УЗИ. Обычно не совпадает с датой сдачи крови. Дата проведения УЗИ. Обычно не совпадает с датой сдачи крови. |
| Плоды | Количество плодов. 1 – одноплодная беременность; 2 – двойня; 3 – тройня |
| ЭКО | Беременность наступила в результате ЭКО |
| КТР | Копчико-теменной размер, определенный во время УЗИ |
| MoM | Кратное медианы (multiple of median), степень отклонения результата от среднего для данного срока беременности |
| Скорр. MoM | Скорригированное MoM. Значение MoM после коррекции по массе тела, возрасту, расовой принадлежности, количеству плодов, наличию диабета, курению, лечению бесплодия методом ЭКО. |
| NT | Толщина воротникового пространства (nuchal translucency). Синоним: шейная складка. В различных вариантах отчетов могут приводиться либо абсолютные значения в мм, либо степень отклонения от медианы (MoM) |
| Возрастной риск | Среднестатистический риск для данной возрастной группы. Не учитываются никакие факторы, кроме возраста. |
| Tr. 21 | Трисомия 21, синдром Дауна |
| Tr. 18 | Трисомия 18, синдром Эдвардса |
| Биохимический риск | Риск аномалий плода после компьютерной обработки данных анализа крови без учета данных УЗИ |
| Комбинированный риск | Риск аномалий плода после компьютерной обработки данных анализа крови с учетом данных УЗИ. Наиболее точный показатель степени риска. |
| fb-HCG | Свободная β-субъединица ХГЧ |
| ДПМ | Дата последней менструации |
| AFP | α-фетопротеин |
| HCG | Общий ХГЧ (human chorionic gonadotropin) |
| uE3 | Свободный эстриол (unconjugated estriol) |
| +NT | Расчет проводился с учетом данных УЗИ |
| mIU/ml | мМЕ/мл |
| ng/ml | нг/мл |
| IU/ml | МЕ/мл |
Дополнительная информация.
Информация для пациентов: обратите внимание, что если Вы планируете пройти пренатальный скрининг в группе компаний ЦИР, то данные УЗИ, сделанного в других учреждениях, будут приниматься в расчет только в случае наличия специального договора группы компаний ЦИР с этими учреждениями.
Информация для врачей
Уважаемые коллеги! В соответствии с Приказом Минздрава № 457 и Постановлением Правительства Москвы № 572 группа компаний ЦИР оказывает услуги другим лечебным учреждениям по проведению пренатального скрининга на риск хромосомных аномалий. Вы можете пригласить наших сотрудников приехать к вам с лекцией по данной программе. Для направления пациентки на скрининг лечащий врач должен заполнить специальное направление. Пациентка может приехать для сдачи крови самостоятельно, но возможно и взятие крови в других учреждениях с последующей доставкой в нашу лабораторию, в том числе и нашим курьером. Если вы хотите получать результаты двойных, тройных и четверных тестов первого и второго триместров беременности, комбинированных с данными УЗИ, пациентка должна приехать к нам для УЗИ, либо мы должны подписать с вашим учреждением специальный договор и включить в программу ваших специалистов УЗИ, но только после выезда нашего эксперта по функциональной диагностике в ваше учреждение и ознакомления с качеством аппаратуры и квалификацией специалистов.