Иммуносупрессивные препараты что это список препаратов
Иммунодепрессант: понятие, виды, особенности
Иммуномодулирующие препараты и иммунодепрессанты имеют еще и другое название – иммуносупрессоры. Они используются для замедления работы и размножения клеток иммунной системы. Их нужно принимать тогда, когда нужно остановить иммунные реакции, например, при пересадке органов, аутоиммунных патологиях, костно-мышечной системы и прочих серьезных заболеваниях.
Особенности иммунодепрессантов
Применять иммуносупрессивные средства нужно тогда, когда другие методы лечения испробованы и не достигнуты желаемые результаты, а шансы на положительный исход намного выше рисков от их использования. Из перечня лекарств-иммунодепрессантов практически все имеют иммуносупрессивную активность, оказывают широкое действие. Их применение понижает антибактериальный и противоопухолевый иммунитет, повышает риск появления инфекционных заражений, онкопатологии.
Поскольку заболевания и осложнения состояния здоровья во многих случаях имеют неблагоприятный исход, то противопоказания для лечения иммуносупрессорами несущественны.
Ученые работают над тем, чтобы придать лекарству узкую сферу действия, то есть, чтобы оно действовало на одну конкретную проблему, не затрагивая другие клетки.
С учетом действия препарата на иммунитет человека, их относят к нескольким группам:
Полностью подавляющие иммунную систему;
Для облегчения проявлений аутоиммунных заболеваний;
Противовоспалительное действие – необходимы при нарушении работы мозга.
Есть и другая классификация препаратов:
Также есть несколько поколений этих средств:
Принцип действия
Иммуноспрессоры имеют определенный механизм работы:
«Азатиоприн» и «Метотрексат» препятствуют разделению клеток, приостанавливают образование белковых элементов. Результат происходит медленно и с момента использования будет заметен только через пол года. Эти препараты имеют противоопухолевое действие. Также если принимать его в небольшом количестве, то будет достигнут противовоспалительный результат. Первый препарат содержит меньшее количество токсичных веществ.
«Циклоспорин». Достигается селективное и обратимое воздействие на клеточный иммунный ответ. Повышается продолжительность функционирования аллогенных трансплантатов разных органов.
Глюкокортикоиды. Отличаются сильным иммунодепрессивным эффектом. Останавливают работу макрофагов, лимфоцитов, не позволяя им попадать в кровь. Если принимать в большом количестве, то будет приостановлена работа иммуноглобулина. Отличаются выраженным и быстрым противовоспалительным действием.
Препараты золота, собираясь в зараженных суставных тканях, уменьшают фагоцитарную работу макрофагов, снижают содержание иммуноглобулина в плазме, что приводит к уменьшению его разрушительного воздействия на суставы. Результат будет заметен спустя 6 месяцев.
Даклизумаб. Это очень сильный препарат, от которого достигается более мощный цитостатический эффект.
Клинико-фармакологические принципы
Чтобы достигнуть желаемого результата от применения лекарственных препаратов, нужно учитывать некоторые клинико-фармакологические принципы:
Большие дозы – маленькие дозы;
Маленькое противовоспалительное действие – большое противовоспалительное действие;
Быстрое лечение – продолжительное лечение;
Разное время достижения результата – эффект будет заметен через конкретный промежуток времени (день, неделя, месяц, полгода);
Подавление производства ДНК – подавление разделения РНК.
Особенности применения
При приеме этих лекарственных препаратов нужно учитывать меры предосторожности. Во-первых, их нужно с осторожностью принимать при беременности, грудном вскармливании, проблемах работы почек и печени, инфекционных заражениях, нарушенной функции костного мозга. Их прописывают при следующих заболеваниях и хирургических вмешательствах:
пересадка органов и тканей;
миокард в хронической форме.
Средства с избирательным воздействием не мешают появлению защитных клеток при инфекционных заболеваниях и практически никак не сказываются на противоопухолевом иммунитете.
Разница между иммунодепрессантов и иммуностимуляторов
Иммунитет человека иногда нуждается в коррекции. В таком случае стоит прибегать к помощи особых лекарственных препаратов – иммунодепрессантов и иммуностимуляторов. Стоит понимать разницу между ними:
при продолжительном хроническом заболевании защитная функция организма нарушается и отмечаются аутоиммунные сбои, то есть происходит самоатака клеток. В этом случае необходима коррекция иммуносупрессорами. Их прописывают при разных аллергиях, чрезмерной работе лимфоцитных клеток, после пересадки тканей и органов;
при заражении вредными микроорганизмами запускается производство особых клеток. Если же их количества недостаточно, то человек заболевает. Для повышения выработки защитных клеток стоит использовать иммуностимуляторы. Как правило их нужно принимать при таких серьезных проблемах, как: хронические медленно протекающие заболевания с регулярными рецидивами, которые спровоцированы микробной и вирусной инфекцией.
Как видно, оба этих средства направлены на улучшение иммунитета индивида.
Можно сделать вывод, что эти препараты обладают широким действием и используются при различных заболеваниях и показаны при пересадке тканей и органов. К тому же у них нет побочных реакций, которые могли бы нанести вред здоровью и жизни человека. Вы также можете приобрести препараты для улучшения кровообращения через наш каталог.
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Иммунодепрессанты (лекарственные препараты, подавляющие активность иммунной системы)
Иммунодепрессанты (иммуносупрессивные препараты) – это особая группа лекарственных средств, которые подавляют иммунитет.
Однако существуют ситуации, когда под влиянием определенных условий защитные иммунные механизмы приобретают извращенные черты и становятся причиной развития нежелательных реакций. К таким реакциям относят аутоиммунные заболевания и реакция отторжения трансплантата.
Аутоиммунные заболевания – это обширная группа воспалительных болезней, связанных с нарушением функции иммунной системы, при котором иммунитет начинает воспринимать собственные органы и ткани (например, щитовидную железу, поджелудочную железу, слюнные, слезные железы, нервную, мышечную, соединительную ткани, капилляры сосудов) как чужеродные объекты и активно атакует их.
Реакция отторжения трансплантата – угрожающая жизни реакция, возникающая у пациента после пересадки ему чужого органа или ткани. При этом иммунитет пациента начинает атаковать пересаженный от донора орган или ткань, принимая его за опасную чужеродную структуру.
Риск развития реакции отторжения трансплантата отсутствует только при аутотрансплантации – когда пациент является донором для самого себя (например, при пересадке кожи из одного участка тела на другой или же при трансплантации заранее отобранного и законсервированного костного мозга или стволовых клеток после тяжелой химиотерапии или лучевой терапии рака) и изотрансплантации – когда донором является однояйцевый близнец, абсолютно идентичный по генетическим и иммунологическим характеристикам пациенту.
Во всех остальных случаях реакция отторжения трансплантата без определенных мер по угнетению иммунитета неминуема.
Для этих целей и используют препараты группы иммунодепрессантов – средства, подавляющие иммунный ответ.
Показания к применению
Препараты иммунодепрессантов применяют при заболеваниях, связанных с извращенно-активным иммунитетом:
Помимо этого, отдельные иммунодепрессанты используют при тяжелом поражении почек – нефротическом синдроме на фоне гломерулонефрита или гломерулосклероза (циклоспорин, глюкокортикостероиды).
Также некоторые препараты иммунодепрессантов (цитостатики, глюкокортикостероиды, ингибиторы кальциневрина) назначают в комплексной или поддерживающей терапии злокачественных опухолей – рака крови, молочной железы, почек, легких, поджелудочной железы, лимфомах, хорионкарциномах и т.д.
Глюкокортикостероиды дополнительно используют при тяжелых аллергиях – анафилактическом шоке, ангионевротическом отёке (отёке Квинке), бронхиальной астме, атопическом дерматите; при резком падении артериального давления – кардиогенном, травматическом, токсическом шоках; при черепно-мозговой травме, отеках мозга и легких.
Фармакологическое действие
Препараты иммунодепрессантов угнетают иммунитет благодаря подавлению роста и развития иммунных клеток – Т-лимфоцитов и В-лимфоцитов, а также уменьшению образования антител.
Иммунодепрессивное и противовоспалительное действие препаратов иммунодепрессантов реализуется также за счет подавления специфических сигнальных молекул, отвечающих за «общение» клеток иммунитета – цитокинов: интерлейкинов (интерлейкина-1, интерлейкина-4, интерлейкина-6), фактора некроза опухоли-альфа.
Глюкокортикоиды также имеют выраженный противоаллергический и противовоспалительный эффекты, повышают артериальное давление (противошоковый эффект), стимулируют обезвреживающую функцию печени (антитоксический эффект).
Иммунодепрессанты группы цитостатиков, глюкокортикоиды, ингибиторы кальциневрина выраженно угнетают рост и развитие раковых клеток, оказывая дополнительно противоопухолевое действие.
Классификация иммунодепрессантов
Препараты иммунодепрессантов классифицируют на:
Иммунодепрессивное действие присуще также противомалярийным препаратам – хлорохину, гидроксихлорохину, препаратам золота – ауранофину, ауротиомалату натрия, ауротиоглюкозе.
Основы лечения препаратами иммунодепрессантов
Лечение препаратами иммунодепрессантов обычно очень длительное – составляет от нескольких месяцев до нескольких лет. Однако чаще всего эти препараты пациенту нужно принимать пожизненно (особенно в случае пересадки органов или тканей).
Препараты глюкокортикостероидов следует использовать рано утром – в промежутке времени между 6 и 7 часами утра. Такой режим помогает препаратам достичь своего максимального эффекта, а также снизить выраженность их побочного действия.
Особенности лечения препаратами иммунодепрессантов
Препараты иммунодепрессантов имеют большое количество побочных эффектов, кроме того, они значительно влияют на действие других лекарственных средств, повышая их токсичность. Поэтому иммунодепрессанты используют только по назначению и под строгим контролем врача.
Препараты иммунодепрессантов, подавляя иммунную защиту организма, делают его гораздо более чувствительным к инфекционным заболеваниям – бактериальным, вирусным, грибковым. Также иммунодепрессанты маскируют симптомы острых инфекционных заболеваний, в том числе простудных, что может привести к развитию более тяжелых состояний, например, пневмонии.
ВНИМАНИЕ! Цены актуальны только при оформлении заказа в электронной медицинской информационной системе Аптека 9-1-1. Цены на товары при покупке непосредственно в аптечных заведениях-партнерах могут отличаться от указанных на сайте!
Иммуносупрессивная терапия
Для того, чтобы не произошло отторжение пересаженного органа необходимо проведение иммуносупрессивной терапии. Неверно думать, будто она полностью выключает или подавляет иммунитет, вызывает выключение защитных механизмов. Современная медикаментозная иммуносупрессия меняет иммунитет, блокируя на разных уровнях механизмы агрессии иммунитета против пересаженного органа. Действительно, состояние иммуносупрессии несколько повышает восприимчивость организма к инфекциям, в первую очередь вирусным. Кроме того, иммуносупрессивные препараты имеют некоторые особенности, которые необходимо знать как врачу, так и пациенту, который их принимает.
Важно помнить следующее. Несоблюдение рекомендаций врача пациентами после трансплантации печени создаёт угрозу жизни. Назначенная иммуносупрессивная терапия должна приниматься неукоснительно и точно до минуты и до таблетки. Человек, лукавящий, обманывающий врачей, родственников в приёме препаратов, обманывает только самого себя. Хорошее самочувствие, большой срок после трансплантации, хорошие показатели не означают, что можно самостоятельно отменить или снизить дозировку иммуносупрессивной терапии. Зная, что эксперименты на людях запрещены, мы не должны ставить экспериментов на самих себе. Перечислим основные препараты, с которыми Вы сможете столкнуться после трансплантации. Эти препараты применяются во всех странах мира. Вы можете быть уверены, что получаете такую же современную иммуносупрессию, как и пациенты в Токио, Ганновере, Нью-Йорке, Москве. Приведённые данные носят ориентирующий характер. За более подробной информацией обращайтесь, пожалуйста, к инструкции по медицинскому применению препарата, вложенной в упаковку.
Если Вы забыли своевременно принять дозу препарата или после приема таблетки Вас вырвало, примите пропущенную дозу. Однако, если уже почти наступило время для приёма следующей дозы, пропустите пропущенную дозу и продолжайте регулярный режим дозирования. Не принимайте двойную дозу, чтобы наверстать пропущенный прием. Один пропущенный прием препарата как правило не опасен, но таких пропусков должно быть как можно меньше.
Такролимус (програф, прилуксид, рединесп)
Иммуносупрессивный препарат такролимус был открыт в 1984 году как продукт жизнедеятельности грибков из почвы в Японии. Являясь макролидным антибиотиком, он обладает слабым противомикробным и противогрибковым действием, но наиболее мощным является его иммуносупрессивное действие. Широко внедрён в клиническую практику благодаря трудам отца современной трансплантологии Томаса Старзла. Химически является 23-членным макролидом. Угнетает кальциневрин, приводя к снижению выделения лимфоцитами интерлейкина-2. В настоящее время такролимус является золотым стандартом и препаратом №1 в проведении иммуносупрессивной терапии после трансплантации печени.
Этот препарат обладает рядом специфических особенностей, которые надо понимать.
Такролимус пролонгированного действия (адваграф)
Форма пролонгированного действия такролимуса полностью идентична такролимусу, однако суточная доза принимается в один прием — как правило, утром. Все предосторожности в отношении такролимуса распространяются и на данную форму.
Циклоспорин А (сандиммун неорал, экорал, панимун беорал)
Циклоспорин был открыт в 1969 году в Норвегии как продукт жизнедеятельности почвенных грибков. В 1972 году в Швейцарии открыто его действие на иммунитет. Как и такролимус, является ингибитором кальциневрина. Имеет меньшую по сравнению с такролимусом эффективность и более выраженную нефротоксичность. Так как концентрация препарата после его приёма меняется, как правило берут кровь для её определения до приёма таблеток (обычно, за 30 минут до очередного приёма) — это называется «нулевой» концентрацией или С0. Также иногда определяют концентрацию препарата на 2 часу после приёма очередной дозы — концентрацию С2. В сложных случаях концентрацию определяют несколько раз в разные сроки после приема препарата, строят кривую препарата и определяют интегральный показатель — площадь под кривой концентрации (AUC). В редких случаях прием циклоспорина повышает артериальное давление. Редким осложнением также является гиперплазия дёсен. При появлении разрастания тканей дёсен необходимо сообщить своему врачу и обратиться к стоматологу. Если у Вас имеется склонность к повышению уровня холестерина в крови, прием циклоспорина может способствовать его повышению.
Мы назначаем циклоспорин довольно редко, например, при непереносимости препаратов такролимуса
Микофенолаты: микофеноловая кислота (майфортик), микофенолата мофетил (селлсепт, майсепт, микофенолат тл)
Препараты микофеноловой кислоты имеют выраженное иммуносупрессивное действие при небольшом количествепобочных эффектов. Они подавляют фермент, синтезирующий основания для образования ДНК, за счёт чего тормозят деление Т и В лимфоцитов. У некоторых пациентов прием препаратов микофеноловой кислоты достаточно редко приводит к прокинетическому эффекту: увеличивается активность кишечника вплоть до развития диареи. При приёме этих препаратов необходимо контролировать уровень лейкоцитов, при тенденции к снижению необходимо корригировать дозировку во избежание развития инфекционных осложнений (вирусных, в первую очередь). Применение цитостатических иммуносупрессивных препаратов несколько замедляет заживление ран
Ингибиторы mTOR рецепторов: сиролимус (рапамун), эверолимус (сертикан)
Азатиоприн
Азатиоприн является классическим иммуносупрессивным препаратом, введенным в клиническую практику в 1978 году основоположником мировой трансплантации Роем Калном. Данный препарат обладает лимфостатическим действием. Превращаясь в активную форму 6-меркаптопурин, азатиоприн подавляет синтез ДНК в быстро делящихся клетках, в том числе, в Т и В лимфоцитах. Контроль концентрации этого препарата не нужен. Нужен контроль количества лейкоцитов в крови, так как азатиоприн может понижать его. Как и у других лимфостатических иммуносупрессивных препаратов, длительный приём азатиоприна может повышать риск развития некоторых опухолей, о чём нужно помнить. На фоне приёма азатиоприна редко может разиваться острый панкреатит. Несмотря на то, что в клинической практике встречаются более эффективные препараты со сходным действием, недорогой азатиоприн до сих пор имеет место в клинической практике лечения пациентов после трасплантации. Принимается два раза в день в одно и то же время.
Преднизолон, метилпреднизолон (метипред)
Глюкокортикоидные гормоны являются классическим компонентом иммуносупрессивной терапии. С их применением связаны частые страхи и домыслы. Действительно, в прошлом, когда после трансплантации глюкокортикоиды длительно применялись в больших дозировках, на этом фоне возникали такие побочные эффекты, как увеличение веса, покраснение лица, чувство «приливов» после приёма таблеток, увеличение аппетита и другие. Однако сейчас схемы снижения глюкокортикоидов претерпели значительные изменения и дозировки и сроки применения препаратов минимизированы, такие побочные эффекты выражены крайне редко. Под действием глюкокортикоидов уменьшаесмя количество лимфоцитов и уменьшается их активность. Наш центр назначает глюкокортикостероиды крайне редко. Через некоторое время мы снижаем дозировку стероидов или отменяем их приём.
Иммуносупрессивные препараты что это список препаратов
Как профилактика отторжения трансплантата, так и лечение аутоиммунных заболеваний требуют подавления иммунных реакций. Однако иммунная супрессия влечет за собой ослабление защитных сил против инфекционных возбудителей и повышение риска развития опухоли в отдаленный период.
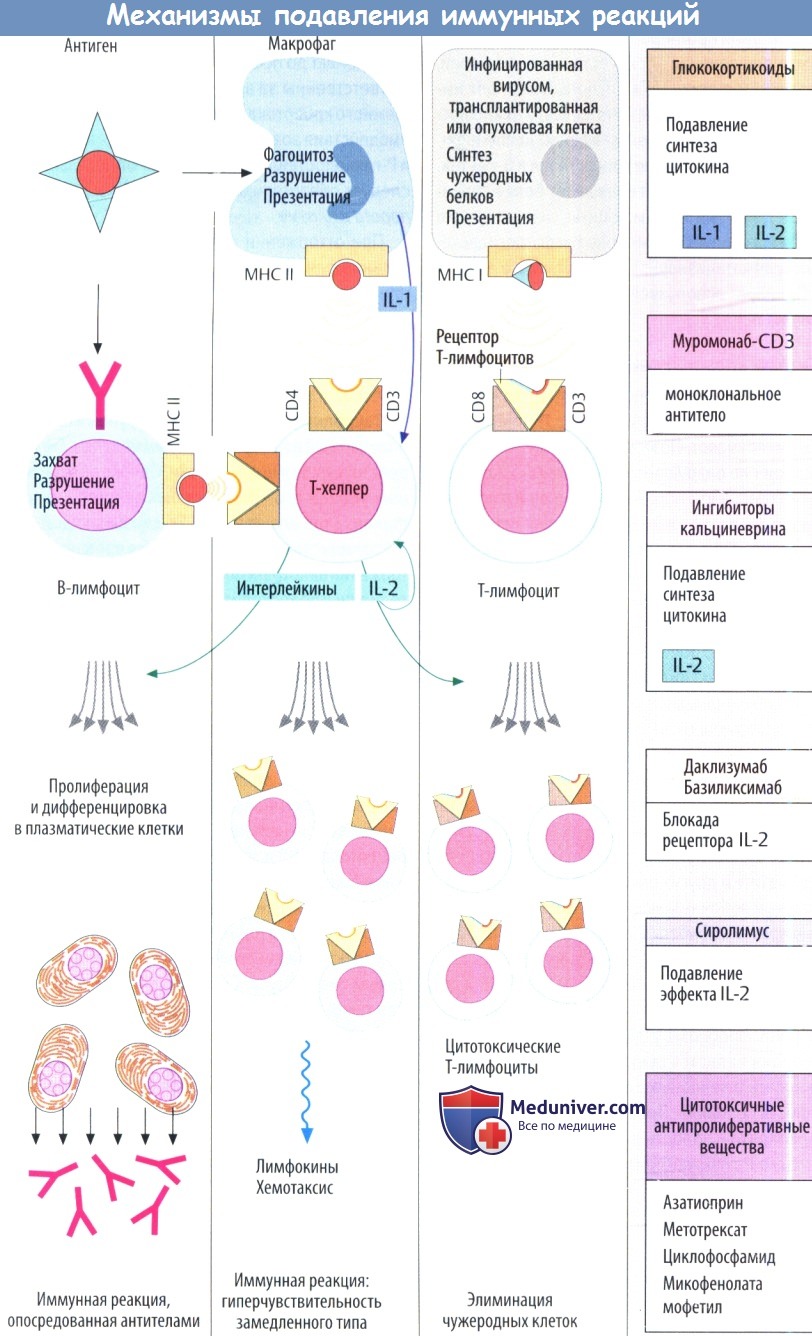
Специфический иммунный ответ начинается со связывания антигена лимфоцитами, несущими рецепторы с соответствующим антигенсвязываю-щим участком. В-лимфоциты распознают структуры поверхностного антигена с помощью мембранных рецепторов, которые похожи на образованные впоследствии антитела. Т-лимфоцитам (и интактным В-клеткам) требуется антиген на поверхности макрофагов или других клеток в сочетании с главным комплексом гистосовместимости (МНС); последний обеспечивает распознавание антигенных структур посредством рецепторов Т-клеток. Т-хелперы несут комплексы CD3 и CD4, цитотоксические Т-клетки — комплекс CD8.
Белки CD участвуют в связывании МНС. Активация Т-клеток также увеличивается при контакте с другими мембранными белками: CD80/86 в случае клетки, несущий антиген, и CD28 на лимфоците. Существует собственный физиологический прерывающий механизм при высвобождении активированными лимфоцитами С028-подобных инертных молекул во внеклеточное пространство; они «покрывают» комплекс CD80/86 и предупреждают контакт с ним и активацию лимфоцитов. Кроме того, распознавание антигена и стимуляция цитокинами играют важную роль в активации лимфоцитов.
Интерлейкин-1 образуется макрофагами, а другие интерлейкины (IL), в т. ч. IL-2, образуются Т-хелперами. При пролиферации антигенспецифических лимфоцитов запускается иммунная защита. I.
I. Воздействие на распознавание антигена. Муромонаб CD3 — моноклональное антитело, направленное против CD3 мышей, которое блокирует распознавание антигена Т-лимфоцитами (используется при отторжении трансплантата).
Глатирамера ацетат состоит из пептидов различной длины, полимеризованных в случайной последовательности из аминокислот глутамина, лизина, аланина и тирозина. Его используют при лечении рассеянного склероза наряду с IFN-β. Данное заболевание является результатом аутоагрессии Т-лимфоцитов направленной против олигодендроцитов, которые образуют миелиновые оболочки аксонов ЦНС.
Причинный антиген, очевидно, является основным миелиновым белком. Глатирамер имеет сходство с последним. Блокируя рецепторы антигена, он нарушает распознавание антигена лимфоцитами.
Абатацепт — слитный белок, состоящий из инертной молекулы лимфоцита CD28 и Fc-фрагмента антитела. Он имитирует физиологическое торможение в результате антигенной стимуляции Т-клеток и применяется при ревматоидном артрите.
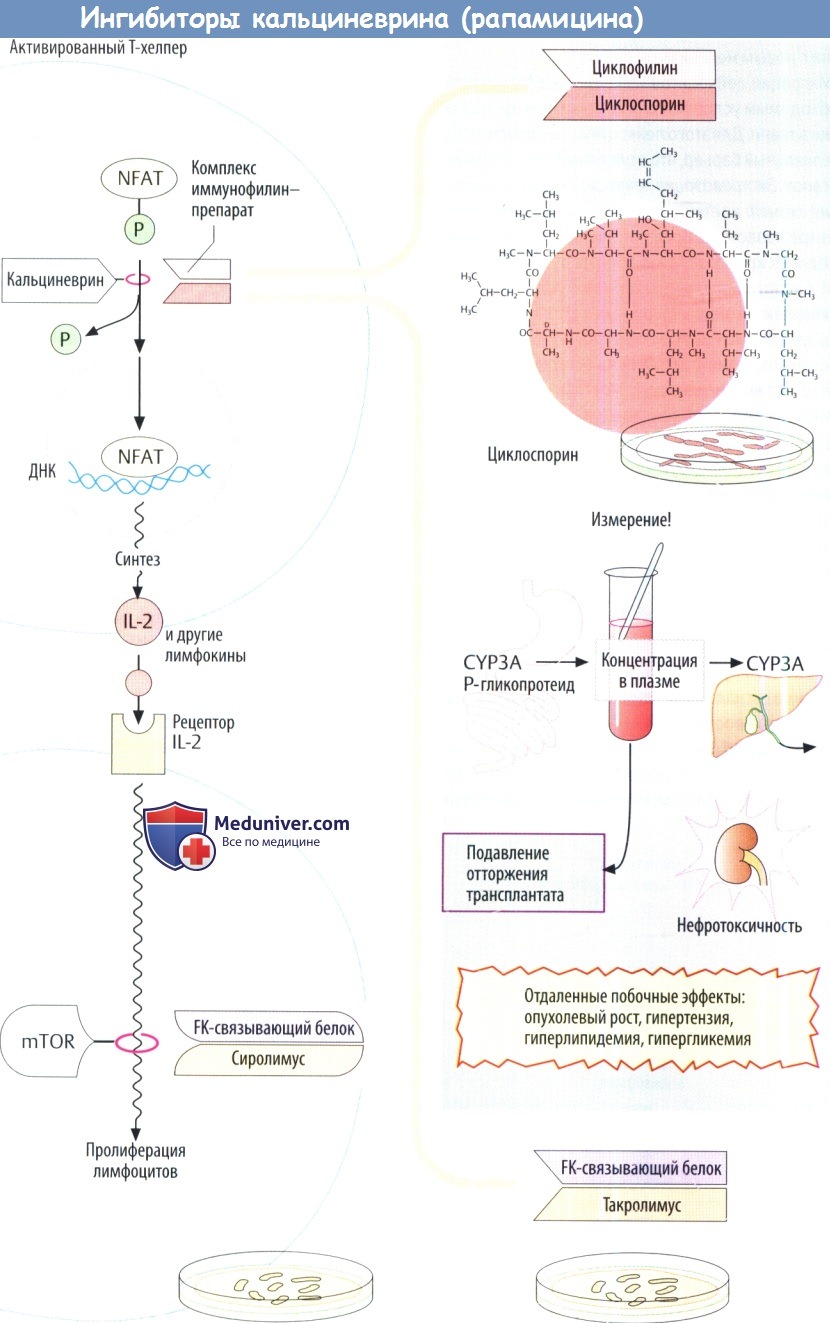
II. Подавление продукции цитокина и его действия. Глюкокортикоиды модулируют экспрессию множества генов. В частности, за счет этого эффект; ингибируется продукция IL-1 и IL-2, что объясняет супрессию зависимых от Т-клеток иммунных ответов. Кроме того, глюкокортикоиды нарушают образование воспалительных цитокинов и сигнальных молекул в других мишенях. Глюкокортикоиды используются при пересадке органов, аутоиммунных и аллергических заболеваниях. Системное применение несет в себе риск ятрогенного синдрома Кушинга.
Циклоспорин и родственные соединения ингибируют продукцию цитокинов, в частности IL-2. В отличие от глюкокортикоидов его применение не сопровождается множеством сопутствующих метаболических эффектов.
Анакинра — рекомбинантная форма эндогенного антагониста рецепторов IL-1, применяется при ревматоидном артрите.
Даклизумаб и базиликсимаб являются моноклональными антителами против рецепторов IL-2. Они состоят из Fab-фрагмента мышей и Fc-фрагмента человека. Их используют для подавления реакций отторжения трансплантата.
III. Нарушение метаболизма клетки в результате подавления пролиферации. В дозах ниже, чем требуюгся для лечения злокачественных опухолей, некоторые цитостатики также используются для иммуносупрессии (азатиоприн, метотрексат и циклофосфамид). Антипролиферативный эффект неспецифичен для лимфоцитов и касается как Т-, так и В-клеток.
Микофенолата мофетил оказывает более специфическое действие на лимфоциты, чем на другие клетки. Он ингибирует инозинмонофосфатдегидроге-назу, которая катализирует синтез пуринов в лимфоцитах. Препарат используется при острых реакциях отторжения ткани.
Циклоспорин связывается с белком циклофилином внутренней среды клетки, а образующийся комплекс ингибирует кальциневрин и, следовательно, продукцию IL-2.
Достижения в современной трансплантологии связаны в основном с введением в практику циклоспорина. В настоящее время он также используется при некоторых аутоиммунных заболеваниях, атопическом дерматите и других расстройствах.
Основным побочным эффектом циклоспорина является нефротоксичность. Поэтому его дозу необходимо титровать таким образом, чтобы уровень препарата в крови не был слишком высоким (риск повреждения почек) и не слишком низким (реакция отторжения). Проблема усложняется еще и тем, что циклоспорин является веществом, которое трудно использовать в лечебных целях. Пероральная био-доступность неполная. Происходит обратный транспорт препарата в полость кишечника посредством выносящего Р-гликопротеидного насоса в дополнение к метаболизму цигохромоксидазами подгрупп 3А.
Печеночные изоферменты CYP3A4 способствует выведению до поступления в системный кровоток и ответственны за выведение циклоспорина из системного кровотока. Различные лекарственные взаимодействия возникают в результате влияния CYP3, и Р-гликопротеида. При подборе оптимальной дозы следует обязательно контролировать уровень препарата в плазме.
При отторжении трансплантата требуется длительное лечение препаратами, вызывающими супрессию. Длительная иммуносупрессия несет в себе повышенный риск развития злокачественных опухолей. Факторами риска сердечно-сосудистых заболеваний могут быть нежелательные реакции — критический и важный момент в отдаленном прогнозе
Такролимус — антибиотик из группы макролидов получаемый из Streptomyces tsukubaensis. По сути oн действует, как и циклоспорин. Однако на молекулярном уровне его «рецептором» является не циклофилин, а так называемый FK-связывающий белок. Такролимус тоже используется для профилактики отторжения аллотрансплантата. По проницаемости эпителия он превосходит циклоспорин, что позволяет применять его местно при атопическом дерматите
Сиролимус (рапамицин) — еще один макролид, продуцируемый Streptomyces hydroscopicus. Иммуносупрессивное действие не связано с ингибированием кальциневрина. Он образует комплекс с FK белком, вызывая особые конформационные изменения, а комплекс далее ингибирует фосфатазу mTOP (мишени рапамицина млекопитающих). Последний управляет сигнальным путем, который начинается рецептором IL-2 и заканчивается активацией митоза в лимфоцитах. Следовательно, сиролимус ингибирует пролиферацию лимфоцитов. Препарат одобрен для профилактики отторжения трансплантата.
Структура и действие эверолимуса аналогичны таковым сиролимуса. Сиролимус также используется для покрытия стентов, которые установлены в атеросклеротических коронарных артериях для сохранения просвета сосудов после баллонной дилатации. Сиролимус предназначен для остановки процессов пролиферации в сосудистой стенке, которая может привести к сужению просвета. Темсиролимус используется при лечении почечноклеточного рака.
V. Ингибиторы миграции лейкоцитов. Натализумаб и эфализумаб — блокаторы интегрина с новым механизмом действия.
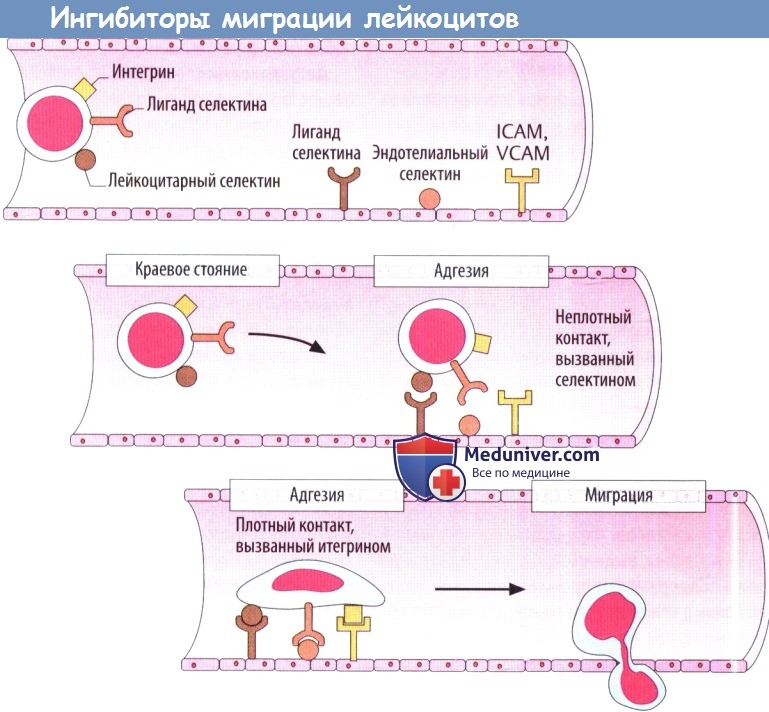
Миграция лейкоцитов из кровотока является необходимым условием для переноса иммунной реакции в ткани. Для этого лейкоциты преодолевают эндотелиальный барьер, что осуществляется в несколько этапов. Экстравазация лейкоцитов в месте повреждения тканей: клетки крови обычно располагаются в центре кровотока. Воспалительная вазодилатация замедляет кровоток, а лейкоциты лучше контактируют с эндотелиальными клетками. Адгезия: между лейкоцитами и эндотелиальными клетками образуются адгезивные мостики.
В первую очередь селектины с некоторыми углеводными остатками контактируют со смежными клетками. Мостики нестабильные, но открываются повторно, что замедляет движение лейкоцитов к эндотелию. Стабильная адгезия с остановкой лейкоцитов обусловлена интегринами в лейкоцитах и белками адгезии в эндотелии (ICAM — внутриклеточная молекула адгезии; VCAM — сосудистая клеточная молекула адгезии). Эндотелиальные клетки в воспаленной области связывают большее количество белков адгезии на мембране. Лейкоциты движутся между контактами эндотелиальных клеток, затем проходятсквозьокружающиебазальные мембраны и мигрируют в ткань, притягиваемые хемотаксическими сигнальными веществами, которые продуцируются при воспалений.
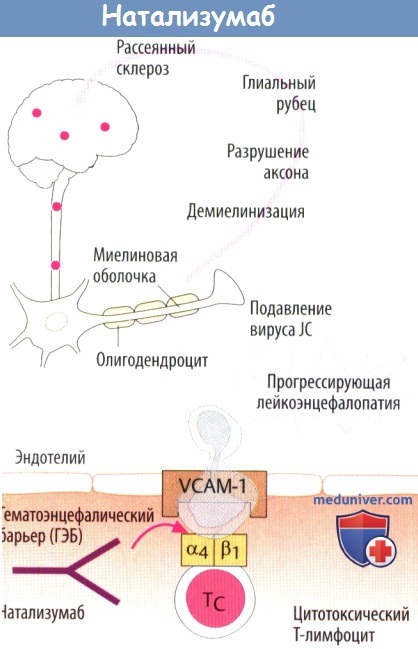
Натализумаб — человеческие антитела против α4-субъединицы интегринов. Интегрины являются гетеродимерными белками, состоящими из субъединиц α и β. Существуют разные изоформы. Связывание натализумаба блокирует миграцию Т-лимфоцитов в ЦНС. Это можно использовать при лечении рассеянного склероза. При данном аутоиммунном заболевании цитотоксические Т-лимфоциты атакуют олигодендроциты, которые продуцируют миелин в ЦНС. Редкой, но очень опасной нежелательной реакцией является прогрессирующая мультифокальная лейкоэнцефалопатия.
Она возникает в результате растормаживания вируса JC (от инициалов пациента у которого впервые выделен вирус). Данный вирус широко распространен, но обычно контролируется иммунной системой. Натализумаб является резервным препаратом, и его нельзя вводить вместе с другими иммуносупрессивными средствами против рассеянного склероза (IFN-β, глатирамера ацетат).
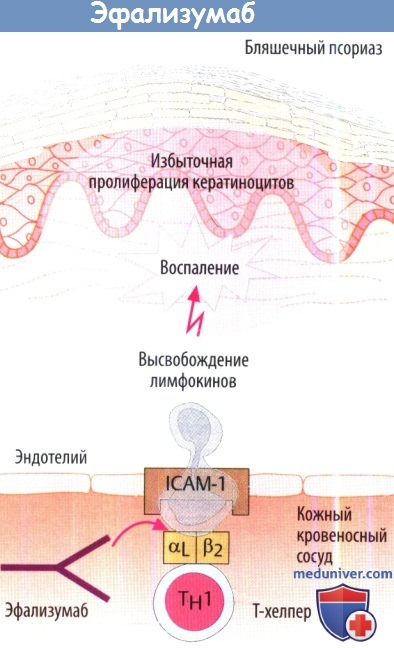
Эфализумаб используют при умеренной и тяжелой формах бляшечного псориаза. Известно, что данное заболевание аутоиммунное. Эфализума действует против а-субъединицы (αL, также известной как CD11) интегрина (LFA-1) Т-хелперов. Это останавливает миграцию лимфоцитов из сосудистого русла. Кроме того, блокируется контакт с клетками пораженной области кожи (клетки, несущие антиген кератиноциты). Побочные эффекты: выраженные гриппоподобные симптомы, повышение числа лимфоцитов. Из-за случаев прогрессирующей мультифокальной лейкоэнцефалопатии, о которых сообщалось у некоторых пациентов после лечения эфализумабом, данный препарат в настоящее время не используется в США и ЕС.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021