Интерстициальная пневмония у взрослых что это
Интерстициальное заболевание легких
Интерстициальные заболевания легких – группа болезней, поражающих легочную ткань, преимущественно хронического характера. Возникают вследствие поражения альвеолярных мешочков. При отсутствии надлежащего лечения приводят к пневмофиброзу, повреждению альвеолярных стенок, эндотелии легочных капилляров альвеолиту.
Причины возникновения
Сегодня известны три группы причин, провоцирующих возникновение и развитие интерстициальных заболеваний. К ним относятся:
Симптоматика заболевания
Поскольку речь идет сразу о группе болезней легких, единую клиническую картину сформировать нельзя. Однако для всех из них характерно постепенное нарастание симптомов. Если у пациента, например, наблюдается дыхательная недостаточность, со временем она приведет к снижению выносливости. Легкое покашливание перерастет в непрекращающийся, сухой кашель. Также на поздних стадиях практически всегда происходит посинение губ и/или ступней и опухание пальцев рук.
Диагностика и лечение
Интерстициальные заболевания легких можно обнаружить при помощи КТ-сканирования или рентгенографии. На снимке отчетливо видно затемнение легких, наличие в них единичных мелких узелков или целой сетки. В особо запущенных случаях (например, при прогрессирующем пневмофиброзе) можно наблюдать полное или частичное разрушение альвеол и формирование кистозных образований. Из-за них легкие приобретают схожесть с медовыми сотами.
После того, как заболевание обнаружено, наступает очередь анализов. Врач отправляет пациента проверить содержание кислорода в крови и протестировать работу легких. В отдельных случаях, если КТ-сканирование не дает однозначных результатов, назначается биопсия. Хирургическим путем из легкого изымается ткань для анализа.
Лечение интерстициальных заболеваний зависит от степени их развития. При относительно легких болезнях (саркоидозе, аллергическом альвеолите экзогенной этиологии) назначают кус противовоспалительных препаратов и противорубцовую терапию. При пневмофиброзе и схожих с ним заболеваниях не обойтись без кислородной терапии и продолжительной реабилитации. В особо тяжелых случаях может потребоваться трансплантация легких.
С каким бы интерстициальным заболеванием легких вы ни столкнулись, пульмонолог медицинского центра «Гармония» сможет помочь. Наша клиника оснащена современным оборудованием, которое позволяет диагностировать болезни на самых ранних стадиях. А опытный врач подберет лечение, подходящее именно вам. Поэтому, если ощущаете, что самочувствие ухудшилось, не затягивайте с визитом. Запишитесь на прием по телефону или через онлайн-форму.
Оглавление:
Пневмония, или воспаление легких – острое локальное воспаление легочной ткани инфекционного характера. Чаще поражаются респираторные отделы легких – альвеолы, бронхиолы. Воспаление может затрагивать интерстициальную ткань, однако в современной классификации его относят к альвеолитам.
В России ежегодно пневмонию диагностируют примерно у 1,5 млн человек. В группе болезней органов дыхания на воспаление легких приходится 50 % летальных исходов. В среднем смертность от заболевания составляет 21 случай на 100 тыс. жителей. Среди всех причин смертности воспаление легких находится на 5 месте после сердечно-сосудистых патологий, онкологических заболеваний, травм и отравлений.
Чаще других риску развития пневмонии подвержены дети до двух лет и люди старше 65 лет. Вероятность летального исхода выше у людей пожилого возраста, имеющих сопутствующие заболевания.
Возбудители болезни
В большинстве случаев пневмония вызывается инфекционными агентами – бактериями, вирусами, грибками.
Бактериальная пневмония находится на первом месте по частоте случаев. Чаще всего ее вызывают грамположительные организмы: пневмококки (40-60 % случаев), стафилококки и стрептококки (от 2 до 5 %). К грамотрицательным бактериям, провоцирующим возникновение воспаления легких, относятся палочки (кишечная, гемофильная), протеи, легионеллы.
Неинфекционные причины
Воспаление легких может развиваться вследствие воздействия аллергенов, токсичных веществ, радиации (в основном, после лучевой терапии у больных с онкопатологией), на фоне травм и ожогов, попадания в дыхательные пути инородных частиц.
Сопутствующие факторы
Виды пневмонии
Классификация заболевания проводится по разным критериям.
По характеру течения выделяют острую пневмонию (до 3 недель) и затяжную (до 2 месяцев). Заболевание может иметь легкую, среднюю или тяжелую степень течения.
В зависимости от того, развилась ли болезнь самостоятельно, или на фоне другой патологии, ее делят на первичную и вторичную. Также выделяют аспирационные, посттравматические, постожоговые, постинфарктные воспаления легких.
Пневмония может быть односторонней и двухсторонней. По степени поражения ее разделяют на:
Пневмонии делят на внебольничные, внутрибольничные (госпитальные) и атипичные.
Внебольничные (амбулаторные, или домашние) – возникают вне лечебного учреждения. Они могут вызываться инфекционными возбудителями на фоне нормального или сниженного иммунитета либо развиваться вследствие аспирации дыхательных путей.
Госпитальные пневмонии делятся на ранние, которые развиваются в срок до 5 суток пребывания больного в стационаре, и поздние, развивающиеся не ранее шестых суток госпитализации. Они, как правило, имеют тяжелое течение и устойчивы к антибиотикотерапии. Подразделяются на аспирационные, вентиляционные (после длительного нахождения на ИВЛ), цитостатические (вследствие приема препаратов химиотерапии) и воспаления легочной ткани, развивающиеся после пересадки органов.
Атипичные пневмонии вызываются нетипичными возбудителями (простейшие, вирусы) и имеют отличную от традиционного воспаления легких клиническую картину.
Осложнения заболевания
Симптомы воспаления легких
Основные признаки типичной пневмонии, вызванной бактериями, – резкое повышение температуры, продуктивный кашель с обильным выделением мокроты, в которой часто появляется примесь гноя. Боль в грудной клетке присутствует при вовлечении в процесс одной или нескольких долей легких, при очаговом поражении болевого синдрома нет или он возникает очень редко. При массивной площади поражения присоединяется одышка.
Атипичный вариант заболевания характеризуется постепенным началом, кашель может быть сухим, без отделения мокроты. Присутствуют симптомы со стороны других органов: головная боль, боли в мышцах, боль и першение в горле, общая слабость. Начало атипичной пневмонии может протекать без температуры (часто такие случаи отмечаются при воспалении легких, вызванном covid-19), однако она, как правило, поднимается при развитии заболевания.
Обращаться к врачу следует при первых признаках заболевания – повышении температуры, кашле, ухудшении общего состояния. При обращении за медицинской помощью на первой стадии развития воспаления и правильном подборе терапии течение болезни будет легче, а риск развития осложнений – ниже.
Лечением пневмонии, если оно проходит в стационаре, занимается врач-пульмонолог. В поликлинике больные, как правило, обращаются к терапевту, который при необходимости направляет их к узким специалистам.
Заразность болезни
Теоретически можно говорить о том, что воспаление легких – заразное заболевание, так как оно вызывается бактериями и вирусами. Однако практически невозможно заболеть им просто находясь рядом с человеком, которому уже поставлен этот диагноз.
Во-первых, заболевание вызывается микроорганизмами, постоянно находящимися во внешней среде, и с которыми люди так или иначе контактируют в повседневной жизни. Для того чтобы при этом человек заболел, должны присутствовать и другие факторы – ослабленный иммунитет, нахождение в закрытых непроветриваемых помещениях, вредные привычки, плохое питание.
Во-вторых, микробы, вызвавшие воспаление легких у одного человека, не обязательно спровоцируют его же у другого. При контакте с больным можно заболеть другим респираторным заболеванием, например бронхитом или ОРВИ.
В-третьих, заразность микробов наиболее высока, когда они находятся в верхних дыхательных путях и выделяются при незначительном кашле, чихании. Воспалительный процесс в легких развивается при преодолении возбудителями первичной защиты и наличии сопутствующих факторов, вирулентность бактерий и вирусов при этом снижается.
Таким образом, больные с воспалением легких не представляют большей опасности для окружающих, чем пациенты с обычным респираторным заболеванием. Их не помещают в инфекционные стационары или отдельные боксы, за некоторыми исключениями, например, в случае с ковидной пневмонией. Однако во всех ситуациях не стоит пренебрегать соблюдением разумных мер безопасности и ограничением контактов здоровых людей с больным.
Лечение пневмонии
Диагноз заболевания ставится на основе жалоб пациента, общего осмотра, аускультации легких, данных рентгеновских снимков, компьютерной или магнитно-резонансной томографии. Пациенту назначают общий анализ крови и мочи, бакпосев мокроты.
Интерстициальная болезнь легких (часть 1)
Стенограмма клинического разбора, представленного доктором Рощиной Т.В. на II Международном Интернет Конгрессе специалистов по внутренним болезням.
Профессор Драпкина О.М.: – Клинико-анатомическую конференцию проведет академик Ивашкин Владимир Трофимович, она будет посвящена интерстициальной болезни легких. Случай доложит лечащий доктор той пациентки, Рощина Татьяна Викторовна.
(00:20) Заставка: Интерстициальная болезнь легких
Пациентка, которая довольно длительное время наблюдалась с диагнозом «интерстициальная болезнь легких», в очередной раз поступила в клинику, у нее развивается острая дыхательная недостаточность. Эта острая дыхательная недостаточность расценивается как результат пневмонии, пациентка умирает, а на секции, на аутопсии обнаруживают злокачественную опухоль легких и все признаки острого респираторного дистресс-синдрома. Поэтому этот треугольник – интерстициальная болезнь легких, злокачественное образование легких и острый респираторный дистресс-синдром – и составит основу, вокруг которой и будет раскручиваться вся клиническая интрига. Пожалуйста, Татьяна Викторовна.
Начиная с 2011 года, у пациентки появляется одышка при выполнении ранее привычных физических нагрузок, и появление одышки заставляет пациентку обратиться за медицинской помощью амбулаторно. Ей выполняется флюорография и в дальнейшем проводится обследование в Городской клинической больнице №83. В клинической больнице пациентке проводится спирометрия, бодиплетизмография, ей выполняется исследование лабораторных анализов, в том числе фибробронхоскопия, которая выявила двусторонний атрофический бронхит и при цитологическом исследовании пролиферацию бронхиального эпителия.
На основании проведенного обследования был установлен диагноз – интерстициальное заболевание легких: идиопатический легочный фиброз, дыхательная недостаточность 1 степени. На данном слайде представлены те критерии Американского торакального общества, Европейского респираторного общества, которые необходимы для постановки диагноза интерстициальной болезни легких при отсутствии хирургической биопсии легкого.
У нашей пациентки были набраны все критерии, за исключением возраста, пациентка была младше 50 лет. Таким образом, этот диагноз можно считать достоверным для этой пациентки, и он был установлен в 83-й больнице, и с ним она была выписана. Однако в момент проведения бронхоскопии у пациентки внезапно возникла остановка дыхания и потеря сознания, в связи с чем для дальнейшего лечения она была переведена в отделение интенсивной терапии, где наблюдалась уже неврологами по поводу острой гипоксической энцефалопатии. Спустя месяц неврологическая симптоматика регрессировала, и пациентка в удовлетворительном состоянии была выписана из 83-й больницы, однако сохраняющаяся одышка послужила поводом для обращения за медицинской помощью и госпитализации в декабре 2011 года в нашу клинику.
Какова тактика, современное лечение интерстициальных заболеваний легких, в соответствии с рекомендациями Американского торакального общества и Европейского респираторного общества? Существуют несколько подходов. Это либо пробная терапия высокими дозами стероидами, либо комбинированная терапия – это преднизолон в сочетании с цитостатиками, пульс-терапия преднизолоном и препарат ацетилцистеин в высоких дозах.
Когда нужно начинать лечение? Лечение должно начинаться при постановке диагноза или получении объективных доказательств прогрессирования заболевания, или при среднетяжелом или тяжелом течении процесса. Поскольку у нашей пациентки было прогрессирование заболевания, среднетяжелое течение процесса, мы выбрали тактику и назначили препарат метипред. Метипред был назначен в дозе 20 мг/сутки. Пациентка принимала этот препарат всего на протяжении месяца, у нее начала изменяться внешность, и она самостоятельно препарат отменила.
В марте 2012 года пациентка вновь госпитализирована к нам в отделение для того, чтобы мы провели повторное обследование и определили дальнейшую тактику ведения этой больной. Учитывая прогрессирование заболевания, прогрессирование одышки, ухудшение по компьютерной томографии, была изменена лечебная тактика и уже назначено два препарата: к системным глюкокортикостероидам был добавлен препарат азатиоприн. Пациентка была выписана из отделения с рекомендациями обратиться к нам в клинику через месяц после того, как она была выписана, то есть в апреле 2012 года.
Пациентка же обратилась к нам только в августе 2012 года. За это время у нее резко усилилась одышка, усилился кашель, она практически перестала выходить из дома, перестала обслуживать себя и отметила изменение концевых фаланг пальцев: у нее появились «барабанные пальцы» и изменение ногтей в виде часовых стеклышек. И 28 августа 2012 года пациентка госпитализирована к нам в отделение.
Пациентка родилась в Москве, по профессии она администратор, в 1997 году пациентка перенесла холецистэктомию, из аллергологического анамнеза на виферон у пациентки наблюдалась крапивница. Пациентка не курит, вредных привычек не имеет. При поступлении состояние пациентки средней тяжести. Обращал на себя внимание диффузный цианоз, частота дыхательных движений 22/мин, сатурация по пульсоксиметру 92%. Обращала на себя внимание деформация фаланг пальцев в виде барабанных палочек и ногтей в виде часовых стеклышек. Перкуторно-коробочный звук, дыхание жесткое, выслушивалась крепитация по всем легочным полям. Тоны сердца были ясные, ритмичные, частота сердечных сокращений – 120/мин, артериальное давление – 120/70. Живот был мягкий, безболезненный, периферических отеков не было, печень не увеличена.
На данном слайде представлены причины быстропрогрессирующей одышки у больных с интерстициальными заболеваниями легких. Это возможно присоединение гнойного воспалительного процесса, развитие опухоли, пневмоторакса, тромбоэмболии мелких ветвей легочной артерии. Все эти возможные причины мы имели в виду, когда проводили обследование, когда встретились с этой пациенткой вновь, однако провести компьютерную томографию мы не успели, поскольку пациентка провела в нашей клинике всего 17 часов. На данном слайде мы видим, что в клиническом анализе крови обращал на себя внимание лейкоцитоз – 17,7*109/л, повышение уровня калия, аланиновой и аспарагиновой трансаминаз, креатинина и глюкозы.
Основное заболевание – интерстициальное заболевание легких: идиопатический легочный фиброз в стадии формирования «сотового легкого», длительно леченный глюкокортикостероидами и цитостатиками. Эмфизема легких, пневмосклероз, легочное сердце. Внебольничная двусторонняя полисегментарная пневмония.
Осложнения: хроническая дыхательная недостаточность, острая дыхательная недостаточность от 29 августа 2012 года, тромбоэмболия мелких ветвей легочной артерии, терминальный отек легких, терминальный отек головного мозга, реанимационные мероприятия. Сопутствующие заболевания: желчно-каменная болезнь, холецистоэктомия в 1997 году и хронический билиарный панкреатит вне обострения.
Здесь показана периневральная инвазия клеток аденокарциномы, опять-таки на фоне диффузной воспалительной реакции. То есть, в процесс вовлечены нервы, нервная система. Далее, сосудистая инвазия, поражение стенки сосудов клетками злокачественной опухоли. Видите, метастаз аденокарциномы в лимфатический узел, отчетливо совершенно прослеживаются атипичные клетки, которые как бы врываются в этот воспалительный инфильтрат. А это метастаз аденокарциномы в надпочечнике. То есть, неврологически ничего в надпоечниках не было, но при секции мы видим метастаз аденокарциномы в надпочечнике.
Что привлекает особое внимание и что, по всей вероятности, объясняет это острейшее развитие финальной стадии болезни у нашей пациентки с нарастанием тяжелой одышки, цианоза, тахипноэ и так далее, и так далее, и с полиорганными изменениями – это обнаружение гиалиновых мембран. Гиалиновые мембраны покрывают значительные площади альвеол, видны также участки слущенного эпителия в альвеолах, и гиалиновые мембраны служат как бы замещающим фактором. Это говорит о том, что пациентка умирала в статусе острого респираторного дистресс-синдрома. Вот гиалиновые мембраны, они здесь хорошо показаны. Гиалиновые мембраны патогномоничный морфологический признак острого респираторного дистресс-синдрома.
Это крупнокапельная жировая дистрофия печени – вы помните значительное повышение аланиновой и аспарониновой трансаминазы. По всей вероятности, это исходное состояние печени, жировая дистрофия, и острая реакция с повышением активности ферментов была усугублена развившейся на фоне острого респираторного дистресс-синдрома гипоксемии, то есть гипоксическим повреждением печени. Вы помните также подъем глюкозы у нашей пациентки, и вы видите на этой картинке мелкий жировой некроз поджелудочной железы, следовательно, поджелудочная железа тоже отреагировала на этот респираторный дистресс-синдром.
Далее почка. Если клубочки находятся в относительно сохранном состоянии, то в правом верхнем углу наверху вы видите канальцы в состоянии некротических изменений. То есть, речь идет о некротическом поражении канальцев почек. Таким образом, патологоанатомический диагноз после гистологического исследования звучал так. Основное комбинированное заболевание включало два конкурирующих заболевания.
Во-первых, множественный периферический рак нижних долей обоих легких (гистологически – очаги инвазивной и минимально инвазивной смешанной аденокарциномы – участки муцинозной, микропапиллярной и немуцинозной аденокарциномы с бронхиоло-альвеолярным характером роста) с прорастанием париетальной плевры и распространенной – я нотирую внимание, уважаемые коллеги, с прорастанием париетальной плевры, это важно нам для дальнейших рассуждений – и распространенной периневральной и васкулярной инвазии. Метастазы рака в перибронхиальный лимфатический узел и левый надпочечник.
Второе конкурирующее заболевание – это идиопатический легочный фиброз (гистологически – обычная интерстициальная пневмония). Может возникнуть вопрос, почему наряду с периферическим раком легкого в качестве конкурирующего заболевания поставлен идиопатический легочный фиброз, который по своим первоначальным проявлениям, конечно, не мог вызвать такую картину. Я думаю, из наших дальнейших рассуждений станет понятным.
Осложнения – это жировая дистрофия миокарда, диффузный жировой гепатоз, некротический нефроз, который обусловил развитие острой почечной недостаточности, и острый респираторный дистресс-синдром, отек легких и реанимационные мероприятия. В связи с этим возник вопрос: можно ли раньше было, на более раннем этапе, догадываться о возможности этой бронхиоло-альвеолярной карциномы легких? Речь идет о бронхиоло-альвеолярной карциноме легких, можно ли было догадываться на основании клинических или рентгенологических данных? И второй вопрос, очень важный: осложнением чего явился острый респираторный дистресс-синдром? Осложнением легочного фиброза, обычной интерстициальной пневмонии – или он явился осложнением бронхиолоальвеолярноклеточной карциномы?
Это очень важные вопросы для нас. Как вы помните, у пациентки «барабанные пальцы» и «часовые стекла» образовались за три месяца до ее смерти. Обычно в учебниках пишут: «барабанные пальцы», «часовые стекла» у пациентов с легочным заболеванием, основные причины – это или хроническая инфекция, или рак легкого. Но никогда ни в одном учебнике не нотируется внимание, сколько требуется времени для того, чтобы развились «барабанные пальцы» и «часовые стекла». И как учитывать?
И на примере этой пациентки мы видим, что наличие злокачественной опухоли может вызывать развитие изменений концевых фаланг пальцев и ногтевого ложа по типу «часовых стекол» быстро, в течение трех месяцев. Следовательно, будущим клиницистам и молодым клиницистам, и не очень молодым клиницистам следует обращать внимание на этот, казалось бы, классический симптом, которым пользовались наши великие предшественники, а мы начинаем об этом забывать.
Интерстициальная пневмония с аутоиммунными признаками (ИПАП): мультидисциплинарный диагноз в пульмонологии и ревматологии
Диагноз идиопатической интерстициальной пневмонии с аутоиммунными признаками (ИПАП) объединяет пациентов с идиопатической интерстициальной пневмонией и рядом клинических, серологических и/или морфологических проявлений, указывающих на наличие системного аутоиммунного процесса, который, однако, не соответствует современным критериям определенного системного заболевания соединительной ткани. Результаты клинических исследований указывают на значительную неоднородность больных данной группы. В обзоре литературы обсуждаются классификационные критерии ИПАП, а также дальнейшие перспективы их применения для улучшения диагностики и лечения пациентов с данной патологией.
Идиопатические интерстициальные пневмонии (ИИП) представляют собой группу диффузных воспалительных и/или фибротических заболеваний легких, объединенных на основании сходных клинических, рентгенологических и гистологических признаков. Диагноз ИИП требует исключения известных причин интерстициальной пневмонии, таких как воздействие экзогенных факторов, токсические эффекты лекарственных препаратов или системное заболевание соединительной ткани (СЗСТ) [1]. Последние представляют собой группу аутоиммунных заболеваний, таких как ревматоидный артрит, системная красная волчанка, идиопатические воспалительные миопатии, синдром Шегрена, системная склеродермия и смешанное заболевание соединительной ткани. Интерстициальная пневмония (ИП) может быть одним из проявлений СЗСТ, причем в части случаев ее развитие предшествует появлению других симптомов заболевания 2.
У пациентов с ИИП могут наблюдаться отдельные клинические симптомы или серологические маркеры, характерные для аутоиммунной патологии, но не позволяющие установить диагноз какого-либо СЗСТ в связи с отсутствием всех необходимых критериев 6. Ранее исследователи предлагали различные критерии и термины для описания вышеуказанной когорты пациентов 8, в связи с чем длительное время отсутствовала возможность проведения мас штабных исследований, посвященных диагностике и лечению данной патологии.
В 2015 году экспертами Европейского респираторного общества (ERS) и Американского торакального общества (ATS) был предложен термин «интерстициальная пневмонии с аутоиммунными признаками (ИПАП)» [10]. Этим термином обозначают ИИП, сопровождающуюся клиническими, серологическими и/или морфологическими признаками, которые указывают на наличие системного аутоиммунного процесса, но не соответствуют современным критериям конкретного СЗСТ. Следует отметить, что это понятие было введено группой пульмонологов и ревматологов, в первую очередь, для удобства диагностики и унификации критериев включения пациентов в клинические исследовании, однако оно не может служить основанием для выбора метода лечения.
Критерии ИПАП
Классификационные критерии ИПАП распределены на три группы, или домена – клинический, серологический и морфологический (табл. 1) [10]. Для установления диагноза ИПАП 2 необходимы наличие ИП по данным компьютерной томографии органов грудной клетки высокого разрешения (КТВР) и/или хирургической биопсии легкого и тщательное клиническое обследование для исключения известных причин ИП, в том числе СЗСТ. Кроме того, диагноз ИПАП предполагает наличие соответствующих классификационных критериев, относящихся по крайней мере к двум из указанных групп.
| 1. | Наличие интерстициальной пневмонии (по данным КТВР или хирургической биопсии легкого) + |
| 2. | Исключение альтернативных причин ИП + |
| 3. | Несоответствие критериям конкретного СЗСТ + |
| 4. | Наличие по крайней мере одного критерия из 2 или более групп: А) Клинической Б) Серологической В) Морфологической |
| А. | Клиническая группа: |
| 1) | Трещины на коже дистальных фаланг пальцев («рука механика») |
| 2) | Кожные язвы дистальных фаланг пальцев |
| 3) | Артриты или скованность в утренние часы ≥60 мин с поражением нескольких суставов |
| 4) | Телеангиэктазии на коже ладоней |
| 5) | Феномен Рейно |
| 6) | Беспричинный отек пальцев |
| 7) | Беспричинная стойкая сыпь на коже разгибательной поверхности пальцев (симптом Готтрона) |
| Б. | Серологическая группа: |
| 1. | Антинуклеарные антитела (АНА) в титре ⩾1:320 при наличии диффузного, гранулярного или гомогенного паттерна свечения или a) АНА при наличии нуклеолярного паттерна (в любом титре) или б) АНА при наличии центромерного паттерна (в любом титре) |
| 2. | Ревматоидный фактор в титре ⩾2N |
| 3. | Антитела к циклическому цитруллинированному пептиду (АЦЦП) |
| 4. | Антитела к двуспиральной ДНК (анти-дсДНК) |
| 5. | Анти-Ro (SS-A) |
| 6. | Анти-La (SS-B) |
| 7. | Антитела к рибонуклеопротеину |
| 8. | Анти-Smith |
| 9. | Антитела к топоизомеразе (Scl-70) |
| 10. | Антитела к тРНК-синтетазе (Jo-1, PL-7, PL-12 и другие, в том числе EJ, OJ, KS, Zo, tRS) |
| 11. | Анти-PM-Scl |
| 12. | Анти-MDA-5 |
| С. | Морфологическая группа: |
| 1. | Предполагаемый паттерн по данным КТВР: a) Неспецифическая интерстициальная пневмония (НСИП) б) Организующая пневмония (ОП) в) Перекрест НСИП и ОП г) Лимфоцитарная интерстициальная пневмония (ЛИП) |
| 2. | Гистологический паттерн по данным биопсии легкого: a) НСИП б) ОП в) Перекрест НСИП и ОП г) ЛИП д) Интерстициальные лимфоидные узелки с герминативными центрами |
| 3. | Внепаренхиматозные легочные и внелегочные проявления (в сочетании с интерстициальной пневмонией) a) Необъяснимый плевральный выпот или утолщение плевры б) Необъяснимый перикардиальный выпот или утолщение перикарда в) Необъяснимое заболевание дыхательных путей (по данным легочных функциональных тестов визуализационных методов или биопсии) г) Необъяснимая легочная васкулопатия |
В клиническую группу критериев включены симптомы, относительно специфичные для ряда СЗСТ, такие как феномен Рейно, телеангиэктазии кожи ладоней, язвы дистальных фаланг пальцев 12. Тем не менее, сами по себе они не позволяют установить диагноз СЗСТ. В то же время алопеция, фотодерматит, язвы слизистой оболочки полости рта, снижение массы тела, сухой синдром, изолированные миалгия и артралгия не были включены в перечень признаков ИПАП в связи с низкой специфичностью.
Морфологическая группа критериев ИПАП включает в себя такие рентгенологические паттерны ИП, как неспецифическая интерстициальная пневмония (НСИП), организующая пневмония (ОП), перекрест НСИП и ОП, лимфоцитарная пневмония (ЛИП). Данные варианты легочного поражения достаточно часто встречаются при ИП, ассоциированных с СЗСТ (СЗСТ-ИП) 15. Обычная интерстициальная пневмония (ОИП) (рис. 2) также может быть выявлены у пациентов с СЗСТ, хотя и встречается реже [17], поэтому она не является критерием исключения ИПАП. Тем не менее, в отличие от НСИП, ОП и ЛИП, картина ОИП не входит в перечень морфологических признаков ИПАП.
Результаты клинических исследований
С момента введения критериев ИПАП в 2015 г. были опубликованы результаты ряда клинических исследований, в основном ретроспективных, в которых изучались проявления, течение и исходы этого заболевания. Хотя основной целью разработки классификационных критериев ИПАП было выделение относительно однородной группы пациентов, тем не менее, в проведенных исследованиях выборки характеризовались значительной вариабельностью [18].
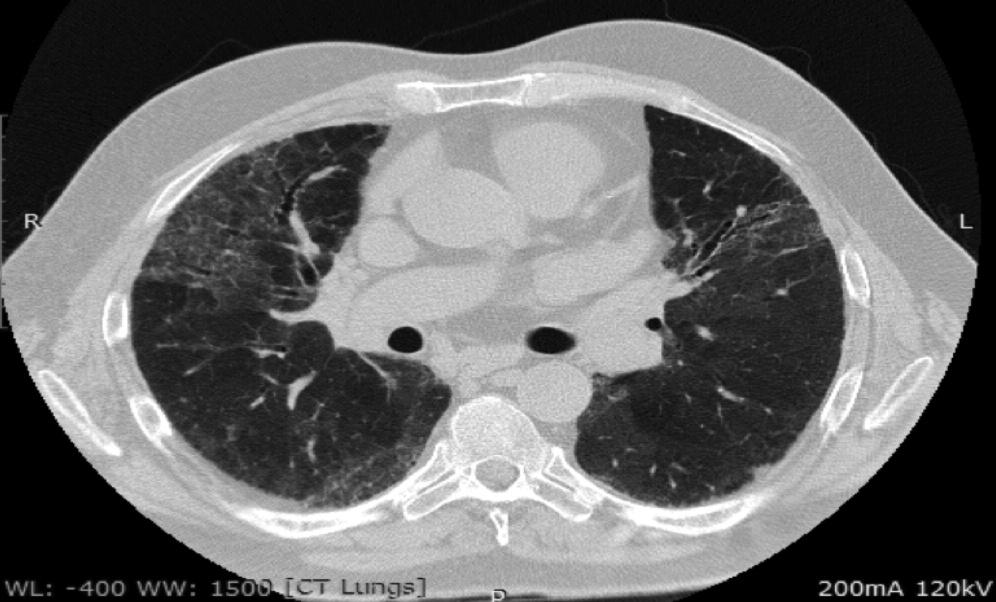
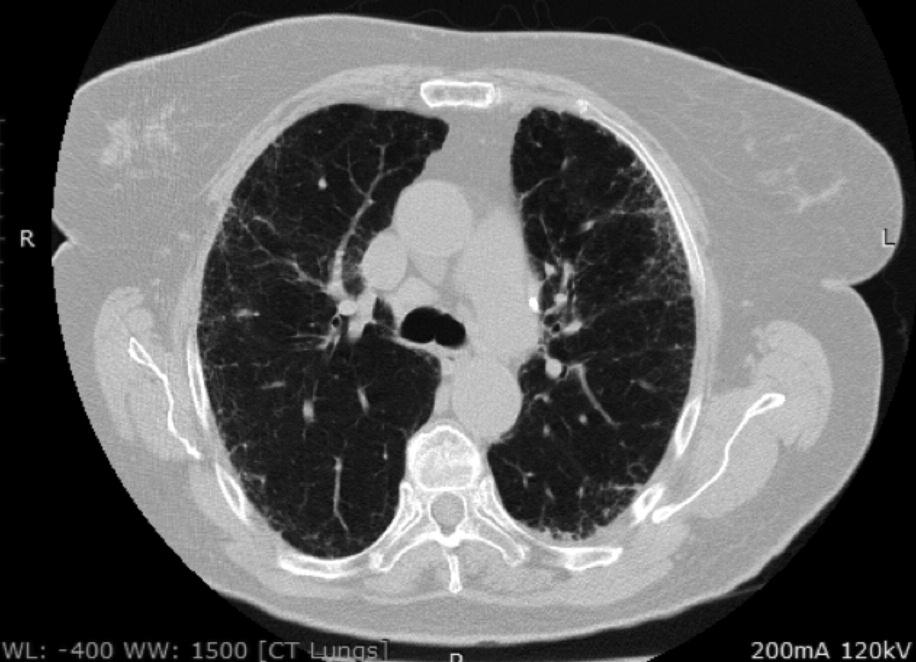
В одном из наиболее крупных исследований J. Oldham с соавт. описали группу из 144 пациентов с ИПАП: средний возраст больных составил 63 года, а приблизительно у половины из них основным рентгенологическим и/или гистологическим паттерном была ОИП [19]. У 14,6% пациентов имелись клинические и серологические критерии диагноза, у 8,3% – клинические и морфологические, у 26,4% – все три критерия. У пациентов с ИПАП и идиопатическим легочным фиброзом (ИЛФ) смертность оказалась сходной. Однако при дополнительном анализе результатов исследования было показано, что выживаемость больных ИПАП зависела от рентгенологического варианта поражения легких. При наличии картины ОИП прогноз был сходным с таковым больных с ИЛФ, тогда как у пациентов с другими рентгенологическими паттернами выживаемость была значительно выше и сопоставимой с таковой при ИП, ассоциирующейся с СЗСТ. По данным многофакторного анализа, независимыми неблагоприятными прогностическими факторами были возраст и снижение диффузионной способности легких для монооксида углерода.
В другом исследовании S. Chartrand и соавт. описали 56 пациентов с ИПАП в возрасте в среднем 54,6 года, большинство из которых были некурящими [20]. Наиболее частым паттерном ИП при КТВР и биопсии легкого была НСИП (51,8%), в то время как ОИП была выявлена всего у 9% пациентов. Более чем у половины пациентов имелись классификационные критерии, относящиеся ко всем трем группам, у 37,5% – серологические и морфологические, у 9% – клинические и морфологические, у 1,5% (1 пациент) – серологические и клинические критерии. Наиболее частым клиническими симптомами были феномен Рейно (39,3%), «рука механика» (28,6%) и симптом Готтрона (17,9%). Среди серологических критериев чаще всего встречались АНА в диагностическом титре (48,2%), анти-Ro/SS-A (42,9%), а также анти-тРНК-синтетазные антитела (АТСА) (35,7%). В исследуемой группе не отмечено ни одного летального исхода в течение периода наблюдения (284±141,3 недель).
К. Ahmad и соавт. наблюдали 57 больных с ИПАП, среди которых у 11,1% выявлены клинические и серологические классификационные критерии, у 7% – клинические и морфологические критерии, у 52,7% – серологические и морфологические критерии, у 29,2% – все три критерия [21]. Средний возраст пациентов с ИПАП составил 64,4±14 лет. Соотношение мужчин и женщин было приблизительно одинаковым. 34% пациентов курили. Наиболее частыми рентгенологическими паттернами были НСИП (42,1%) и ОИП (28%), тогда как основным внепаренхиматозным проявлением среди морфологических критериев оказалась легочная васкулопатия (17,5%). В течение периода наблюдения длительностью 16 месяцев умерли 7 пациентов. Много факторный анализ показал, что только курение было неблагоприятным прогностическим фактором. В то же время следует отметить, что в отличие от исследования J. Oldham и соавт., авторы не выявили различия выживаемости между группами пациентов с паттернами ОИП и НСИП.
В исследование Y. Ito и соавт. были включены 99 пациентов с ИПАП [22]. Один пациент с паттерном ОИП был исключен из анализа. Среди остальных 98 пациентов у 64,3% выявлен морфологический паттерн НСИП, у 20,4% – ОП, у 15,3% – перекрест НСИП и ОП. Пятилетняя выживаемость составила 71,1%, средняя продолжительность жизни после установления диагноза – 12,5 лет. Неблагоприятным прогностическим фактором было наличие паттерна НСИП, в то время как серологических предикторов прогноза выявлено не было. У 12 (12,2%) пациентов с ИПАП в динамике отмечено развитие СЗСТ (в большинстве случаев – ревматоидного артрита).
К. Yoshimura с соавт. выделили подгруппу пациентов с ИПАП среди больных с фибротическими вариантами хронической ИП (ОИП и фиброзным вариантом НСИП) [23]. Среди классификационных критериев ИПАП чаще других встречались морфологические (97% пациентов), реже – серологические (72%) и клинические (53%). У пациентов с ИПАП были отмечены более высокая выживаемость и более низкая обострений основного заболевания. При анализе подгрупп у пациентов с ИПАП, сочетавшейся с паттерном НСИП, выживаемость была выше, чем у больных с идиопатической НСИП. Также следует отметить, что в данном исследовании была выявлена тенденция к более высокой выживаемости пациентов с ИПАП, у которых определялся паттерн ОИП, по сравнению с таковой больных с ИЛФ.
H. Chung и соавт. изучали морфологические предикторы прогноза у пациентов с ИПАП [24]. У большинства из них (65,4%) при КТВР был выявлен паттерн типичной или возможной ОИП. По данным однофакторного анализа, достоверными рентгенологическими признаками, ассоциированными со снижением выживаемости, были ретикулярные изменения, зоны «сотового легкого», мозаичная вентиляция (при отсутствии эмфиземы), а также увеличение диаметра легочной артерии. В то же время наличие паттерна ОИП по данным КТВР, а также степень выраженности фиброзных изменений в легких не позволяли предсказать прогноз. По данным многофакторного анализа, независимыми достоверными предикторами неблагоприятного прогноза оказались только зоны «сотового легкого» и увеличение диаметра легочной артерии.
Таким образом, большинство данных, характеризующих группу пациентов с ИПАП, получены в ретроспективных одноцентровых исследованиях, что не позволяет экстраполироват их на всю популяцию таких больных. Этим также может частично объясняться выраженная неоднородность результатов вышеуказанных работ. В частности, в настоящее время остается до конца не выясненным прогностическое значение паттерна ОИП у пациентов с ИПАП: в ряде исследований прогноз в данной подгруппе пациентов не отличался от такового у пациентов ИЛФ, в то время как авторы других работ не выявили сходной закономерности. Кроме того, следует отметить, что в большинстве исследований не учитывалось влияние проводимой иммуносупрессивной терапии на прогноз пациентов с ИПАП. С одной стороны, это ограничивает прогностическое значение полученных результатов исследований, а, с другой стороны, не позволяет разработать рекомендации относительно рациональной фармакотерапии данной патологии.
Обсуждение
Действующие в настоящее время критерии ИПАП были предложены в 2015 г. группой экспертов в области пульмонологии и ревматологии с целью выделения отдельной когорты пациентов с ИИП и признаками системных аутоиммунных заболеваний, не соответствующих классификационным критериям конкретного СЗСТ. Преимущество предложенной классификации заключается в том, что она заменила множество введенных ранее и различающихся между собой определений ИПАП, а также стала основой для разработки критериев включения пациентов в клинические исследования, необходимые для изучения этой патологии.
С учетом новых данных, полученных в группах пациентов с ИПАП, ряд исследователей предлагают различные варианты пересмотра и доработки существующих критериев заболевания. В частности, G. Sambataro и соавт. [18] указывают на то, что наличие среди критериев ИПАП специфичных или даже патогномоничных признаков СЗСТ (симптом Готтрона [25], «рука механика», антитела к цитруллинированному пептиду, АТСА и ряд других аутоантител) не является рациональным. Это объясняется тем, что классификационные критерии ИПАП пересекаются с таковыми недифференцированного заболевания соединительной ткани 27 или с критериями, предложенными для ранней диагностики некоторых СЗСТ. Таким образом, в дебюте часть СЗСТ могут ложно классифицироваться как ИПАП. Примером могут служить критерии ранней диагностики системной склеродермии (very early diagnosis of systemic sclerosis, VEDOSS) [28], которые позволяют идентифицировать пациентов с высоким риском развития этого заболевания. Данная группа пациентов представляет большой интерес, особенно учитывая тот факт, что наличие явных «склеродермических» признаков позволяет не только установить диагноз, но и начать лечение на ранней стадии заболевания.
Кроме того, критериям ИПАП может соответствовать часть пациентов с антисинтетазным синдромом. Принимая во внимание отсутствие единых международных критериев этого синдрома, пациентам с ИП и антисинтетазными антителми (АТСА) может был установлен диагноз как антисинтетазного синдрома, так и ИПАП, несмотря на высокий риск развития у них остальных клинических проявлений классической триады симптомов (артрит и/или миозит) [29]. В отношении антисинтетазного синдрома существует еще одна проблема: с одной стороны, у всех пациентов с ИП необходимо определять антитела, ассоциированные с воспалительными миопатиями, однако на практике в большинстве клинических лабораторий полный перечень данных аутоантител рутинно не исследуется, поэтому антисинтетазный синдром может остаться недиагностированным.
Рядом исследователей были предложены дополнения к существующему определению ИПАП, в частности в серологическую группу критериев рекомендовано включение дополнительных антител, таких как АНЦА [30] и анти-Ku антитела [31]. Уже описаны когорты пациентов с АНЦА-позитивной ИП. Тем не менее, на настоящий момент количество данных относительно этой группы больных весьма ограничено. H. Yamada описал группу из 92 пациентов с ИП, которую ранее классифицировали как ИЛФ с наличием АНЦА [32]. В данной когорте у 35,8% отмечалось наличие АНЦАассоциированного васкулита в дебюте заболевания, еще у 17,4% пациентов он развился в течение нескольких лет после установления диагноза, а у оставшихся 46,8% пациентов ИП оставалась единственным клиническим проявлением заболевания. У части пациентов при биопсии легкого определялись признаки васкулита с поражением интерстиция и/или бронхов. Авторами статьи предложено два возможных механизма формирования интерстициальных изменений в легких при наличии АНЦА. Первый предполагает развитие интерстициального фиброза в результате субклинических альвеолярных геморрагий. В соответствии со второй гипотезой в ответ на образование воспалительных цитокинов миелопероксидаза экспрессируется на поверхности нейтрофилов, что может приводить к фиксации циркулирующих АНЦА с последующей дегрануляцией нейтрофилов и высвобождением активных форм кислорода, которые вызывают повреждение легочной ткани и развитию фиброза. Второй механизм, в частности, способен объяснить развитие АНЦА-ассоциированной ИП без признаков системного васкулита.
Таким образом, текущие диагностические критерии ИПАП охватывают весьма неоднородную группу пациентов, в связи с чем в большинстве исследований проводился поиск прогностических факторов выживаемости пациентов с ИПАП. Особый интерес вызывает морфологический паттерн ОИП, относительно значения которого в настоящее время нет единого мнения. Отсутствие ОИП в группе морфологических критериев ИПАП, с одной стороны, и более низкая выживаемость в данной подгруппе пациентов по результатам ряда исследований, с другой стороны, ставят вопрос о том, не должны ли пациенты с ОИП исключаться из клас сификационной группы ИПАП. Тем не менее, до появления данных проспективных исследований, подтверждающих внутригрупповую неоднородность ИПАП, выявления достоверных предикторов прогноза выживаемости и ответа на различные варианты терапии, пациентов с ОИП следует включать в группу ИПАП при наличии клинических и/или серологических критериев данного диагноза [33].
В ближайшем будущем необходимо проведение проспективных клинических исследований с целью изучения эффективности иммуносупрессивных, и возможно, антифибротических препаратов у пациентов с ИПАП. При большинстве вариантов СЗСТ-ИП и не-ОИП вариантах идиопатической ИП основной медикаментозной терапии являются глюкокортикостероиды, которые в части случаев сочетают с иммунодепрессивными и генно-инженерными биологическими препаратами, однако они неэффективны при ИЛФ, который представляет собой вариант идиопатической ИП с рентгенологическим паттерном ОИП [34,35]. Учитывая доказанную эффективность антифибротической терапии у пациентов с ИЛФ, не исключена возможность ее применения у части пациентов с ИПАП.
Заключение
Диагноз ИПАП был введен с целью унификации группы пациентов с ИП, у которых определяются отдельные симптомы системных аутоиммунных заболеваний. Тем не менее, данные клинических исследований указывают на то, что текущее определение ИПАП, вероятно, не позволяет выделить однородную популяцию больных. Уточнение классификационных критериев ИПАП может оказаться полезным для выделения отдельных вариантов этого состояния, отличающихся по клиническому течению, ответу на терапию и прогнозу, в том числе вероятности развития определенных системных заболеваний соединительной ткани. Для подтверждения данной гипотезы требуется проведение многоцентровых проспективных исследований с междисциплинарным подходом к диагностике и выбору терапии пациентов с ИПАП.

