Инвазивный аспергиллез что это
Инвазивный аспергиллез что это
Инвазивный аспергиллез является второй по частоте микотической инфекцией у больных с нейтропенией.
Эпидемиология инвазивного аспергиллеза. Основные возбудители инфекционного процесса — Aspergillus fumigatus (90 %), A. flavus, A. niger, A. terreus. В последнее время отмечается расширение спектра возбудителей инвазивного аспергиллеза. Частота заболевания составляет при трансплантации сердца и/или легких 19—26 %, при остром лейкозе 5—24 %, при аллогенной трансплантации костного мозга 4—9 %, при аутологичной трансплантации костного мозга без гемопоэтических факторов роста 0,5—6 %, с гемопоэтическими факторами роста менее 1%, при трансплантации печени 1,5-10%.
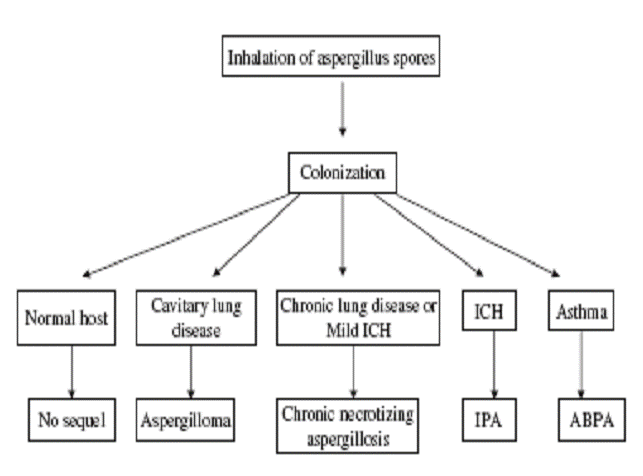
Патогенез инвазивного аспергиллеза. Входными воротами для Aspergillus spp. в большинстве случаев являются верхние дыхательные пути. Споры аспергиллов распространены повсюду, но определяется большая заселенность ими огнеупорных материалов, вентиляционных систем, некоторых продуктов питания (перец, орехи, пакетики с чаем, сыр, йогурт). Инфицирование аспергиллами возможно также через мелко распыляемую воду во время принятия душа или умывания.
Количество спор этих грибов резко возрастает в жаркие и влажные периоды года. Описаны случаи возникновения внутрибольничных эпидемий инвазивного аспергиллеза в госпиталях при проведении ремонтных работ в здании клиник или рядом.
В некоторых случаях развитию инвазивного аспергиллеза предшествует колонизация аспергиллами слизистых оболочек верхних дыхательных путей. Возможны и другие входные ворота для развития инвазивного аспергиллеза, например кишечник.
Факторы риска инвазивного аспергиллеза. В развитии инвазивного аспергиллеза велико значение длительно сохраняющейся нейтропении. S. L. Gerson и соавт. показали значимую корреляцию между длительностью нейтропении и частотой возникновения инвазивного аспергиллеза. Вероятность развития аспергиллеза прогрессивно возрастала после 6-го дня нейтропении, ежедневно на 1 %, и до 22-го дня, но в период с 22-го по 36-й день наблюдался стремительный прирост возможной инвазии аспергиллами, который увеличивался ежедневно уже на 4,5%.
Другим значимым фактором риска возникновения аспергиллеза является наличие болезни «трансплантат против хозяина» (ТПХ) у реципиентов аллогенных гемопоэтических стволовых клеток (ГСК). Так, инвазивный аспергиллез был причиной смерти 8 из 10 больных с признаками болезни ТПХ и только у 2 из 36 пациентов, не имевших этой болезни. Развитие инвазивного аспергиллеза в подобных случаях индуцируют как сама болезнь ТПХ, проявляющая мощное иммуносупрессивное действие, так и препараты, используемые для лечения данного осложнения: прежде всего длительное применение глюкокортикоидов, приводящее к функциональному повреждению макрофагов; назначение антитимоцитарного глобулина и других средств, оказывающих депрессивное действие на кроветворение. Подтверждением этому является более высокая частота инвазивного аспергиллеза при трансплантации ГСК от неродственного донора или не полностью совместимого родственного донора, достигающая 28 %.
В эксперименте in vitro выявлено ускорение роста A. fumigatus и A. flavus на 30—40 % в присутствии гидрокортизона. Данный эффект был дозозависимым, максимально интенсивный рост отмечался при определенной концентрации дексаметазона, соответствующей in vivo дозе преднизалона более 1 мг/кг. При анализе 27 случаев инвазивного аспергиллеза у реципиентов костного мозга кумулятивная доза преднизолона в течение недели, составившая более 7 мг/кг, была ассоциирована с более высокой частотой летальных исходов: умерли 9 из 10 пациентов и только 3 из 8 больных при использовании преднизолона в дозе, равной 7 мг/кг или менее в неделю.
Клиническая картина аспергиллеза
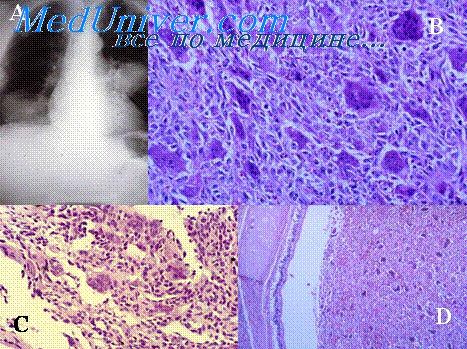
Первичным очагом при инвазивном аспергиллезе являются в основном легкие (90 %), реже придаточные пазухи носа (10—15 %), крайне редко — головной мозг. Описаны случаи инвазивного аспергиллеза кишечника в виде язв и некроза (подтверждено гистологически) у больных с гемобластозами, в основном в период нейтропении, при отсутствии поражения легких.
У больных с нейтропенией поражение легочной ткани аспергиллами протекает по типу инвазивного аспергиллеза. На первых этапах у 25—33 % больных инвазивный легочный аспергиллез протекает бессимптомно, признаки имеющейся инфекции появляются только при прогрессии микотического процесса. Наиболее частый симптом — лихорадка на фоне терапии антибиотиками широкого спектра действия. К ранним симптомам относят появление кашля, который вначале бывает сухим, в дальнейшем может быть кровохарканье; возможны появление болей в грудной клетке, одышки. Если проводят лечение глюкокортикоидами, то лихорадки может не быть, и боль в грудной клетке также может быть минимальной.
При прогрессии инвазивного процесса может развиться легочное кровотечение, при субплевральном расположении очага — спонтанный пневмоторакс.
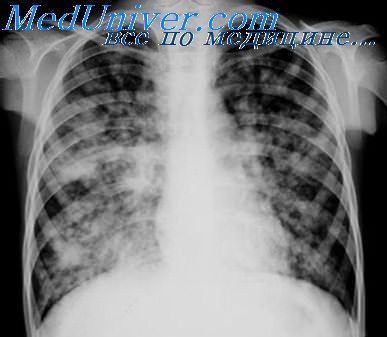
Рентгенологическая картина легких при аспергиллезе не является строго специфичной: определяются инфильтраты треугольной формы или округлые, четко очерченные, прилежащие к плевре. В начальный период болезни инфильтрация легких на рентгенограммах может не определяться практически у 70 % больных. В подобных случаях при диагностике основными являются данные компьютерной томографии: небольшие нодулярные образования, окруженные зоной просветления по периферии — «ореол» (область разрежения, представляющая собой геморрагический инфильтрат, окружающий некротизированную ткань легкого, заполненную мицелием), и/или небольшие инфильтраты треугольной формы, обращенные основанием к плевре или соединенные с плеврой. Затемнения треугольной формы появляются вследствие обтурации легочных сосудов мицелием и развития инфаркта легочной ткани.
Может быть только один очаг поражения, но чаще всего их несколько. После восстановления количества гранулоцитов выявляется другой признак, характерный для инвазивного аспергиллеза: формирование воздушной полости в виде полумесяца в нодулярных очагах — симптом «серпа» или образование центральной полости (очаги некроза легочной ткани). Обнаружение зоны просветления («ореол») около очага или симптома «серпа» относятся к признакам, высокоспецифичным для инвазивного микоза легких, которое может быть вызвано грибами не только рода Aspergillus, но и Mucorales, Trichosporon spp., Blastoschizomyces spp., Fusarium spp. Следует отметить, что столь специфичные для инвазивного аспергиллеза радиологические признаки («ореол», симптом «серпа») удается зарегистрировать только в начале заболевания, в «продвинутой» стадии эти проявления крайне неспецифичны.
Прогноз при солитарном очаге поражения более благоприятный, чем при диффузном или билатеральном вовлечении легочной ткани. Однако внезапные кровотечения, часто профузного характера, чаще возникают из отдельных, фокусных очагов.
В 10—15 % случаев аспергиллезной инвазии первичным очагом бывают придаточные пазухи носа. Первые признаки аспергиллезного риносинусита неспецифичны: повышение температуры тела, головная боль, носовое кровотечение, затем появляются ринорея, боль в области придаточных пазух носа. На слизистой оболочке нижней стенки и перегородки носовых ходов можно обнаружить изменения струпьевидного характера («корки») или изъязвления. При прогрессировании инвазивного аспергиллезного риносинусита в патологический процесс вовлекаются околоносовые пазухи, а в дальнейшем развивается деструкция области мягкого и твердого неба с распространением на лобные пазухи. Отмечаются выраженный периорбитальный отек на стороне поражения, асимметрия лица, выраженный болевой синдром. На рентгенограммах проявления аспергиллезного риносинусита варьируют от минимального утолщения слизистой оболочки до полной облитерации пазух и деструкции костной ткани.
Диагноз подтверждается выявлением Aspergillus spp. с участков изъязвления носовых ходов и из биоптатов (пункционные аспираты) придаточных пазух носа при микроскопии, культуральном и гистологическом исследованиях. Ввиду высокой вероятности диссеминации инфекции рекомендуется провести компьютерное исследование легких у больных с доказанным аспергиллезным риносинуситом даже при отсутствии клинических симптомов вовлечения легких.
Эффективность терапии зависит от хирургического дренирования очага инфекции, удаления некротизированных участков тканей на фоне проведения адекватной противогрибковой терапии и отмены иммуносупрессивной терапии. Несмотря на интенсивное, адекватно проводимое лечение, летальность при этой патологии остается крайне высокой.
Аспергиллы могут вызывать локализованное поражение дыхательных путей и приводить к развитию некротического трахеобронхита, который проявляется кашелем, кровохарканьем, лихорадкой, приступами удушья. Гипоксия возникает редко вследствие обструкции бронхов и формирования ателектазов. К редким проявлениям относится развитие псевдомембранозного трахеобронхита. Для подтверждения диагноза проводят бронхоскопию, во время которой удаляют детрит из просвета бронхов. Прогрессирование заболевания у иммунокомпрометированных больных характеризуется развитием некроза бронха, перфорацией трахеи, инвазивного аспергиллеза легких.
Гематогенная диссеминация аспергиллеза наблюдается у 30—40 % больных легочным аспергиллезом. Чаще происходит инвазия аспергиллами кожи и головного мозга. Диагностика осложнений трудна.
Наиболее часто определяемое поражение кожи аспергиллами у больных с нейтропенией — это место входа центрального венозного катетера или около него. Инвазия аспергиллами кожи может быть в виде первичного процесса, а не только как следствие гематогенной диссеминации. Отмечается некротическое повреждение кожи, сходное с проявлениями, вызванными синегнойной палочкой. Вначале появляется эритема, которая быстро увеличивается в размерах, сопровождается болью, далее цвет в центре очага изменяется от красного до пурпурного, а затем до черного. Необходимо провести посевы, гистологическое исследование биоптата.
Поражение аспергиллами головного мозга крайне редко бывает первичным, изолированным; как правило, это проявление гематогенной диссеминации. Диссеминация в головной мозг возникает у 10—20 % больных с инвазивным аспергиллезом легких и у 40—56 % репициентов костного мозга. Клинически может проявляться нарушением сознания, фокальными или генерализованными судорогами. Симптомы менингизма крайне редки. В случаях массивного поражения головного мозга симптоматика может быстро прогрессировать до развития глубокой комы. На компьютерных томограммах выявляются один или несколько гиподенсных очагов с четкими границами.
Летальность при этой патологии крайне высокая, в литературе приведены отдельные случаи излечения. При гематогенной диссеминации возможно поражение аспергиллами любого органа.
Редкими проявлениями аспергиллезной инвазии бывают эпиглоттит, поражение плевры, эндофтальмит, менингит, эндокардит, перикардит, вовлечение желудочно-кишечного тракта, печени, перитонит, тиреоидит, поражение паренхимы почки и лоханок, остеомиелит. Диагноз ставят на основании выделения Aspergillus spp. в посевах из очагов поражения или результатов гистологического исследования биоптатов. В большинстве случаев лечение этих проявлений сопряжено с рядом трудностей; прогноз неблагоприятный.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Инвазивный аспергиллез что это
Pulmonary aspergillosis: a clinical update
O.S. ZMEILI, A.O. SOUBANI
Division of Pulmonary, Allergy, Critical Care and Sleep, Wayne State University School of Medicine,Detroit, USA
Q J Med 2007; 100:317–334
Инвазивный аспергиллез легких (ИАЛ).
ИАЛ возникает преимущественно у иммуноскопрометированных пациентов. Главные факторы риска для ИАЛ (таблица 1) включают: нейтропению, пересадки гематопоэтических стволовых клеток и солидных органов, длительную и высокодозную кортикостероидную терапию, злокачественные заболевания крови, цитотоксическую терапию, развившийся СПИД и хроническая гранулематозная болезнь (ХГБ) [1,7,8].
Нейтропения, особенно абсолютная, когда количество нейтрофилов менее 500 кл/мм 3 самый важный фактор риска и ИАЛ напрямую связано с длительностью и степенью нейтропении. Риск ИАЛ у больных с нейтропенией оценивается в 1% в день в течение первых трех недель, а затем он возрастает до 4% в день [7]. Пересадки солидных органов, особенно трансплантации легких и ХГБ также являются существенным фактором риска для развития ИАЛ [9,10]. Имеются несколько факторов, которые предрасполагают к ИАЛ после проведения трансплантации: множественные иммунные дефекты, включая длительную нейтропению до пересадки стволовых клеток, применение терапии против отторжения и болезни «трансплантат против хозяина», такой как кортикостероиды и циклоспорин, парентерального питания, массивной антибактериальной терапии и длительную госпитализацию.
Нейтрофильная дисфункция, которую наблюдают при ХГБ, является следующим фактором риска для ИАЛ, и ИАЛ является существенной причиной смерти этих пациентов [21].
С другой стороны ИАЛ относительно редко встречается у больных с ВИЧ инфекцией, особенно при использовании высокоактивной антиретровирусной терапии. По недавним сообщениям частота ИАЛ у ВИЧ-инфицированных больных с выделенными из мокроты грибами Aspergillus составила 2% [22]. Почти при всех случаях аспергиллеза, связанного со СПИДом, отмечено низкое количество CD 4, обычно менее 100 кл/мм 3 и у 50% ВИЧ-инфицированных больных с ИАЛ имела место нейтропения или же они получали кортикостероиды. В результате можно сказать, что в этих случаях нет других факторов риска, нежели прогрессирующий СПИД 24. у этих пациентов в дополнение к обычной клинической картине ИАЛ имеет место большая частота случаев трахеобронхиальных поражений [26,26]. Гистопатологическое подтверждение диагноза обычно необходимо в установлении диагноза ИАЛ у больных СПИДом, так как просто выделение грибов Aspergillus из респираторных секретов является недостаточным для предположения инвазивного заболевания [27]. Такие пациенты обычно плохо отвечают на лечение [22-25,27].
Недавние сообщения представили описания случаев ИАЛ у иммунокомпетентных больных. Выделяют две группы риска: пациенты с тяжелым течением ХОБЛ и очень тяжелые больные. Из 13 случаев ИАЛ, диагностированного у больных ХОБЛ, поступивших в отделение интенсивной терапии с острым респираторным дистрессом, единственным фактором риска была кортикостероидная терапия [28]. Больные ХОБЛ имеют повышенную склонность к ИАЛ по нескольким причинам, включая структурные изменения легочной архитектуры, длительное применение кортикостероидов, частые госпитализации, антибактериальную терапию и сопутствующие заболевания, такие как сахарный диабет, алкоголизм и недоедание. Подавляющее большинство случаев, описанных в литературе, имели летальный исход 30.
Диагностика ИАЛ требует существенных усилий. Ранний диагноз ИАЛ у больных с тяжелыми иммунодефицитами труден, поэтому у больных с факторами риска инвазивных заболеваний всегда необходимо помнить о возможности развития таких процессов.
«Золотым стандартом» в диагностике ИАЛ остается гистологический диагноз, полученный при исследовании легочной ткани, полученной после торакоскопии или открытой биопсии [47]. Наличие перегородок в ветвящемся под острым углом мицелии проникающем в легочную ткань с выделением из этого патматериала культуры Aspergillus это и есть достоверная диагностика ИАЛ (рис.3). Гистологическое исследование позволяет исключить другие диагнозы, такие как злокачественные опухоли или негрибковые инфекции. Как было установлено совсем недавно, гистологические исследования при ИАЛ могут различаться в зависимости от предлежащего заболевания. У больных с аллогенной трансплантацией стволовых клеток и болезнью «трансплантат против хозяина» имело место интенсивное воспаление с нейтрофильной инфильтрацией, обширным коагуляционным некрозом, связанным с инвазией мицелия в сосуды и большим количеством грибов. В обеих этих группах одинаково интенсивно происходила диссеминация в другие органы [3].
Бронхоскопия с проведением бронхоальвеолярного лаважа (БАЛ) в большинстве случаев полезна в диагностике ИАЛ, особенно у больных с диффузными поражениями легких. Чувствительность и специфичность положительных результатов исследования промывной жидкости бронхов составляет примерно 50% и 97% соответственно. Впрочем, эти данные довольно ненадежны, поскольку имеются много данных и о значительно меньшей пользе от этих исследований [50,52,66-70]. Исследование БАЛ, тем не менее, является безопасным и полезным методом диагностики у пациентов группы высокого риска с подозрением на ИАЛ. В добавок, получение материала позволяет провести культуральное микологическое исследование, а также может быть полезным в определении антигена Aspergillus в БАЛ и исключить другие инфекции. Трахеобронхиальная биопсия в диагностике ИАЛ обычно не помогает и связана с увеличением риска кровотечения, поэтому ее производят редко [52].
Pfeiffer и соавт. провели мета-анализ исследований с оценкой эффективности теста на галактоманнан для диагностики ИАЛ. Были включены двадцать семь исследований за период с 1996 по 2005 годы и диагноз ИАЛ устанавливали согласно критериям Группы по изучению микозов Европейской организации по исследованию и лечению рака. В целом была определена чувствительность 71% и специфичность 89% для доказанных случаев инвазивного аспергиллеза. Отрицательный прогностический уровень составил 92-98% и положительный предсказательный уровень 25-62% [80]. Pfeiffer и соавторы сделали вывод, что тест на галактоманнан более полезен для диагностики у пациентов, которые имеют злокачественные заболевания крови и лиц, у перенесших аллогенную трансплантацию стволовых клеток, чем у реципиентов солидных органов или у больных без нейтропении.
Полимеразная цепная реакция (ПЦР) – другой путь диагностики ИАЛ, при котором определяют ДНК Aspergillus в бронхоальвеолярной жидкости и в сыворотке крови. Положительный тест на ДНК Aspergillus предполагает чувствительность 67-100% и специфичность 55-95% для ИАЛ [89]. Специфичность и чувствительность ПЦР была также доложена как 100% и 65-92% соответственно в образцах сыворотки крови 91. Тем не менее этот тест часто связывают с ложно-положительными результатами, поскольку он не дает различия между колонизацией и инфекцией. Определение ПЦР для нуклеиновой кислоты Aspergillus ограничено специализированными лабораториями и не может рассматриваться как рутинное исследования.
Роль определения галактоманнана и других серологических тестов в диагностике ИАЛ продолжает изучаться. Кроме того, их ценность у различных лиц в качестве контрольных тестов и значимость для определения прогноза у больных инвазивными микозами пока остается неясной. Проводимые проспективные исследования пытаются определиться с этими вопросами, однако до тех пор, пока достоверные данные не будут доступны, эти тесты должны рассматриваться как дополнительные диагностические исследования и не должны заменять клинические и рентгенологические (в отдельных случаях и инвазивные) процедуры для подтверждения диагноза ИАЛ.
Группа по изучению микозов Европейской организации по исследованию и лечению рака предложила несколько критериев для диагностики инвазивных грибковых инфекций [94]. Эти критерии включают факторы самого организма, микробиологические факторы и малые и большие клинические критерии (таблица 2). Два последовательных положительных теста на галактоманнан в сыворотке при соответствующей клинике могут рассматриваться как «вероятный» ИАЛ [94]. Тем не менее, критерии Группы по изучению микозов Европейской организации по исследованию и лечению рака не основаны на принципах доказательности и также могут быть не подтверждены в будущем. Их следует применять как руководство для клинических и эпидемиологических исследований и они не обязательно должны быть использованы у каждого больного.
Таблица 2. Диагностические критерии для ИАЛ.
Гистологическое и цитологическое исследование легочной ткани, полученное при пункционной биопсии аспирационной иглой с определением мицелия или получение биоптата с очевидным ассоциированным тканевым поражением; ИЛИ высев культуры Aspergillus из образца полученного в ходе стерильной процедуры из легких или другого места клинически и рентгенологически соответствующего инфекции.
Наличие факторов риска (таблица 1); ПЛЮС микробиологические критерии (положительная микроскопия на Aspergillus или получение культуры гриба при исследовании мокроты или бронхоальвеолярной жидкости, или положительный тест на галактоманнан); ПЛЮС клинические критерии, соответствующие инфекции (один большой или два малых критерия*).
Наличие факторов риска (см. таблицу 1) ПЛЮС микробиологические критерии (положительная микроскопия мокроты на Aspergillus или выделение культуры из мокроты или бронхоальвеолярной жидкости или положительный тест на галактоманнан); ИЛИ клинические критерии соответствующие инфекции (один большой или два малых *).
* Большой клинический критерий: новые характерные инфильтраты на КТ (симптом венчика, мениска или полость внутри участка консолидации). Малые критерии: симптомы инфекции нижних дыхательных путей (кашель, боли в грудной клетке, кровохарканье или одышка); физикальные проявления шума трения плевры; какие-либо новые инфильтраты, не соответствующие большим критериям; плевральный выпот.
Лечение ИАЛ является трудной задачей и смертность при этом заболевании остается очень высокой, несмотря не внедрение в практику нескольких новых антифунгальных препаратов. Лечение должно начинаться сразу же как только возникает клинические подозрение на наличие ИАЛ и все время пока разрабатывается последующая тактика. Многие годы препаратом первой линии для лечения ИАЛ был амфотерицин В в рекомендуемых дозах 1-1,5 мг/кг/день. Тем не менее амфотерицин В имеет серьезные побочные эффекты, включая нефротоксичность, электролитные нарушения и гиперчувствительность. В связи с этим для снижения этих побочных эффектов в практику были введены новые липид-ассоциированные формы амфотерицина В (например, липомомальный амфотерицин В и липидный комплекс амфотерицина В). Для антифунгальной эквивалетности со старой формой препарата требуется назначение более высоких дозы липидассоциированных.
В одном рандомизированном исследовании пациентов, получающих химиотерапию про поводу острого миелогенного лейкоза, назначение с целью профилактики гранулоцито- макрофаго- колониестимулирующего фактора привело к снижению частоты фатальной грибковой инфекции по сравнению с плацебо (1,9 против 19% соответственно) и снижению общей смертности [118]. Возможность назначения колоние-стимулирующих факторов рекомендуется рассматривать у больных с нейтропенией при серьезных инфекциях, однако окончательных исследований, которые бы доказывали улучшение у больных конкретно с ИАЛ, пока нет [119].
Интерферон-гамма другой цитокин, который, как показано in vitro и на экспериментальных моделях, усиливает иммунный ответ за счет увеличения активности нейтрофилов и моноцитов против Aspergillus [116,120,121] и может снижать риск аспергиллезной инфекции у больных хронической гранулематозной болезнью [122]. Однако очевидность значимости добавления интерферона-гамма в качестве дополнительной терапии ИАЛ ограничена лишь отдельными сообщениями и малым их количеством и практических руководств по их значению в лечении ИАЛ пока нет [123]. Имеются определенные опасения по поводу возможности применения интерферона-гамма у реципиентов аллогенных трансплантатов стволовых клеток, так как это может ухудшать течение болезни «трансплантат против хозяина», тем не менее, недавние испытания показали что в течение этой терапии болезнь «трансплантат против хозяина» улучшилась [124].
Лечение ИАЛ является трудной задачей и важным подходом к этой проблеме является его профилактика у пациентов с повышенным риском. Следует исключить госпитализацию пациентов в помещения, где ведутся ремонтные работы, надо использовать высоко-эффективные очистители воздуха с или без ламинарной вентиляции, поскольку доказано, что обе системы полезны [126]. Мета-анализ показал, что для предупреждения грибковых инфекций у больных с нейтропенией был эффективен итраконазол [127]. Предварительные данные также позволяют предполагать эффективность позаконазола для профилактики ИАЛ у больных с острым миелогенным лейкозом или миелодиспластическим синдромом [128]. В настоящее время в процессе разработки находятся исследования по профилактике ИАЛ у пациентов высокого риска другими противогрибковыми агентами, такими как вориконазол, каспофунгин и микафунгин.
Хронический некротический аспергиллез.
ХНА обычно встречается в среднем или пожилом возрасте с поврежденной местной защитой, связанной с предлежащими хроническими заболеваниями легких, такими как ХОБЛ, ранее перенесенный туберкулез легких, последствия оперативных вмешательств, лучевая терапия, пневмокониозы, муковисцидоз, инфаркты легкого и (менее часто) саркоидоз [132]. Он может также встречаться у пациентов с умеренными иммунодефицитами вследствие сахарного диабета, алкоголизма, хронических заболеваний печени, низкодозной терапии кортикостероидами, недоеданием и заболеваниями соединительной ткани, такими как ревматоидный артрит и анкилозирующий спондилит [130].
Бывает довольно трудно отличить ХНА от аспергиллемы, особенно если недоступны предыдущие рентгенограммы [133]. Тем не менее, при ХНА имеется локальная инвазия легочной ткани и наличие предшествующей полости вовсе не обязательно, хотя полость с грибковым комком может развиваться в легких как вторичный феномен вследствие деструкции грибами легочной ткани. В недавнем сообщении об аспергиллемах при СПИДе отмечено прогрессирование их со временем с существенной морбидностью и некоторой летальностью [133]. Это возможно отражает возможность того, что аспергиллема может инвазировать в стенку полости, вызывая локальную паренхимальную деструкцию, которую и наблюдают у пациентов с ХНА [131].
Клинические проявления и диагностика.
Пациенты часто жалуются на конституциональные симптомы, такие как лихорадка, потеря веса длительность 1-6 месяцев, недомогание, утомляемость в добавок хронический продуктивный кашель и кровохарканье, которые варьируют от легкой до сильной степени [133]. Изредка пациенты могут быть вообще не иметь никаких симптомов.
Таблица 3. Диагностические критерии ХНА
Диагностические критерии
Хроническое (более 1 месяца) легочные или системные симптомы, включая, по крайней мере одни из следующих: потеря веса, продуктивный кашель, кровохарканье.
Рентгенологические
Полостные легочные поражения с наличие паракавитарных инфильтратов. Образование новых полостей и увеличение размера полостей со временем.
Антифунгальная терапия является основой лечения больных с ХНА. Амфотерицин В применялся изначально в дозе 0,5-1 мг/кг/день (4-5 мг/кг/день для липидассоциированных форм) с благоприятными результатами [130,131]. Итраконазол появился позднее как эффективная альтернатива относительно токсичному амфотерицину В [131,137] и совсем недавно вориконазол вошел как первичная терапия ХНА. В недавнем проспективном исследовании, где вориконазол 200 мг давали два раза в день в период от 4 до 24-х недель как первичную или терапию второй линии 39 больным с ХНА [96], полный или частичный ответ наблюдали у 43% пациентов и улучшение или стабилизацию у 80%. Авторы делают заключение, что вориконазол являлся безопасным и эффективным лечением и может быть использован для первичной терапии или в качестве препарата второй линии для лечения пациентов с ХНА.
Хирургическая резекция играет незначительную роль в лечении ХНА и остается в качестве запасного варианта для в целом здоровых молодых пациентов с локальным заболеванием и хорошими легочными резервами, для пациентов, не переносящих антифунгальную терапию и для пациентов с остаточным локализованным, но активным процессом, несмотря на антифунгальную терапию. Binder и соавт. сообщили, что 90% пациентов, которые перенесли хирургическую резекцию, имели хороший ответ, однако оперативное лечение было связано со значительными послеоперационными осложнениями [130].
Сообщения о смертности от ХНА широко варьируют и может быть был ограничена неполным наблюдением в динамике [133]. Смертность была 39% у американских авторов, но менее 10% у европейских, которые использовали в лечении итраконазол [131].
Предположительно росту Aspergillus на стенке полости способствует неадекватный дренаж. Грибные комки могут перемещаться в пределах полости, но обычно не инвазируют в окружающую легочную паренхиму и кровеносные сосуды, хотя описаны и исключения [144,145]. В большинстве случаев поражение остается стабильным, но в 10% случаев аспергиллема может уменьшаться в размерах или спонтанно разрешаться без лечения [146]. Аспергиллема редко увеличивается в размерах.
Большинство больных с аспергиллемой асимптоматичны. Когда симптомы присутствуют, то большинство больных отмечают умеренное кровохарканье, хотя могут случаться и тяжелые и жизненно опасные кровохарканья, особенно при предлежащем туберкулезе [147]. Кровотечения обычно осуществляются из бронхиальных сосудов и могут быть следствием локальной инвазии в кровеносные сосуды, устилающие стенки полости, эндотоксины, выделяющиеся из грибов или механического раздражения незащищенной сосудистой сети внутри полости перемещающимся грибковым комком [144,148,149].
Смертность от кровохарканья, вызванного наличием аспергиллемы, составляет от 2 до 14% 151.
Реже у пациентов может развиваться кашель, одышка, которая вероятно связана в большей степени с предлежащими легочными заболеваниями, лихорадка, которая может быть вторичной к имеющемуся предлежащему легочному заболевания или бактериальной суперинфекцией в полости.
Имеются некоторые факторы риска, которые определяют плохой прогноз аспергиллемы. Они включают тяжесть предлежащего заболевания, нарастание размеров или количества поражений как это видно на рентгенограмме легких, иммуносупрессию (включая кортикостероиды), нарастание специфических к Aspergillus титров IgG антител, рецидивирующие кровохарканья большого объема, наличие предлежащего саркоидоза и ВИЧ-инфекцию [155].
Какой-либо консенсус по лечению аспергиллемы отсутствует. Лечение рассматривается только тогда, когда пациенты имеют симптомы, особенно кровохарканье. Ингаляционные, внутриполостные и интрабронхиальные инстилляции антифунгальных агентов были использованы и описаны в малом количестве больных и без стойкого эффекта [153,163,164].
При аспергиллеме особенно у пациентов с массивным кровохарканьем может быть эффективным введение амфотерицина В чрезкожно под контролем КТ, что дает прекращение кровохарканья в течение нескольких дней [165,166]. Значение внутривенного введения амфотерицина В не определено, однако в небольшом количестве исследований эта методика не дало никакого улучшения [167].
Хирургическая резекция полости и удаление грибного комка обычно показано у больных с повторными кровохарканьями, если легочная функция достаточна для проведения операции. Хирургическое лечение связано с относительно высокой смертностью на уровне от 7 до 23% [149-151,172-175]. Наиболее частые причины смерти в послеоперационном периоде это тяжелые предлежащие заболевания, пневмония, острый инфаркт миокарда и ИАЛ [153, 175]. Другие послеоперационные осложнения, включают кровотечения, остаточные плевральные полости, бронхоальвеолярные фистулы, эмпиему и респираторные нарушения.
Бронхиальная артериальная эмболизация должна быть рассмотрена лишь как временная мера у больных с жизненно-опасными кровохарканьями, так как кровохарканье из-за наличия массивных коллатеральных кровеносных сосудов обычно рецидивирует [176]. Роль новейших антифунгальных азолов, таких как вориконазол в лечении аспергиллемы все еще определяется.
Аллергический бронхолегочный аспергиллез (АБЛА).
Клинические проявления и диагностика.
Таблица 4. Диагностические критерии АБЛА
Уровень общего IgE более 1000 нг/мл
Наличие в настоящее время или ранее инфильтратов в легких.
Центальные бронхоэктазы.
Периферическая эозинофилия крови (1000 кл/мкл).
1. Soubani AO, Chandrasekar PH. The clinical spectrum of pulmonary aspergillosis. Chest 2002; 121:1988–99.
2. Rankin NE. Disseminated aspergillosis and moniliasis associated with agranulocytosis and antibiotic therapy. Br Med J 1953; 1:918–19.
3. Chamilos G, Luna M, Lewis RE, et al. Invasive fungal infections in patients with hematologic malignancies in a tertiary care cancer center: an autopsy study over a 15-year period (1989–2003). Haematologica 2006; 91:986–9.
4. Groll AH, Shah PM, Mentzel C, Schneider M, Just- Nuebling G, Huebner K. Trends in the postmortem epidemiology of invasive fungal infections at a university hospital. J Infect 1996; 33:23–32.
5. Yeghen T, Kibbler CC, Prentice HG, et al. Management of invasive pulmonary aspergillosis in hematology patients: a review of 87 consecutive cases at a single institution. Clin Infect Dis 2000; 31:859–68.
6. Fukuda T, Boeckh M, Carter RA, et al. Risks and outcomes of invasive fungal infections in recipients of allogeneic hematopoietic stem cell transplants after nonmyeloablative conditioning. Blood 2003; 102:827–33.
7. Gerson SL, Talbot GH, Hurwitz S, Strom BL, Lusk EJ, Cassileth PA. Prolonged granulocytopenia: the major risk factor for invasive pulmonary aspergillosis in patients with acute leukemia. Ann Intern Med 1984; 100:345–51.
8. Segal BH, Walsh TJ. Current approaches to diagnosis and treatment of invasive aspergillosis. Am J Respir Crit Care Med 2006; 173:707–17.
9. Soubani AO, Miller KB, Hassoun PM. Pulmonary complications of bone marrow transplantation. Chest 1996; 109:1066–77.
10. Kotloff RM, Ahya VN, Crawford SW. Pulmonary complications of solid organ and hematopoietic stem cell transplantation. Am J Respir Crit Care Med 2004; 170:22–48.
11. Morgan J, Wannemuehler KA, Marr KA, et al. Incidence of invasive aspergillosis following hematopoietic stem cell and solid organ transplantation: interim results of a prospective multicenter surveillance program. Med Mycol 2005; 43(Suppl. 1):S49–58.
12. Wald A, Leisenring W, van Burik JA, Bowden RA. Epidemiology of Aspergillus infections in a large cohort of patients undergoing bone marrow transplantation. J Infect Dis 1997; 175:1459–66.
13. Marr KA, Carter RA, Boeckh M, Martin P, Corey L. Invasive aspergillosis in allogeneic stem cell transplant recipients: changes in epidemiology and risk factors. Blood 2002; 100:4358–66.
14. Marr KA, Carter RA, Crippa F, Wald A, Corey L. Epidemiology and outcome of mould infections in hematopoietic stem cell transplant recipients. Clin Infect Dis 2002; 34:909–17.
15. Baddley JW, Stroud TP, Salzman D, Pappas PG. Invasive mold infections in allogeneic bone marrow transplant recipients. Clin Infect Dis 2001; 32:1319–24.
16. Junghanss C, Marr KA, Carter RA, et al. Incidence and outcome of bacterial and fungal infections following nonmyeloablative compared with myeloablative allogeneic hematopoietic stem cell transplantation: a matched control study. Biol Blood Marrow Transplant 2002; 8:512–20.
17. Warris A, Bjorneklett A, Gaustad P. Invasive pulmonary aspergillosis associated with infliximab therapy. N Engl J Med 2001; 344:1099–100.
18. Cordonnier C, Ribaud P, Herbrecht R, et al. Prognostic factors for death due to invasive aspergillosis after hematopoietic stem cell transplantation: a 1-year retrospective study of consecutive patients at French transplantation centers. Clin Infect Dis 2006; 42:955–63.
19. Ribaud P, Chastang C, Latge JP, et al. Survival and prognostic factors of invasive aspergillosis after allogeneic bone marrow transplantation. Clin Infect Dis 1999; 28:322–30.
20. Nichols WG, Corey L, Gooley T, Davis C, Boeckh M. High risk of death due to bacterial and fungal infection among cytomegalovirus (CMV)-seronegative recipients of stem cell transplants from seropositive donors: evidence for indirect effects of primary CMV infection. J Infect Dis 2002; 185:273–82.
21. Segal BH, Barnhart LA, Anderson VL, Walsh TJ, Malech HL, Holland SM. Posaconazole as salvage therapy in patients with chronic granulomatous disease and invasive filamentous fungal infection. Clin Infect Dis 2005; 40:1684–8.
22. Libanore M, Prini E, Mazzetti M, et al. Invasive Aspergillosis in Italian AIDS patients. Infection 2002; 30:341–5.
23. Denning DW, Follansbee SE, Scolaro M, Norris S, Edelstein H, Stevens DA. Pulmonary aspergillosis in the acquired immunodeficiency syndrome. N Engl J Med 1991; 324:654–62.
24. Lortholary O, Meyohas MC, Dupont B, et al. Invasive aspergillosis in patients with acquired immunodeficiency syndrome: report of 33 cases. French Cooperative Study Group on Aspergillosis in AIDS. Am J Med 1993; 95:177–87.
25. Mylonakis E, Barlam TF, Flanigan T, Rich JD. Pulmonary aspergillosis and invasive disease in AIDS: review of 342 cases. Chest 1998; 114:251–62.
26. Kemper CA, Hostetler JS, Follansbee SE, et al. Ulcerative and plaque-like tracheobronchitis due to infection with Aspergillus in patients with AIDS. Clin Infect Dis 1993; 17:344–52.
27. Wallace JM, Lim R, Browdy BL, et al. Risk factors and outcomes associated with identification of Aspergillus in respiratory specimens from persons with HIV disease. Pulmonary Complications of HIV Infection Study Group. Chest 1998; 114:131–7.
28. Ader F, Nseir S, Le Berre R, et al. Invasive pulmonary aspergillosis in chronic obstructive pulmonary disease: an emerging fungal pathogen. Clin Microbiol Infect 2005; 11:427–9.
29. Carrascosa Porras M, Herreras Martinez R, Corral Mones J, Ares Ares M, Zabaleta Murguiondo M, Ruchel R. Fatal Aspergillus myocarditis following short-term corticosteroid therapy for chronic obstructive pulmonary disease. Scand J Infect Dis 2002; 34:224–7.
30. Bulpa PA, Dive AM, Garrino MG, et al. Chronic obstructive pulmonary disease patients with invasive pulmonary aspergillosis: benefits of intensive care? Intensive Care Med 2001; 27:59–67.
Pulmonary aspergillosis 329
31. Vandewoude KH, Blot SI, Depuydt P, et al. Clinical relevance of Aspergillus isolation from respiratory tract samples in critically ill patients. Crit Care 2006; 10:R31.
32. Dimopoulos G, Piagnerelli M, Berre J, Eddafali B, Salmon I, Vincent JL. Disseminated aspergillosis in intensive care unit patients: an autopsy study. J Chemother 2003; 15:71–5.
33. Vandewoude KH, Blot SI, Benoit D, Colardyn F, Vogelaers D. Invasive aspergillosis in critically ill patients: attributable mortality and excesses in length of ICU stay and ventilator dependence. J Hosp Infect 2004; 56:269–76.
34. Meersseman W, Vandecasteele SJ, Wilmer A, Verbeken E, Peetermans WE, Van Wijngaerden E. Invasive aspergillosis in critically ill patients without malignancy. Am J Respir Crit Care Med 2004; 170:621–5.
35. Janssen JJ, Strack van Schijndel RJ, van der Poest Clement EH, Ossenkoppele GJ, Thijs LG, Huijgens PC. Outcome of ICU treatment in invasive aspergillosis. Intensive Care Med 1996; 22:1315–22.
36. Garnacho-Montero J, Amaya-Villar R, Ortiz-Leyba C, et al. Isolation of Aspergillus spp. from the respiratory tract in critically ill patients: risk factors, clinical presentation and outcome. Crit Care 2005; 9:R191–9.
37. Garnacho-Montero J, Amaya-Villar R. A validated clinical approach for the management of aspergillosis in critically ill patients: ready, steady, go! Crit Care 2006; 10:132.
38. Khasawneh F, Mohamad T, Moughrabieh MK, Lai Z, Ager J, Soubani AO. Isolation of Aspergillus in critically ill patients: a potential marker of poor outcome. J Crit Care 2006; 21:322–7.
39. Iwen PC, Rupp ME, Langnas AN, Reed EC, Hinrichs SH. Invasive pulmonary aspergillosis due to Aspergillus terreus: 12-year experience and review of the literature. Clin Infect Dis 1998; 26:1092–7.
40. Young RC, Bennett JE, Vogel CL, Carbone PP, DeVita VT. Aspergillosis. The spectrum of the disease in 98 patients. Medicine (Baltimore) 1970; 49:147–73.
41. Prystowsky SD, Vogelstein B, Ettinger DS, et al. Invasive aspergillosis. N Engl J Med 1976; 295:655–8.
42. Allo MD, Miller J, Townsend T, Tan C. Primary cutaneous aspergillosis associated with Hickman intravenous catheters. N Engl J Med 1987; 317:1105–8.
43. Albelda SM, Talbot GH, Gerson SL, Miller WT, Cassileth PA. Pulmonary cavitation and massive hemoptysis in invasive pulmonary aspergillosis. Influence of bone marrow recovery in patients with acute leukemia. Am Rev Respir Dis 1985; 131:115–20.
44. Judson MA, Sahn SA. Endobronchial lesions in HIV-infected individuals. Chest 1994; 105:1314–23.
45. Nathan SD, Shorr AF, Schmidt ME, Burton NA. Aspergillus and endobronchial abnormalities in lung transplant recipients. Chest 2000; 118:403–7.
46. Denning DW. Invasive aspergillosis. Clin Infect Dis 1998; 26:781–803.
47. Ruhnke M, Bohme A, Buchheidt D, et al. Diagnosis of invasive fungal infections in hematology and oncology– guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol 2003; 82(Suppl. 2):S141–8.
48. Soubani AO, Khanchandani G, Ahmed HP. Clinical significance of lower respiratory tract Aspergillus culture in elderly hospitalized patients. Eur J Clin Microbiol Infect Dis 2004; 23:491–4.
49. Nalesnik MA, Myerowitz RL, Jenkins R, Lenkey J, Herbert D. Significance of Aspergillus species isolated from respiratory secretions in the diagnosis of invasive pulmonary aspergillosis. J Clin Microbiol 1980; 11:370–6.
50. Horvath JA, Dummer S. The use of respiratory-tract cultures in the diagnosis of invasive pulmonary aspergillosis. Am J Med 1996; 100:171–8.
51. Treger TR, Visscher DW, Bartlett MS, Smith JW. Diagnosis of pulmonary infection caused by Aspergillus: usefulness of respiratory cultures. J Infect Dis 1985; 152:572–6.
52. Soubani AO, Qureshi MA. Invasive pulmonary aspergillosis following bone marrow transplantation: risk factors and diagnostic aspect. Haematologia 2002; 32:427–37.
53. Yu VL, Muder RR, Poorsattar A. Significance of isolation of Aspergillus from the respiratory tract in diagnosis of invasive pulmonary aspergillosis. Results from a three-year prospective study. Am J Med 1986; 81:249–54.
54. Tang CM, Cohen J. Diagnosing fungal infections in immunocompromised hosts. J Clin Pathol 1992; 45:1–5.
55. Duthie R, Denning DW. Aspergillus fungemia: report of two cases and review. Clin Infect Dis 1995; 20:598–605.
56. Libshitz HI, Pagani JJ. Aspergillosis and mucormycosis: two types of opportunistic fungal pneumonia. Radiology 1981; 140:301–6.
57. Kuhlman JE, Fishman EK, Siegelman SS. Invasive pulmonary aspergillosis in acute leukemia: characteristic findings on CT, the CT halo sign, and the role of CT in early diagnosis. Radiology 1985; 157:611–14.
58. Caillot D, Casasnovas O, Bernard A, et al. Improved management of invasive pulmonary aspergillosis in neutropenic patients using early thoracic computed tomographic scan and surgery. J Clin Oncol 1997; 15:139–47.
59. Caillot D, Mannone L, Cuisenier B, Couaillier JF. Role of early diagnosis and aggressive surgery in the management of invasive pulmonary aspergillosis in neutropenic patients. Clin Microbiol Infect 2001; 7(Suppl. 2):54–61.
60. Kuhlman JE, Fishman EK, Burch PA, Karp JE, Zerhouni EA, Siegelman SS. Invasive pulmonary aspergillosis in acute leukemia. The contribution of CT to early diagnosis and aggressive management. Chest 1987; 92:95–9.
61. Curtis AM, Smith GJ, Ravin CE. Air crescent sign of invasive aspergillosis. Radiology 1979; 133:17–21.
62. Gaeta M, Blandino A, Scribano E, Minutoli F, Volta S, Pandolfo I. Computed tomography halo sign in pulmonary nodules: frequency and diagnostic value. J Thorac Imaging 1999; 14:109–13.
63. Greene R. The radiological spectrum of pulmonary aspergillosis. Med Mycol 2005; 43(Suppl. 1):S147–54.
64. Heussel CP, Kauczor HU, Heussel GE, et al. Pneumonia in febrile neutropenic patients and in bone marrow and blood stem-cell transplant recipients: use of high-resolution computed tomography. J Clin Oncol 1999; 17:796–805.
65. Horger M, Hebart H, Einsele H, et al. Initial CT manifestations of invasive pulmonary aspergillosis in 45 non-HIV immunocompromised patients: association with patient outcome? Eur J Radiol 2005; 55:437–44.
66. Albelda SM, Talbot GH, Gerson SL, Miller WT, Cassileth PA. Role of fiberoptic bronchoscopy in the diagnosis of invasive pulmonary aspergillosis in patients with acute leukemia. Am J Med 1984; 76:1027–34.
67. Kahn FW, Jones JM, England DM. The role of bronchoalveolar lavage in the diagnosis of invasive pulmonary aspergillosis. Am J Clin Pathol 1986; 86:518–23.
68. Levy H, Horak DA, Tegtmeier BR, Yokota SB, Forman SJ. The value of bronchoalveolar lavage and bronchial washings in the diagnosis of invasive pulmonary aspergillosis. Respir Med 1992; 86:243–8.
69. Reichenberger F, Habicht J, Matt P, et al. Diagnostic yield of bronchoscopy in histologically proven invasive pulmonary aspergillosis. Bone Marrow Transplant 1999; 24:1195–9.
70. Maschmeyer G, Beinert T, Buchheidt D, et al. Diagnosis and antimicrobial therapy of pulmonary infiltrates in febrile neutropenic patients–guidelines of the Infectious Diseases Working Party (AGIHO) of the German Society of Hematology and Oncology (DGHO). Ann Hematol 2003;
71. Panackal AA, Marr KA. Scedosporium/Pseudallescheria infections. Semin Respir Crit Care Med 2004; 25:171–81.
72. Walsh TJ, Groll AH. Overview: non-fumigatus species of Aspergillus: perspectives on emerging pathogens in immunocompromised hosts. Curr Opin Investig Drugs 2001; 2:1366–7.
73. Lass-Florl C, Griff K, Mayr A, et al. Epidemiology and outcome of infections due to Aspergillus terreus: 10-year single centre experience. Br J Haematol 2005; 131:201–7.
74. Steinbach WJ, Benjamin DK, Jr., Kontoyiannis DP, et al. Infections due to Aspergillus terreus: a multicenter retrospective analysis of 83 cases. Clin Infect Dis 2004; 39:192–8.
75. Hachem RY, Kontoyiannis DP, Boktour MR, et al. Aspergillus terreus: an emerging amphotericin B-resistant opportunistic mold in patients with hematologic malignancies. Cancer 2004; 101:1594–600.
76. Kontoyiannis DP, Lewis RE, May GS, Osherov N, Rinaldi MG. Aspergillus nidulans is frequently resistant to amphotericin B. Mycoses 2002; 45:406–7.
77. Walsh TJ, Raad I, Patterson TF, et al. Treatment of invasive aspergillosis with posaconazole in patients who are refractory to or intolerant of conventional therapy: an externally controlled trial. Clin Infect Dis 2007; 44:2–12.
78. Boutboul F, Alberti C, Leblanc T, et al. Invasive aspergillosis in allogeneic stem cell transplant recipients: increasing antigenemia is associated with progressive disease. Clin Infect Dis 2002; 34:939–43.
79. Marr KA, Balajee SA, McLaughlin L, Tabouret M, Bentsen C, Walsh TJ. Detection of galactomannan antigenemia by enzyme immunoassay for the diagnosis of invasive aspergillosis: variables that affect performance. J Infect Dis 2004; 190:641–9.
80. Pfeiffer CD, Fine JP, Safdar N. Diagnosis of invasive aspergillosis using a galactomannan assay: a meta-analysis. Clin Infect Dis 2006; 42:1417–27.
81. Herbrecht R, Letscher-Bru V, Oprea C, et al. Aspergillus galactomannan detection in the diagnosis of invasive aspergillosis in cancer patients. J Clin Oncol 2002; 20:1898–906.
82. Singh N, Obman A, Husain S, Aspinall S, Mietzner S, Stout JE. Reactivity of platelia Aspergillus galactomannan antigen with piperacillin-tazobactam: clinical implications based on achievable concentrations in serum. Antimicrob Agents Chemother 2004; 48:1989–92.
83. Marr KA, Laverdiere M, Gugel A, Leisenring W. Antifungal therapy decreases sensitivity of the Aspergillus galactomannan enzyme immunoassay. Clin Infect Dis 2005; 40:1762–9.
84. Ansorg R, van den Boom R, Rath PM. Detection of Aspergillus galactomannan antigen in foods and antibiotics. Mycoses 1997; 40:353–7.
85. Busca A, Locatelli F, Barbui A, et al. Usefulness of sequential Aspergillus galactomannan antigen detection combined with early radiologic evaluation for diagnosis of invasive pulmonary aspergillosis in patients undergoing allogeneic stem cell transplantation. Transplant Proc 2006; 38:1610–13.
86. Musher B, Fredricks D, Leisenring W, Balajee SA, Smith C, Marr KA. Aspergillus galactomannan enzyme immunoassay and quantitative PCR for diagnosis of invasive aspergillosis with bronchoalveolar lavage fluid. J Clin Microbiol 2004; 42:5517–22.
87. Klont RR, Mennink-Kersten MA, Verweij PE. Utility of Aspergillus antigen detection in specimens other than serum specimens. Clin Infect Dis 2004; 39:1467–74.
88. Salonen J, Lehtonen OP, Terasjarvi MR, Nikoskelainen J. Aspergillus antigen in serum, urine and bronchoalveolar lavage specimens of neutropenic patients in relation to clinical outcome. Scand J Infect Dis 2000; 32:485–90.
89. Hizel K, Kokturk N, Kalkanci A, Ozturk C, Kustimur S, Tufan M. Polymerase chain reaction in the diagnosis of invasive aspergillosis. Mycoses 2004; 47:338–42.
90. Buchheidt D, Baust C, Skladny H, et al. Detection of Aspergillus species in blood and bronchoalveolar lavage samples from immunocompromised patients by means of 2-step polymerase chain reaction: clinical results. Clin Infect Dis 2001; 33:428–35.
91. Loeffler J, Kloepfer K, Hebart H, et al. Polymerase chain reaction detection of aspergillus DNA in experimental models of invasive aspergillosis. J Infect Dis 2002; 185:1203–6.
92. Halliday C, Hoile R, Sorrell T, et al. Role of prospective screening of blood for invasive aspergillosis by polymerase chain reaction in febrile neutropenic recipients of haematopoietic stem cell transplants and patients with acute leukaemia. Br J Haematol 2006; 132:478–86.
93. Obayashi T, Yoshida M, Mori T, et al. Plasma (1–43)-beta- D-glucan measurement in diagnosis of invasive deep mycosis and fungal febrile episodes. Lancet 1995; 345:17–20.
94. Ascioglu S, Rex JH, de Pauw B, et al. Defining opportunistic invasive fungal infections in immunocompromised patients with cancer and hematopoietic stem cell transplants: an international consensus. Clin Infect Dis 2002; 34:7–14.
95. Johnson LB, Kauffman CA. Voriconazole: a new triazole antifungal agent. Clin Infect Dis 2003; 36:630–7.
96. Sambatakou H, Dupont B, Lode H, Denning DW. Voriconazole treatment for subacute invasive and chronic pulmonary aspergillosis. Am J Med 2006; 119:527.e17–24.
97. Ghannoum MA, Kuhn DM. Voriconazole – better chances for patients with invasive mycoses. Eur J Med Res 2002; 7:242–56.
98. Herbrecht R, Denning DW, Patterson TF, et al. Voriconazole versus amphotericin B for primary therapy of invasive aspergillosis. N Engl J Med 2002; 347:408–15.
99. Pitisuttithum P, Negroni R, Graybill JR, et al. Activity of posaconazole in the treatment of central nervous system fungal infections. J Antimicrob Chemother 2005; 56:745–55.
100. Spanakis EK, Aperis G, Mylonakis E. New agents for the treatment of fungal infections: clinical efficacy and gaps in coverage. Clin Infect Dis 2006; 43:1060–8.
101. Cohen-Wolkowiez M, Benjamin DK, Jr., Steinbach WJ, Smith PB. Anidulafungin: a new echinocandin for the treatment of fungal infections. Drugs Today (Barc) 2006; 42:533–44.
102. Aliff TB, Maslak PG, Jurcic JG, et al. Refractory Aspergillus pneumonia in patients with acute leukemia: successful therapy with combination caspofungin and liposomal amphotericin. Cancer 2003; 97:1025–32.
103. Kontoyiannis DP, Hachem R, Lewis RE, et al. Efficacy and toxicity of caspofungin in combination with liposomal amphotericin B as primary or salvage treatment of invasive aspergillosis in patients with hematologic malignancies. Cancer 2003; 98:292–9.
104. Graybill JR, Bocanegra R, Gonzalez GM, Najvar LK. Combination antifungal therapy of murine aspergillosis: liposomal amphotericin B and micafungin. J Antimicrob Chemother 2003; 52:656–62.
105. Marr KA, Boeckh M, Carter RA, Kim HW, Corey L. Combination antifungal therapy for invasive aspergillosis. Clin Infect Dis 2004; 39:797–802.
106. Perea S, Gonzalez G, Fothergill AW, Kirkpatrick WR, Rinaldi MG, Patterson TF. In vitro interaction of caspofungin acetate with voriconazole against clinical isolates of Aspergillus spp. Antimicrob Agents Chemother 2002; 46:3039–41.
107. Denning DW, Marr KA, Lau WM, et al. Micafungin (FK463), alone or in combination with other systemic antifungal agents, for the treatment of acute invasive aspergillosis. J Infect 2006; 53:337–49.
108. Klont RR, Mennink-Kersten MA, Ruegebrink D, et al. Paradoxical increase in circulating Aspergillus antigen during treatment with caspofungin in a patient with pulmonary aspergillosis. Clin Infect Dis 2006; 43:e23–5.
109. Moreau P, Zahar JR, Milpied N, et al. Localized invasive pulmonary aspergillosis in patients with neutropenia. Effectiveness of surgical resection. Cancer 1993; 72:3223–6.
110. Reichenberger F, Habicht J, Kaim A, et al. Lung resection for invasive pulmonary aspergillosis in neutropenic patients with hematologic diseases. Am J Respir Crit Care Med 1998; 158:885–90.
111. Habicht JM, Reichenberger F, Gratwohl A, Zerkowski HR, Tamm M. Surgical aspects of resection for suspected invasive pulmonary fungal infection in neutropenic patients. Ann Thorac Surg 1999; 68:321–5.
112. Pidhorecky I, Urschel J, Anderson T. Resection of invasive pulmonary aspergillosis in immunocompromised patients. Ann Surg Oncol 2000; 7:312–17.
113. Matt P, Bernet F, Habicht J, et al. Predicting outcome after lung resection for invasive pulmonary aspergillosis in patients with neutropenia. Chest 2004; 126:1783–8.
114. Baron O, Guillaume B, Moreau P, et al. Aggressive surgical management in localized pulmonary mycotic and nonmycotic infections for neutropenic patients with acute leukemia: report of eighteen cases. J Thorac Cardiovasc Surg 1998; 115:63–8.
115. Giles FJ. Monocyte-macrophages, granulocyte-macrophagecolony-stimulating factor, and prolonged survival among patients with acute myeloid leukemia and stem cell transplants. Clin Infect Dis 1998; 26:1282–9.
116. Roilides E, Holmes A, Blake C, Venzon D, Pizzo PA, Walsh TJ. Antifungal activity of elutriated human monocytes against Aspergillus fumigatus hyphae: enhancement by granulocyte-macrophage colony-stimulating factor and interferon-gamma. J Infect Dis 1994; 170:894–9.
117. Roilides E, Sein T, Holmes A, et al. Effects of macrophage colony-stimulating factor on antifungal activity of mononuclear phagocytes against Aspergillus fumigatus. J Infect Dis 1995; 172:1028–34.
118. Rowe JM, Andersen JW, Mazza JJ, et al. A randomized placebo-controlled phase III study of granulocyte-macrophage colony-stimulating factor in adult patients (455 to 70 years of age) with acute myelogenous leukemia: a study of the Eastern Cooperative Oncology Group (E1490). Blood
119. Ozer H, Armitage JO, Bennett CL, et al. 2000 update of recommendations for the use of hematopoietic colonystimulating factors: evidence-based, clinical practice guidelines. American Society of Clinical Oncology Growth Factors Expert Panel. J Clin Oncol 2000; 18:3558–85.
120. Roilides E, Uhlig K, Venzon D, Pizzo PA, Walsh TJ. Prevention of corticosteroid-induced suppression of human polymorphonuclear leukocyte-induced damage of Aspergillus fumigatus hyphae by granulocyte colonystimulating factor and gamma interferon. Infect Immun 1993; 61:4870–7.
121. Nagai H, Guo J, Choi H, Kurup V. Interferon-gamma and tumor necrosis factor-alpha protect mice from invasive aspergillosis. J Infect Dis 1995; 172:1554–60.
122. A controlled trial of interferon gamma to prevent infection in chronic granulomatous disease. The International Chronic Granulomatous Disease Cooperative Study Group. N Engl J Med 1991; 324:509–16.
123. Safdar A. Strategies to enhance immune function in hematopoietic transplantation recipients who have fungal infections. Bone Marrow Transplant 2006; 38:327–37.
124. Safdar A, Rodriguez G, Ohmagari N, et al. The safety of interferon-gamma-1b therapy for invasive fungal infections after hematopoietic stem cell transplantation. Cancer 2005; 103:731–9.
125. Price TH, Bowden RA, Boeckh M, et al. Phase I/II trial of neutrophil transfusions from donors stimulated with G-CSF and dexamethasone for treatment of patients with infections in hematopoietic stem cell transplantation. Blood 2000; 95:3302–9.
126. Sherertz RJ, Belani A, Kramer BS, et al. Impact of air filtration on nosocomial Aspergillus infections. Unique risk of bone marrow transplant recipients. Am J Med 1987; 83:709–18.
127. Mattiuzzi GN, Kantarjian H, O’Brien S, et al. Intravenous itraconazole for prophylaxis of systemic fungal infections in patients with acute myelogenous leukemia and high-risk myelodysplastic syndrome undergoing induction chemotherapy. Cancer 2004; 100:568–73.
128. Ullmann AJ, Cornely OA. Antifungal prophylaxis for invasive mycoses in high risk patients. Curr Opin Infect Dis 2006; 19:571–6.
129. Gefter WB, Weingrad TR, Epstein DM, Ochs RH, Miller WT. “Semi-invasive” pulmonary aspergillosis: a new look at the spectrum of aspergillus infections of the lung. Radiology 1981; 140:313–21.
130. Binder RE, Faling LJ, Pugatch RD, Mahasaen C, Snider GL. Chronic necrotizing pulmonary aspergillosis: a discrete clinical entity. Medicine (Baltimore) 1982; 61:109–24.
131. Saraceno JL, Phelps DT, Ferro TJ, Futerfas R, Schwartz DB. Chronic necrotizing pulmonary aspergillosis: approach to management. Chest 1997; 112:541–8.
132. Grahame-Clarke CN, Roberts CM, Empey DW. Chronic necrotizing pulmonary aspergillosis and pulmonary phycomycosis in cystic fibrosis. Respir Med 1994; 88:465–8.
133. Denning DW. Chronic forms of pulmonary aspergillosis. Clin Microbiol Infect 2001; 7(Suppl. 2):25–31.
134. Kim SY, Lee KS, Han J, et al. Semiinvasive pulmonary aspergillosis: CT and pathologic findings in six patients. AJR Am J Roentgenol 2000; 174:795–8.
135. Parra I, Remacha A, Rezusta A, et al. Chronic necrotizing pulmonary aspergillosis. Med Mycol 2004; 42:369–71.
136. Denning DW, Riniotis K, Dobrashian R, Sambatakou H. Chronic cavitary and fibrosing pulmonary and pleural aspergillosis: case series, proposed nomenclature change, and review. Clin Infect Dis 2003; 37(Suppl. 3):S265–80.
137. Caras WE, Pluss JL. Chronic necrotizing pulmonary aspergillosis: pathologic outcome after itraconazole therapy. Mayo Clin Proc 1996; 71:25–30.
138. Kauffman CA. Quandary about treatment of aspergillomas persists. Lancet 1996; 347:1640.
139. Zizzo G, Castriota-Scanderbeg A, Zarrelli N, Nardella G, Daly J, Cammisa M. Pulmonary aspergillosis complicating ankylosing spondylitis. Radiol Med 1996; 91:817–8.
140. Kawamura S, Maesaki S, Tomono K, Tashiro T, Kohno S. Clinical evaluation of 61 patients with pulmonary aspergilloma. Intern Med 2000; 39:209–12.
141. Aspergilloma and residual tuberculous cavities–the results of a resurvey. Tubercle 1970; 51:227–45.
142. Rosenheim SH, Schwarz J. Cavitary pulmonary cryptococcosis complicated by aspergilloma. Am Rev Respir Dis 1975; 111:549–53.
143. Sarosi GA, Silberfarb PM, Saliba NA, Huggin PM, Tosh FE. Aspergillomas occurring in blastomycotic cavities. Am Rev Respir Dis 1971; 104:581–4.
144. Tomee JF, van der Werf TS, Latge JP, Koeter GH, Dubois AE, Kauffman HF. Serologic monitoring of disease and treatment in a patient with pulmonary aspergilloma. Am J Respir Crit Care Med 1995; 151:199–204.
145. Rafferty P, Biggs BA, Crompton GK, Grant IW. What happens to patients with pulmonary aspergilloma? Analysis of 23 cases. Thorax 1983; 38:579–83.
146. Gefter WB. The spectrum of pulmonary aspergillosis. J Thorac Imaging 1992; 7:56–74.
147. Faulkner SL, Vernon R, Brown PP, Fisher RD, Bender HW, Jr. Hemoptysis and pulmonary aspergilloma: operative versus nonoperative treatment. Ann Thorac Surg 1978; 25:389–92.
148. Addrizzo-Harris DJ, Harkin TJ, McGuinness G, Naidich DP, Rom WN. Pulmonary aspergilloma and AIDS. A comparison of HIV-infected and HIV-negative individuals. Chest 1997; 111:612–18.
149. Aslam PA, Eastridge CE, Hughes FA Jr. Aspergillosis of the lung–an eighteen-year experience. Chest 1971;
150. Garvey J, Crastnopol P, Weisz D, Khan F. The surgical treatment of pulmonary aspergillomas. J Thorac Cardiovasc Surg 1977; 74:542–7.
151. Daly RC, Pairolero PC, Piehler JM, Trastek VF, Payne WS, Bernatz PE. Pulmonary aspergilloma. Results of surgical treatment. J Thorac Cardiovasc Surg 1986; 92:981–8.
152. Karas A, Hankins JR, Attar S, Miller JE, McLaughlin JS. Pulmonary aspergillosis: an analysis of 41 patients. Ann Thorac Surg 1976; 22:1–7.
153. Jewkes J, Kay PH, Paneth M, Citron KM. Pulmonary aspergilloma: analysis of prognosis in relation to haemoptysis and survey of treatment. Thorax 1983; 38:572–8.
154. Glimp RA, Bayer AS. Pulmonary aspergilloma. Diagnostic and therapeutic considerations. Arch Intern Med 1983; 143:303–8.
155. Stevens DA, Kan VL, Judson MA, et al. Practice guidelines for diseases caused by Aspergillus. Infectious Diseases Society of America. Clin Infect Dis 2000; 30:696–709.
156. Tuncel E. Pulmonary air meniscus sign. Respiration 1984; 46:139–44.
157. Roberts CM, Citron KM, Strickland B. Intrathoracic aspergilloma: role of CT in diagnosis and treatment. Radiology 1987; 165:123–8.
158. Bandoh S, Fujita J, Fukunaga Y, et al. Cavitary lung cancer with an aspergilloma-like shadow. Lung Cancer 1999; 26:195–8.
159. Le Thi Huong D, Wechsler B, Chamuzeau JP, Bisson A, Godeau P. Pulmonary aspergilloma complicating Wegener’s granulomatosis. Scand J Rheumatol 1995; 24:260.
160. McCarthy DS, Pepys J. Pulmonary aspergilloma–clinical immunology. Clin Allergy 1973; 3:57–70.
161. Judson MA. Noninvasive Aspergillus pulmonary disease. Semin Respir Crit Care Med 2004; 25:203–19.
162. Andrews CP, Weiner MH. Aspergillus antigen detection in bronchoalveolar lavage fluid from patients with invasive aspergillosis and aspergillomas. Am J Med 1982; 73:372–80.
163. Yamada H, Kohno S, Koga H, Maesaki S, Kaku M. Topical treatment of pulmonary aspergilloma by antifungals. Relationship between duration of the disease and efficacy of therapy. Chest 1993; 103:1421–5.
164. Munk PL, Vellet AD, Rankin RN, Muller NL, Ahmad D. Intracavitary aspergilloma: transthoracic percutaneous injection of amphotericin gelatin solution. Radiology 1993; 188:821–3.
165. Lee KS, Kim HT, Kim YH, Choe KO. Treatment of hemoptysis in patients with cavitary aspergilloma of the lung: value of percutaneous instillation of amphotericin B. AJR Am J Roentgenol 1993; 161:727–31.
166. Klein JS, Fang K, Chang MC. Percutaneous transcatheter treatment of an intracavitary aspergilloma. Cardiovasc Intervent Radiol 1993; 16:321–4.
167. Hammerman KJ, Sarosi GA, Tosh FE. Amphotericin B in the treatment of saprophytic forms of pulmonary aspergillosis. Am Rev Respir Dis 1974; 109:57–62.
168. Campbell JH, Winter JH, Richardson MD, Shankland GS, Banham SW. Treatment of pulmonary aspergilloma with itraconazole. Thorax 1991; 46:839–41.
169. Dupont B. Itraconazole therapy in aspergillosis: study in 49 patients. J Am Acad Dermatol 1990; 23:607–14.
170. Impens N, De Greve J, De Beule K, Meysman M, De Beuckelaere S, Schandevyl W. Oral treatment with itraconazole of aspergilloma in cavitary lung cancer. Eur Respir J 1990; 3:837–9.
171. Tsubura E. [Multicenter clinical trial of itraconazole in the treatment of pulmonary aspergilloma. Pulmonary Aspergilloma Study Group]. Kekkaku 1997; 72:557–64 (Abstract).
172. Soltanzadeh H, Wychulis AR, Sadr F, Bolanowski PJ, Neville WE. Surgical treatment of pulmonary aspergilloma. Ann Surg 1977; 186:13–16.
173. Massard G, Roeslin N, Wihlm JM, Dumont P, Witz JP, Morand G. Pleuropulmonary aspergilloma: clinical spectrum and results of surgical treatment. Ann Thorac Surg 1992; 54:1159–64.
174. Kilman JW, Ahn C, Andrews NC, Klassen K. Surgery for pulmonary aspergillosis. J Thorac Cardiovasc Surg 1969; 57:642–7.
175. Chen JC, Chang YL, Luh SP, Lee JM, Lee YC. Surgical treatment for pulmonary aspergilloma: a 28 year experience. Thorax 1997; 52:810–13.
176. Uflacker R, Kaemmerer A, Picon PD, et al. Bronchial artery embolization in the management of hemoptysis: technical aspects and long-term results. Radiology 1985; 157:637–44.
177. Basich JE, Graves TS, Baz MN, et al. Allergic bronchopulmonary aspergillosis in corticosteroid-dependent asthmatics. J Allergy Clin Immunol 1981; 68:98–102.
178. Mroueh S, Spock A. Allergic bronchopulmonary aspergillosis in patients with cystic fibrosis. Chest 1994; 105:32–6.
179. Wang JL, Patterson R, Rosenberg M, Roberts M, Cooper BJ. Serum IgE and IgG antibody activity against Aspergillus fumigatus as a diagnostic aid in allergic bronchopulmonary aspergillosis. Am Rev Respir Dis 1978; 117:917–27.
180. Cockrill BA, Hales CA. Allergic bronchopulmonary aspergillosis. Annu Rev Med 1999; 50:303–16.
181. Knutsen AP, Slavin RG. In vitro T cell responses in patients with cystic fibrosis and allergic bronchopulmonary aspergillosis. J Lab Clin Med 1989; 113:428–35.
182. Chauhan B, Santiago L, Kirschmann DA, et al. The association of HLA-DR alleles and T cell activation with allergic bronchopulmonary aspergillosis. J Immunol 1997; 159:4072–6.
183. Bosken CH, Myers JL, Greenberger PA, Katzenstein AL. Pathologic features of allergic bronchopulmonary aspergillosis. Am J Surg Pathol 1988; 12:216–22.
184. Rosenberg M, Patterson R, Mintzer R, Cooper BJ, Roberts M, Harris KE. Clinical and immunologic criteria for the diagnosis of allergic bronchopulmonary aspergillosis. Ann Intern Med 1977; 86:405–14.
185. Mintzer RA, Rogers LF, Kruglik GD, Rosenberg M, Neiman HL, Patterson R. The spectrum of radiologic findings in allergic bronchopulmonary aspergillosis. Radiology 1978; 127:301–7.
186. Greenberger PA, Patterson R. Diagnosis and management of allergic bronchopulmonary aspergillosis. Ann Allergy 1986; 56:444–8.
187. Greenberger PA. Immunologic aspects of lung diseases and cystic fibrosis. Jama 1997; 278:1924–30.
188. Patterson R, Greenberger PA, Radin RC, Roberts M. Allergic bronchopulmonary aspergillosis: staging as an aid to management. Ann Intern Med 1982; 96:286–91.
189. Patterson R, Greenberger PA, Halwig JM, Liotta JL, Roberts M. Allergic bronchopulmonary aspergillosis. Natural history and classification of early disease by serologic and roentgenographic studies. Arch Intern Med 1986; 146:916–18.
190. Rosenberg M, Patterson R, Roberts M, Wang J. The assessment of immunologic and clinical changes occurring during corticosteroid therapy for allergic bronchopulmonary aspergillosis. Am J Med 1978; 64:599–606.
191. Wang JL, Patterson R, Roberts M, Ghory AC. The management of allergic bronchopulmonary aspergillosis. Am Rev Respir Dis 1979; 120:87–92.
192. Capewell S, Chapman BJ, Alexander F, Greening AP, Crompton GK. Corticosteroid treatment and prognosis in pulmonary eosinophilia. Thorax 1989; 44:925–9.
193. Safirstein BH, D’Souza MF, Simon G, Tai EH, Pepys J. Fiveyear follow-up of allergic bronchopulmonary aspergillosis. Am Rev Respir Dis 1973; 108:450–9.
194. Mikita CP, Mikita JA. Allergic bronchopulmonary aspergillosis. Allergy Asthma Proc 2006; 27:82–4.
195. Hilton AM, Chatterjee SS. Bronchopulmonary aspergillosis– treatment with beclomethasone dipropionate. Postgrad Med J 1975; 51(Suppl. 4):98–103.
196. Seaton A, Seaton RA, Wightman AJ. Management of allergic bronchopulmonary aspergillosis without maintenance oral corticosteroids: a fifteen-year follow-up. Q J Med 1994; 87:529–37.
197. Stevens DA, Schwartz HJ, Lee JY, et al. A randomized trial of itraconazole in allergic bronchopulmonary aspergillosis. N Engl J Med 2000; 342:756–62.
198. Skov M, Main KM, Sillesen IB, Muller J, Koch C, Lanng S. Iatrogenic adrenal insufficiency as a side-effect of combined treatment of itraconazole and budesonide. Eur Respir J 2002; 20:127–33.