Исмиген или бронхомунал для ребенка что лучше
Средства для повышения иммунитета
Вопрос иммунитета актуален сегодня, как никогда. Есть ли препараты для его усиления? Как правильно это сделать без вреда для здоровья?
Что влияет на иммунитет
Так как иммунитет — это комплекс реакций всего организма для защиты от внешних вторжений, на его работу влияет множество факторов. Сюда можно отнести:
Все эти факторы влияют на иммунитет в комплексе. Если, какое-то воздействие избыточно и организм не может с ним справиться в пределах нормальной реакции, могут возникать сбои, которые приводят в том числе и к снижению иммунитета. Например, короткий контролируемый стресс в виде закаливания, тренировки, некоторого периода голода простимулирует организм и поможет укрепить иммунитет.
Если стресс хронический, например, эмоциональный, это приводит к истощению нервной системы, разбалансировке гормонального фона и, естественно, отражается на иммунной системе. Так в исследованиях было показано, что после хронического стресса при контакте с вирусом, типа ОРВИ, у этих людей развивались выраженные симптомы, как слабость, выделения из носа. У другой группы, без воздействия стресса эти симптомы были минимальны или отсутствовали.
Значительная часть бактерий и вирусов поступает в организм через пищеварительную систему. Если нарушена работа ферментов, кислотность, микрофлора, повышена проницаемость кишечной стенки, есть воспалительные процессы, ослаблен местный иммунитет, тогда может снижаться защитная функция и чужеродные агенты могут попасть в кровь.
Гормональные препараты, вредные привычки, инфекции могут ослаблять иммунитет. Часто мы забываем о таком важном элементе здоровья, как сон. Недостаток сна и его нарушения, также могут снижать защитные силы организма.
Нарушения иммунитета
Изменения в работе иммунной системы можно разделить на 2 вида:
Во втором случае запускаются процессы воспаления, которые повреждают собственные ткани организма. Речь идет о таких проблемах, как:
Разберем более подробно ситуацию снижения иммунитета.
Низкий иммунитет
Как понять что иммунитет ослаблен и надо срочно что-то делать? Многие слышали такое понятие, как ЧБД — часто болеющие дети. Родители считают количество ОРВИ в год и если оно превышает 4 раза начинают волноваться. Но ВОЗ считает нормой у детей посещающих детский сад и младших школьников цифру 8, если это обычная простуда.
Насторожить как у детей, так и взрослых должны:
Проблемы с иммунитетом могут быть врожденного характера, связанные с генетическими особенностями, или приобретенного, то есть возникшие в процессе жизни.
Что делать
Кажется, что если иммунитет низкий, нужно срочно его повысить. Благо в аптеке можно найти множество иммуномодуляторов с обещанием сделать иммунитет сильнее. Прежде чем глотать таблетки, можно обратить внимание на факторы риска. Ведь без их устранения улучшения могут быть только временными. Это будет все равно что стучать молотком по пальцу, но каждый раз потом накладывать лечебную мазь. Может сначала стоит убрать молоток.
Выполнить все рекомендации мало кому удается, поэтому хочется прибегнуть к достижениям современной науки.
Препараты
Непосредственно к иммуномодуляторам можно отнести только те продукты, которые непосредственно модулируют, то есть напрямую действуют на какие-то звенья иммунитета. В идеале, они должны приводить его работу в норму. Все остальные как витамины, БАДы, адаптогены могут оказывать влияние на иммунитет, но называть их иммуномодуляторами не совсем корректно.
Иммуномодуляторы
Идеального иммуномодулятора, который бы при приеме приводил в норму все звенья иммунитета пока не существует. К настоящим иммуномодуляторам на сегодняшний день можно отнести:
Эти молекулы действуют на конкретные звенья иммунной цепи и их действие относительно изучено.
Лизаты
Витамины и микроэлементы
Витамин D обладает очень широким спектром действия на весь организм, а не только на состояние костей и мышц. Если рассматривать его влияние на иммунитет, то здесь он способствует снятию воспаления за счет блокирования взаимодействия между клетками иммунитета. При его дефиците растет риск аутоиммунных заболеваний (ревматоидный артрит, системная красная волчанка, сахарный диабет 1 типа). Витамин D обладает иммуномодулирующими свойствами и может повышать гуморальный и клеточный иммунитет. Существуют водо- и жирорастворимые формы холекальциферола. При нарушении работы пищеварения может нарушаться его усвояемость.

Витамин С оказывает стимулирующее действие на иммунную систему. Под его действием нейтрофилы увеличивают свою способность распознавать и уничтожать бактерии и вирусы. Аскорбиновая кислота нужна для синтеза эндогенных интерферонов и цитокинов. Комбинация витаминов А,С и цинка стимулирует выработку антител.
Цинк участвует в процессах влияющих на синтез Т-лимфоцитов, стимулирует фагоцитарную активность нейтрофилов. Запасов цинка в организме нет, он должен поступать с мясом, бобовыми, сырами.
Комбинированные препараты
Многие витамины и минералы обладают синергетическим эффектом. При недостатке одних, прием моно препарата может быть неэффективным. Для этого производители выпускают комплексные сбалансированные продукты:
БАДы
Обычно БАДы включают в себя различные вытяжки из трав с адаптогенным эффектом. Нередко их комбинируют с витаминами.
Интерфероны
Эта группа препаратов также очень распространена в России и на постсоветском пространстве. Западные коллеги не разделяют нашего оптимизма по использованию данной группы препаратов и применяют её в редких случаях при определенных заболеваниях. Но не у обычных людей с симптомами ОРВИ и тем более не для профилактики.
На нашем рынке представлены:
Вывод
Просто так принимать средства напрямую усиливающие иммунитет не следует. Это может спровоцировать аллергические и аутоиммунные реакции. Лучше заняться общим укреплением здоровья, правильным питанием, восполнением дефицита витаминов и микроэлементов. Если вы подозреваете серьезные проблемы с иммунитетом обратитесь к иммунологу, пройдите профосмотр.
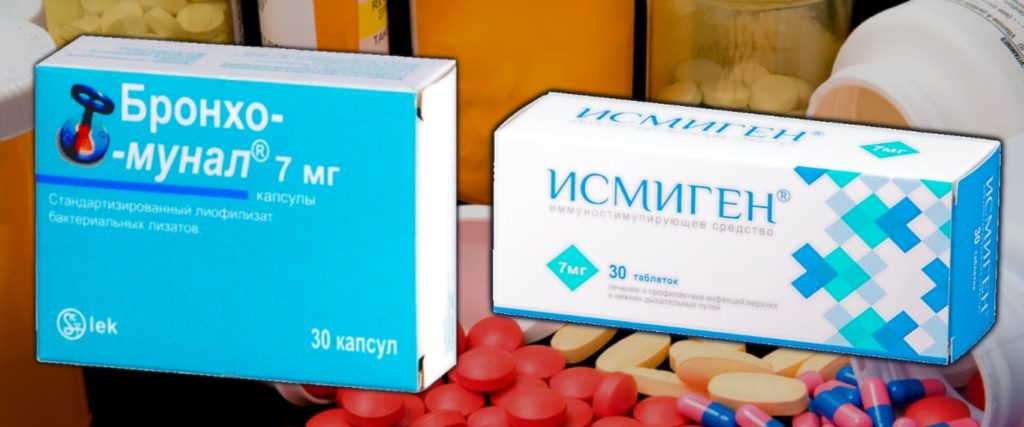
Исмиген или Бронхомунал – что лучше? Коротко о главном!
В качестве профилактического и лечебного средства при заболеваниях органов дыхания врачи часто назначают Бронхомунал и Исмиген. Эти препараты относятся к группе иммуномодулирующих, то есть стимулирующих естественные защитные силы организма. Есть ли разница между этими двумя средствами, и какое лучше?
Сравнение лекарств
Если на выбор назначены Бронхомунал или Исмиген, перед покупкой стоит подробнее ознакомиться с их основными характеристиками. Краткие сведения о составе, показаниях, принципе действия и противопоказаниях помогут сделать правильный выбор.
Состав
Действующим веществом обоих препаратов является лизат (высушенные фрагменты) болезнетворных бактерий, чаще всего вызывающих инфекции органов дыхания:
Состав активного комплекса у Бронхомунала и Исмигена одинаков, а дозировка может отличаться. «Взрослый» вариант для обоих лекарств – 7 мг, для детского Бронхомунала – 3,5 мг. Есть также некоторые отличия в составе вспомогательных веществ.
Механизм действия
Лизат болезнетворных бактерий в составе Бронхомунала и Исмигена при приеме повышает местный и общий иммунитет. Слизистые оболочки органов дыхания и пищеварительных путей начинают активно вырабатывать иммуноглобулины, уничтожающие возбудителей инфекции. усиливается и защита организма в целом, благодаря чему выздоровление ускоряется, уменьшается риск повторного заболевания (рецидива) и обострения хронических форм.
Показания
Исмиген и Бронхомунал назначаются для лечения различных острых воспалений дыхательных путей и лор-органов:
Если перечисленные заболевания носят хронический характер, Исмиген и Бронхомунал используются для профилактики обострений.
Противопоказания
Несмотря на одинаковый состав, в части противопоказаний препараты отличаются. Исмиген нельзя принимать:
Бронхомунал строго противопоказан к приему только в случае индивидуальной непереносимости.
Побочные действия
Бронхомунал переносится хорошо, крайне редко могут возникнуть:
Побочные эффекты лечения Исмигеном тоже встречаются в единичных случаях:
Формы выпуска и цена
Бронхомунал выпускается в Швейцарии в виде капсул для приема внутрь с разной дозировкой действующего вещества:
Исмиген – препарат итальянского производства, представляет собой подъязычные таблетки 7 мг. Стоимость зависит от количества средства в упаковке:
Исмиген или Бронхомунал – что лучше?
Плюсами Исмигена можно считать чуть более доступную цену и отсутствие влияния на желудочно-кишечный тракт (так как активные компоненты усваиваются еще в ротовой полости и желудок с кишечником не раздражают).
В остальном препараты идентичны по сфере применения и эффективности, о чем свидетельствуют отзывы пациентов. Поэтому если нет специфических противопоказаний, выбрать можно любой, ориентируясь на способ приема (внутрь или под язык до полного растворения), а также цену и наличие в аптеке.
Бронхомунал лучше выбрать для ребенка в возрасте от полугода до трех лет, так как подъязычные таблетки малыши правильно принимать просто не могут (а содержимое капсулы можно смешать с пищей или напитками). Этот же препарат предпочтительнее для будущих и кормящих мам (инструкция не запрещает его в таких случаях, но советует соблюдать осторожность). Исмиген же лучше выбрать людям, имеющим заболевания желудка и кишечника, чтобы не повышать риск расстройств пищеварения.
Стенограмма доклада профессора Гаращенко Т.И.
X Съезд педиатров России «Пути повышения эффективности медицинской помощи детям»
«Применение топических иммуномодуляторов в группе часто болеющих детей»
Часть 1
В принципе, в группе часто болеющих детей, как я говорила, ЛОР-патология составляет до 90%. И абсолютно точно, что у половины детей имеется гиперплазия лимфоидной ткани. В первую очередь вы будете это наблюдать в первых возрастных группах, это у детей до 5-летнего возраста редко гиперплазия аденоидных вегетаций в половине случаев. Надо сказать, что аденоидные вегетации в принципе ткань, которая эволюционирует в те сроки, когда эволюционирует тимус. Вам видно, эти параллели, которые имеются между двумя этими органами иммунитета.
Вторая часть, она посвящена конечно гиперплазии лимфоидной ткани глотки. Надо сказать, что очень многие педиатры всегда думают, что гиперплазия физиологическая реакция. Да, существует физиологическая гиперплазия, которая наступает в 5-7 лет. А сейчас окончательным сроком развития миндалин считается возраст 10 лет. Только после 10 лет к ним можно предъявлять какие-то претензии, до этого они еще не окончили свое биологическое развитие. Инволюция миндалин начинается с возраста 55 лет и оканчивается в 175 лет, если бы мы до этого возраста дожили.
Следующая группа: проблема хронических тонзиллитов рецидивирующих в том, что не всегда рецидивирующий тонзиллит. Тонзиллит проходит и остаются зреющие, так называемые тонзиллярные лимфатические узлы. Вот этот единственный лимфатический узел, который находится в средней югулярной группе на передней поверхности шеи.И наконец, надо сказать, что для детей, часто болеющих, характерна еще одна патология. Это рецидивирующие вирусные ларингиты, в том числе не только вирусные ларингиты, но и эпиглосситы, которые у детей, это воспаление лимфоидной ткани надгортанника. Это частая патология.
Что представляет из себя на сегодняшний день иммунная система часто болеющего ребенка? Если мы будем говорить о часто болеющем ребенке, о тех детях, которые болеют чаще 6 раз в году, это может быть группа от 2 до 7лет, она ярко выражается. И группа детей от 7 до 15 лет. То надо сказать, что у детей группы от 2 до 7 лет имеется явное снижение у каждого пятого ребенка вообще из всей группы так называемых Т-хелперов. А вот у детей от 7 и старше лет, если он продолжает болеть больше 6 раз в год, там имеется примерно у 50% снижение и относительного и абсолютного количества уровня основных клеток Т-хелперов, причем не только Т-хелперов, сиди третьих и так называемых четвертых клеток.
Надо сказать, что группа часто болеющих детей компрометировано и по системе противовирусной и киллерной защиты. Вы понимаете, почему в группе часто болеющих детей возможны, в том числе онкопролиферативные заболевания. Потому, что на сегодняшний день дети, которые болеют чаще 6 раз в год от 10 до 15% имеют снижение и сиди 16 клеток киллеров и примерно столько же детей имеют снижение и сиди 19-ых клеток. Не просто, у них еще снижен первый фактор защиты, очень важный, это фагоцитоз. Когда вы смотрите на иммунорегуляторный индекс, или исследуете вообще способность к фагоцитозу, захватыванию, представлению антигена любой бактерии, вируса, гаптена к той иммунной системе, то именно здесь может быть этот пробел. Все остальное нормально, а вот такая система, она у вас не представлена. Следующий слайд. Что в гуморальном иммунитете часто болеющих детей? Надо сказать, у часто болеющих детей у 30% с 2 до 7 лет имеется снижение иммуноглобулина класса G. Причем, надо сказать, что вот такое снижение уровня иммуноглобулина G оно, вот, общего уровня вообще основного антителобразующего сывороточного показателя. И, надо сказать, что кроме этого, а вот у детей, которым больше 7 лет, болеют респираторными заболеваниями или вообще скажем ЛОР-патологией, а в основном доминируют не только вирусная, но и превалирует затем бактериальная патология, это как вы представляете сами по себе. С любой вирусной инфекцией, как говорят французы, вирус выносит приговор, а приводит его в исполнение бактерия.
Любая вирусная инфекция оканчивается, даже грипп, он оканчивается в сроки от 5 до 7 дней. Значит, зачем тогда заставлять приходить на третьи сутки к врачу-терапевту, чтоб за ним смотрели? Именно для того, что бы определиться, не присоединяется ли бактериальная инфекция. Надо сказать, что все эти больные, которые дают так называемые ОРЗ, уже не ОРВИ, а ОРЗ у детей, а фактически каждый пятый ребенок имеет уже после семилетнего возраста диагноз, смешанные показатели иммуноглобулинов G в сыворотке крови, и такой же низкий иммуноглобулина А. Вот это уже предмет вашего, так сказать, размышления, какой больной должен быть обязательно направлен к врачу-иммунологу, аллергологу. У нас эта специальность, вы знаете, совмещена. И что очень важно, обратите внимание, 15-20, 15-20, 50% уровень так скажем CD4 клеток после 7 лет у детей часто болеющих. Но у 90% детей страдают не эти факторы гуморального иммунитета, а первая линия защиты, секреторный иммунитет, та иммунная система, которая сопряжена со слизистыми оболочками. Она более древняя. Она практически автономна. Может работать автономно и поэтому, следующий слайд, когда мы с вами определяем вообще часто болеющего ребенка, особенно развивающегося ребенка.
Это препарат имудон вы видите, содержит 13 штаммов бактерий. Повышает уровень иммуноглобулина А, фагоцитоз и усиливает выработку лизоцима. Применяется у детей с целью лечения по 6 таблеток в день, и с целью профилактики. Вот скажем, вашей обычной 20-дневной профилактики. Пожалуйста, следующий слайд. Вы видите, в состав этого препарата входит лактобактерия. Помните, я вам показывала, тяжелейшие заболевания иммунокомпрометированных детей вот они чем вызываются. Enterococcus fekalis, Enterococcus sangvinis для стоматитов, золтистый стафилококк, Klebsiella pneumonie, которая вызывает тяжелые формы септических заболеваний легких и менингиты у детей, особенно первого может быть года жизни и коренебактерия дифтерии. Обратите внимание, Candida albikans, у нас ни в одном другом препарате, кроме этого препарата, нет фрагментов этих бактериальных лизатов против Candida. Пожалуйста, следующий слайд. Как вставлены возбудители инфекций в эти препараты? Вы должны вот сейчас увидеть разницу, есть препараты топические, вы видите ИРС19. Есть препараты бронхомунал и рибомунил. Практически такой же состав у бронхомунала, как у ИРС19, но однако этот топически применяется, а тот системно. И вы видите, вакцина ВП4 у него комбинированный способ применения: вначале дают интраназально, затем орально. 5 дней вы даете интраназально, затем 5 дней орально. Или же можете вводить этот препарат еще и внутримышечно. Но, не советую вводить, потому, что иногда дает анафилактические реакции. Пожалуйста, следующий.
Иммунопрофилактика острых респираторных инфекций: рутинная практика и новые возможности
Появление в арсенале педиатров нового иммуномодулятора бактериального происхождения, характеризующегося хорошей переносимостью и высокой клинико-иммунологической эффективностью, позволяет надеяться, что его применение в комплексной программе иммунопрофила
Occurrence of the new immunomodulator of bacterial origin in pediatrician’s arsenal, which is characterized by good endurability and high clinic and immunologic efficiency gives us the hope that its application in the complex immunoprophylaxis program in children will allow to significantly reduce the rate of morbidity and frequency of exacerbations in patients with recurrent diseases of respiratory tract.
Острые респираторные инфекции (ОРИ) остаются наиболее частыми инфекционными заболеваниями у детей [1, 2]. Отмечено, что среди всех причин обращения за медицинской помощью в детские поликлиники более 70% приходится на ОРИ, а в период сезонного подъема заболеваемости этот показатель достигает 90%. Высокий уровень заболеваемости детей ОРИ, нередкое при этом развитие тяжелых осложнений, а также существенный экономический и социальный ущерб определяют необходимость разрабатывать и внедрять в практику эффективные способы профилактики [1–3].
Доказано, что наиболее эффективным способом профилактики инфекционных заболеваний является вакцинопрофилактика [4]. При этом, обсуждая проблему респираторных инфекций в педиатрии, обязательно следует подчеркнуть знаковое для России событие — включение в последние годы в Национальный календарь прививок вакцинацию против гемофильной В (Нib) и пневмококковой инфекции [5]. Опыт стран, где вакцинация детей против пневмококковой и Нib-инфекции проводится уже в течение ряда лет, свидетельствует о снижении частоты тяжелых пневмоний и острых средних отитов, вызванных данными возбудителями [6].
Существенный вклад в снижение заболеваемости острыми респираторными инфекциями вносит и программа вакцинации против гриппа. Однако следует отметить, что, несмотря на высокую иммуногенность современных гриппозных вакцин, их профилактическая эффективность в ряде случаев может быть ниже ожидаемой. Это обусловлено очень высокой антигенной изменчивостью гриппозных возбудителей, что может приводить к несовпадению вакцинных штаммов с эпидемическими. Примером может служить текущий эпидсезон, в течение которого отмечено появление и широкое распространение новой разновидности вируса гриппа А (H3N2), который существенно отличается от вакцинного штамма, что, вероятно, и определило интенсивность эпидемического процесса в период 2014–2015 гг. [7].
Так, в России, как и во многих странах мира, по индикаторам интенсивности эпидемический подъем заболеваемости в 2014–2015 гг. был выше по сравнению с сезоном 2013–2014 гг. Доминирующим в структуре циркулирующих вирусов гриппа был A (H3N2), на долю которого, по предварительным результатам, пришлось более 50,0%. В отличие от предыдущего года большую активность проявил вирус гриппа В, долевое участие которого составило более 20%. В ряде регионов России регистрируют случаи гриппа A (H1N1)pdm09, с которым, как и ранее, связывают более тяжелое течение гриппозной инфекции и летальные случаи. В среднем по РФ, к 7–8 неделе 2015 г. показатели заболеваемости гриппом и острыми респираторными вирусными инфекциями (ОРВИ) «прошли» пиковые значения и приобрели стойкую тенденции к снижению [8].
Оперативная информация Роспотребнадзора об эпидситуации по заболеваемости ОРВИ и гриппом в Российской Федерации за период с 2 по 8 марта 2015 г. свидетельствует в целом о том, что, несмотря на четкую тенденцию к снижению недельных уровней заболеваемости, в некоторых регионах она все еще остается высокой [9]. Так на 10-й неделе 2015 г. на территории России превышение недельных эпидемических порогов заболеваемости гриппом и ОРВИ по совокупному населению было зарегистрировано в 22 субъектах. При этом превышение эпидпорога по центральному городу без превышения эпидпорога по субъекту зарегистрировано в 10 городах: Белгород, Владимир, Орел, Рязань, Тула, Уфа, Казань, Ижевск, Чебоксары и Пенза. Среди детей в возрасте 0–2 года превышение недельных порогов заболеваемости отмечено в 8 субъектах, среди детей 3–6 лет недельные пороги заболеваемости ОРВИ и гриппом превышены в 18 субъектах, в возрастной группе 7–14 лет превышение недельных порогов заболеваемости зарегистрировано в 30 субъектах Российской Федерации. Среди лиц старше 15 лет превышение недельных порогов заболеваемости отмечено в 15 субъектах Российской Федерации. В связи с высоким уровнем заболеваемости гриппом и ОРВИ в указанных регионах в ряде детских образовательных учреждений в период 10-й недели (2–8 марта 2015) продолжалось приостановление учебного процесса для снижения интенсивности циркуляции респираторных вирусов. При этом в указанный период в структуре респираторных вирусов продолжают доминировать вирусы гриппа А (H3N2) и В [9].
В США текущий эпидсезон (2014–2015 гг.) по данным Центров по контролю и профилактике заболеваний (Centers for Disease Control and Prevention, CDC) также характеризуется преобладанием вирусов гриппа А (H3N2) в этиологической структуре гриппозной инфекции [7]. При этом среди 1150 штаммов вируса гриппа, выделенных от пациентов и антигенно верифицированных, вирусы гриппа А (Н3N2) составили 78,4%, вирусы гриппа В — 21,4%, а вирусы гриппа А (Н1N1) обнаруживали в единичных случаях (0,2%). Следует отметить, что среди вирусов гриппа А (Н3N2) значительно (73,6%) преобладал вирус гриппа А/Швейцария/9715293/13 (Н3N2), антигены которого существенно отличаются от вакцинного штамма сезона 2014–2015 гг. В то же время текущий сезон (2014–2015 гг.) характеризуется значительным совпадением между эпидемическими и вакцинными штаммами вируса гриппа В. Так, процент совпадения по вирусу гриппа В/Массачусетс/2/2012 (линия Ямагата) составляет более 92%, а по вирусу гриппа В/Брисбен/60/2008 (линия Виктория) — более 93% [7].
Таким образом, одной из причин большей интенсивности эпидемии 2014–2015 гг. стало появление, а затем широкое распространение дрейф-варианта вируса гриппа A (H3N2), штамма А/Швейцария/9715293/13, который по своим биологическим свойствам значительно отличается от свойств вируса, входившего в состав гриппозных вакцин, рекомендованных для стран Северного полушария (А/Техас/50/2012). Однако хотя новый вариант и изменил свои свойства, вакцинный штамм относился к этому же подтипу вируса гриппа и, следовательно, мог обеспечить защиту привитых, в частности, от тяжелых форм гриппозной инфекции и развития осложнений. Такие же различия были получены и в отношении вируса гриппа В, который также изменил свои свойства по сравнению с вакцинным (В/Пхукет/3073/2013 и В/Массачусетс/2/2012 соответственно). Все из циркулирующих штаммов чувствительны к препаратам с антинейраминидазной активностью (осельтамивир, занамивир, перамивир) и продолжают оставаться резистентными к ремантадину.
Учитывая высокую антигенную изменчивость вирусов гриппа и отсутствие прививок против других острых респираторных вирусных инфекций, существенным дополнением к программе вакцинопрофилактики является комбинация ее с неспецифическими иммунопрофилактическими средствами. Особое значение указанный подход приобретает для детей с рекуррентными респираторными инфекциями, которых в отечественной педиатрической практике принято называть «часто болеющими» [2, 10, 11]. Для неспецифической иммунопрофилактики острых и рекуррентных респираторных инфекций используют препараты природного и рекомбинантного интерферона, химические и биологические индукторы эндогенного интерферона, а также иммуномодуляторы бактериального происхождения, которые имеют наиболее высокий уровень доказательности. К иммуномодуляторам бактериального происхождения относятся бактериолизаты (Исмиген, Бронхо-Ваксом, Бронхо-мунал, ИРС 19, Имудон), рибосомально-протеогликановые комплексы (Рибомунил) и синтетические аналоги компонентов клеточной мембраны бактериальной стенки (Ликопид) [12].
Высокая профилактическая и клинико-иммунологическая эффективность бактериальных иммуномодуляторов доказана результатами целой серии рандомизированных, контролируемых исследований, а также представлена в систематических обзорах и метаанализах [13–16]. В основе механизма действия препаратов данного класса лежат процессы, инициирующие естественную активацию иммунитета. Так, входящие в состав бактериальных иммуномодуляторов универсальные «маркеры чужеродности» (фрагменты клеточной мембраны, содержащие липополисахариды и/или протеогликаны), распознаются Toll-подобными рецепторами гранулоцитов и дендритных клеток, что является первоначальным импульсом для активации врожденного иммунитета. При этом усиливается фагоцитоз в исполнении нейтрофилов, моноцитов и тканевых макрофагов, повышается активность дендритных клеток и натуральных киллеров, усиливается продукция интерферона и других цитокинов. Благодаря стимуляции факторов врожденного иммунитета повышается противоинфекционная резистентность, что активно препятствует размножению как вирусных, так и бактериальных возбудителей, в случае их проникновения в организм.
Кроме этого бактериолизаты и рибосомально-протеогликановые комплексы, благодаря антигенам, содержащимся в их составе, активируют адаптивный иммунитет, вызывая вакциноподобный эффект. При этом отмечено, что специфическая антителопродукция осуществляется преимущественно в системе местного иммунитета. Увеличение концентрации специфических иммуноглобулинов в секретах (слюна, назальная и трахеобронхиальная слизь) против тех пневмотропных бактериальных возбудителей, антигены которых представлены в препаратах, определяет высокий профилактический потенциал терапии, существенно снижая риск рецидивов респираторных бактериальных инфекций. Учитывая, что современные бактериальные иммуномодуляторы являются высокоочищенными препаратами, изготовленными из инактивированных возбудителей, их применение характеризуется не только клинико-иммунологической эффективностью, но и высоким профилем безопасности [13–16].
При изучении фармакологических эффектов бактериальных иммуномодуляторов было установлено, что позитивное влияние на адаптивный иммунитет оказывают только те препараты, в которых антигены возбудителей не повреждены и представлены в достаточной концентрации. При этом активация приобретенного иммунитета напрямую зависит от иммуногенности препаратов. В связи с этим особые надежды возлагаются на Исмиген — иммуномодулятор бактериального происхождения с более высоким уровнем иммуногенности [12]. Последнее достигается за счет особенностей технологии производства препарата — Исмиген получают за счет разрушения бактерий под действием высокого давления, а не путем химической инактивации, как другие лизаты. Считается, что благодаря этому в препарате Исмиген большая часть антигенов сохраняется неповрежденными, что и определяет высокую клинико-иммунологическую эффективность.
Исмиген содержит продукты лизиса как грамположительных (Streptococcus pneumoniae (6 серотипов), Staphylococcus aureus, Streptococcus pyogenes, Streptococcus viridans), так и грамотрицательных возбудителей (Klebsiella pneumoniae, Klebsiella ozaenae, Haemophilus influenzae b, Moraxella catarrhalis). Исмиген, как и другие бактериальные лизаты, обладает комбинированным иммунологическим эффектом, характеризующимся одновременной активацией врожденного и адаптивного иммунитета. Препарат выпускается в таблетках для сублингвального применения и разрешен для лечения и профилактики острых респираторных инфекций у взрослых и детей старше 3 лет [12]. Таблетки Исмиген принимаются сублингвально для улучшения контакта антигенов со слизистой ротовой полости (часть слизистой всей дыхательной системы). При этом было доказано, что сублингвальный прием препарата может дополнительно способствовать более высокой эффективности. За счет непосредственного взаимодействия бактериальных компонентов, входящих в Исмиген, со слизистой полости рта, устраняется риск снижения иммуногенности препарата под действием ферментов желудочно-кишечного тракта [17].
G. F. Rossi (2003) изучал влияние Исмигена на состояние местного иммунитета, а также его клиническую эффективность у 34 детей и взрослых c рекуррентными респираторными инфекциями [19]. При этом исходное состояние местного иммунитета против таких наиболее частых бактериальных возбудителей респираторного тракта, как Klebsiella pneumoniae, Staphylococcus aureus, Streptococcus pyogenes, Moraxella catarrhalis, Haemophilus influenzae и Streptococcus pneumonia, характеризовалось низкими уровнями или полным отсутствием специфических s-IgA в слюне у подавляющего большинства обследованных. При этом если к Staphylococcus aureus и Klebsiella pneumonia специфические s-IgA выявляли у 24–29% пациентов соответственно, то к остальным возбудителям еще реже — не выше 12–15%.
Особо было отмечено, что у детей титр штамм-специфических s-IgA в слюне обнаруживали в единичных случаях — у 6,3% обследованных. Проанализировав полученные результаты, G. F. Rossi и соавт. (2003) предположили, что вероятной причиной рекуррентных инфекций является инертность местного иммунитета. В связи с этим была предпринята попытка активизировать штамм-специфический местный иммунитет с помощью поливалентного механического бактериального лизата (Исмиген). При этом было установлено, что курсовое применение препарата Исмиген приводило к существенному повышению концентрации специфических s-IgA в слюне у большинства детей и взрослых [19].
F. Braido и соавт. (2011) при изучении клинико-иммунологической эффективности поливалентного механического бактериального лизата Исмиген у 33 взрослых пациентов с рекуррентными респираторными инфекциями отметили позитивный результат лечения в 78,8% случаев [21]. При этом у 25 из 27 пациентов с положительной клинической динамикой уменьшение частоты респираторных инфекций сопровождалось увеличением в слюне концентрации специфических антител, а также ее опсонизирующей активности против возбудителей, лизаты которых содержатся в препарате. Авторы при этом отметили корреляцию между положительной клинической эффективностью и высоким содержанием в слюне штаммо-специфических IgA и IgG, в то время как зависимости от титров IgМ выявлено не было [21].
Очень интересные данные были получены G. Lanzilli и соавт., которые в серии работ, проведенных как in vitro [22], так и in vivo [23], показали высокую клинико-иммунологическую эффективность поливалентного бактериального лизата Исмиген, в том числе и у пожилых пациентов с хронической обструктивной болезнью легких. При этом было отмечено, что на фоне применения препарата Исмиген в периферической крови значительно увеличивалось количество Т-лимфоцитов (преимущественно CD 3+4+ клеток) и натуральных киллеров. Авторы обратили внимание на тот факт, что количество В-клеток памяти, а также CD 3+ CD 8+ при этом оставалось неизменными, в то время как увеличилось количество ранних и переходных форм В-клеток памяти. Одновременно было отмечено, что терапия Исмигеном сопровождалась усилением синтеза интерлейкинов (ИЛ-2, ИЛ-10, ИЛ-12) и гамма-интерферона. Позитивные сдвиги иммунитета сопровождались модификацией течения заболевания — отмечено уменьшение частоты респираторных инфекций и рецидивов основного заболевания.
Аналогичные клинические результаты были получены M. Cazzola и соавт. (2011) при 12-месячном контролируемом рандомизированном исследовании у 63 взрослых пациентов с хронической обструктивной болезнью легких [24]. Установлено, что 3-месячный курс терапии Исмигеном повышал эффективность базисной терапии, что позволило снизить частоту обострений, применения глюкокортикоидов и антибиотиков, а также уменьшить число госпитализаций. На основании полученных данных авторы делают вывод о необходимости включать Исмиген в комплексную терапию при хронической обструктивной болезни легких [24].
R. Ricci и соавт. (2014) при проведении многоцентрового, рандомизированного, двойного слепого, плацебо-контролируемого исследования также отметили высокую клинико-иммунологическую эффективность у пожилых пациентов с хронической обструктивной болезнью легких [25]. При этом было установлено, что позитивные иммунологические эффекты Исмигена (активация дендритных клеток, усиление фагоцитоза, повышение титров штамм-специфических антител с опсонизирующей активностью в слюне) сопровождались четким клиническим улучшением — у пациентов на фоне терапии снижалась заболеваемость острыми респираторными инфекциями и уменьшалась частота рецидивов [25].
Особый интерес представляют данные о клинико-иммунологической эффективности Исмигена у детей [19, 26, 27]. Так, F. Rosaschino и L. Cattaneo (2004) в пилотном, рандомизируемом, открытом, контролируемом исследовании провели изучение переносимости и клинической эффективности Исмигена у 89 детей с рекуррентными респираторными инфекциями. Период наблюдения составил 12 месяцев: 3 месяца во время лечения и 9 последующих месяцев после окончания терапии. Было установлено, что применение Исмигена способствовало значительному сокращению числа респираторных инфекций. При этом в осенне-зимний период частота респираторных инфекций в группе детей, получавшей Исмиген, была на 40% ниже, чем у пациентов из группы контроля пациента (p
* ГБОУ ДПО РМАПО МЗ РФ, Москва
** ГОУ ВПО ХМАО-Югры ХМГМА, Ханты-Мансийск
*** ФГБУ ФНИЦЭМ им. Н. Ф. Гамалеи МЗ РФ, Москва