какие клетки свертывают кровь
Кровотечение должно быть остановлено
Кровь как орган
Форменные элементы крови
Рисунок 1. Форменные элементы крови
Тромбоциты (кровяные пластинки) представляют собой фрагменты гигантских клеток костного мозга. Совместно с белками плазмы они обеспечивают быстрое свертывание крови, вытекающей из поврежденного кровеносного сосуда, что приводит к остановке кровотечения и тем самым защищает организм от кровопотери.
Баланс свертывающей и противосвертывающей систем крови
Факторы, нарушающие это хрупкое равновесие, например, даже незначительные повреждения стенки кровеносного сосуда приводят к ускорению времени свертывания крови и образованию более крупных сгустков крови, видимых невооруженным глазом. Поэтому неудивительно, что и искусственный клапан сердца также может нарушить естественный баланс свертывающей и противосвертывающей систем.
Для измерения свертываемости крови необходим простой анализ на определение времени свертывания крови, позволяющий рассчитать международное нормализованное отношение (МНО) при помощи автоматического анализатора свертывания крови.
Чем ниже МНО, тем быстрее сворачивается кровь, то есть тем она «гуще». Чем выше МНО, тем дольше сворачивается кровь, то есть тем она «жиже» и выше опасность кровотечений.
Анализ на свертывание крови позволит подобрать наиболее оптимальную дозировку антикоагулянтов.
«Внутрисосудистое свертывание крови при COVID-19 определяет весь ход болезни»
 Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Сегодня известно, что при COVID-19, в первую очередь, страдает свертывающая система крови. Вот почему у всех умерших от осложнений новой коронавирусной инфекции находят большое количество тромбов. Как это объяснить? Почему это заметили не сразу? Каким образом и почему это происходит? Можно ли предотвратить развитие такого осложнения? Об этом – наш разговор с А.Д. Макацария, академиком РАН, одним из крупнейших в мире специалистов по изучению нарушений свертываемости крови, создателем Школы клинической гемостазиологии, заведующим кафедрой Сеченовского университета. Александр Давидович и его ученики активно сотрудничают с университетом Сорбонны, Венским, Римским, Миланским и Тель-Авивским университетами, Технион в Хайфе. Под его руководителем защищено 150 кандидатских и докторских диссертаций. Автор более 1200 научных трудов, в том числе 40 монографий.
– Александр Давидович, в последнее время во всем мире появляется всё больше сообщений о том, что при COVID-19 страдает свертывающая система крови. Так ли это, и если да, то чем вы объясняете этот феномен?
– Безусловно, это так. Более того, хочу сказать, что практически нет такой инфекции (вирусной или, тем более, бактериальной), которая бы не влияла на свертывание крови. Доказательство тому – учение о сепсисе и септическом шоке как универсальной модели ДВС-синдрома – синдрома диссеминированного внутрисосудистого свертывания крови. Степень тяжести тромботических нарушений зависит от особенностей возбудителя и организма-хозяина (иммунная система, система гемостаза, наличие сопутствующих заболеваний и т.д.).
– Но ведь не у всех пациентов развивается сепсис и септический шок?
– Конечно, не у всех. Поэтому очень актуальным и далеко не изученным в настоящее время является механизм патогенеза осложнений, вызванных коронавирусной инфекцией. Во многом это обусловлено особенностями вируса, а также особенностями организма человека, начиная от количества и качества рецепторов, представленных у человека и их способностью связываться с этим вирусом. Безусловно, на исходы заболевания огромное влияние оказывает коморбидность, то есть наличие сопутствующих хронических заболеваний у пациента.
– Почему, по вашему мнению, эта особенность течения болезни проявилась не сразу?
— Я считаю, что все это проявилось сразу, но не было адекватно оценено врачами изначально: еще не было такого количества вскрытий и широкого тестирования на гемостазиологические маркеры. Надо сказать, мы занимаемся изучением этой проблемы довольно давно, практически с самого начала эпидемии. Еще в самом начале апреля мы опубликовали работу, основанную на первых наблюдениях наших китайских коллег. Работа называлась «COVID-19 и синдром диссеминированного внутрисосудистого свертывания крови». Она имела чрезвычайно широкий резонанс, поскольку уже тогда врачи начали понимать роль свертывающей системы крови в инфекционном процессе.
– Каков механизм тромбообразования при covid-19 и отличается ли он от этого процесса при других патологиях?
– Это очень непростой вопрос. На сегодняшний день однозначно можно утверждать – при этом вирусе с самого начала имеет место активация гемостаза, внутрисосудистое свертывание крови и тромбообразование в сосудах мелкого калибра жизненно важных органов. При этом повреждаются не только легкие, а блокада микроциркуляции и ее необратимый характер определяют исход заболевания. Позднее начало антикоагулянтной терапии является неблагоприятным фактором. Причем этот процесс внутрисосудистого свертывания в капиллярах легкого играет важную роль в развитии острого респираторного дистресс-синдрома (ОРДС), о котором все говорят. Но далеко не все с самого начала уловили связь между внутрисосудистым свертыванием крови и ОРДС.
В западной литературе даже появился термин «легочная интраваскулярная коагуляция». Практически во всех случаях имеет место активация системного воспалительного ответа. Это общебиологическая реакция, которая особенно проявляется в ответ на инфекцию, вирусные возбудители. Международные организации признали, что коронавирусная инфекция – это сепсис.
Таким образом, цитокиновый и тромботический шторм усугубляют состояние больного и определяют степень тяжести. Но есть и особенности. Возможно, при COVID-19 в первую очередь повреждается фибринолиз – часть системы гемостаза, которая обеспечивает процесс разрушения уже сформированных кровяных сгустков, тем самым, выполняя защитную функцию предотвращения закупорки кровеносных сосудов фибриновыми сгустками. Отсюда синдром фибринирования при меньшей частоте геморрагических осложнений. И отсюда же открывается перспектива применения тромболитиков, о чем сейчас так много говорят и пишут. А впервые предложили такую схему наши американские коллеги.
– А ведь есть немало людей с нарушениями свертываемости крови. Сейчас, во время эпидемии, для них настали трудные времена.
– Это так. В нашей популяции есть люди не только с явными, но и со скрытыми нарушениями гемостаза, предрасполагающими к тромбозам – генетические тромбофилии, антифосфолипидный синдром и ряд других заболеваний, сопровождающихся избыточной активацией системы гемостаза; а также люди с высокой готовностью к супервоспалительному ответу (врожденные факторы и ряд ревматологических и иммунных заболеваний). Им сейчас важно контролировать своё состояние, а врачам не забывать об этом.
Вообще надо сказать, что открытие NET расширило горизонты в понимании биологии нейтрофилов и роли этих клеток в организме. Использование организмом хозяина хроматина в сочетании с внутриклеточными белками в качестве естественного противомикробного агента имеет древнюю историю и меняет наше представление о хроматине как только о носителе генетической информации. Благодаря избыточному и неконтролируемому формированию NET, нейтрофилы могут способствовать развитию патологического венозного и артериального тромбоза, или «иммунотромбоза», а также играют важную роль в процессах атеротромбоза и атеросклероза. Высвобождение NET является, как выяснилось, одной из причин тромбообразования при таких состояниях, как сепсис и рак. Наличие NET при этих заболеваниях и состояниях дает возможность использовать их или отдельные компоненты в качестве потенциальных биомаркеров. NET и их компоненты могут быть привлекательны в качестве терапевтических мишеней. Дальнейшие исследования нейтрофилов и NET необходимы для разработки новых подходов к диагностике и лечению воспалительных и тромботических состояний.
– Размышляя о высокой летальности у пациентов, которым пришлось применить ИВЛ, вы констатируете, что мы, возможно, пошли не тем путем. А какой путь может оказаться более верным?
– Да, я имел в виду, что при оценке вентиляционно-перфузионных нарушений при COVID-19 превалируют перфузионные нарушения, нарушения микроциркуляции, а это значит, что главная терапевтическая мишень – восстановление нормальной перфузии тканей, то есть противотромботическая терапия, а возможно, даже и фибринолитическая. Механическая вентиляция не может решить вопрос перфузионных нарушений.
– Видите ли вы, что в связи с эпидемией стали более частыми проблемы тромбообразования в акушерско-гинекологической практике?
– Случилось так, что во многом и благодаря нашим стараниям (лекциям и публикациям), большинство акушеров сегодня осведомлены о том, что беременность – это состояние так называемой физиологической гиперкоагуляции, и этим пациенткам нередко назначаются антикоагулянты во время беременности. Тем не менее, требуются дальнейшие исследования для вынесения суждения о частоте тромбозов у беременных с COVID-19.
Вообще надо сказать, что большинство осложнений беременности либо обусловлены, либо сочетаются с высоким тромбогенным потенциалом. Генетические факторы свертывания крови, особенно антифосфолипидный синдром, являются факторами риска огромного количества осложнений беременности – это и внутриутробные гибели плода, и неудачи ЭКО, и задержка внутриутробного развития плода, и преждевременная отслойка плаценты, что приводит к тяжелым тромбогеморрагическим осложнениям, это, наконец, тромбозы и тромбоэмболии. Поэтому, конечно, можно ожидать, что в условиях COVID-19 эти осложнения могут представлять собой еще большую опасность. Ведь вирус может быть фактором, активирующим факторы свертываемости крови. Конечно, тут нужны обобщающие исследования, но уже сейчас наши отдельные наблюдения говорят о том, что риск таких осложнений возрастает.
– Являются ли, на ваш взгляд, одним из проявлений этой проблемы случаи тяжелого течения covid-19 в педиатрии (состояния, похожие на синдром Кавасаки)?
– Глава ВОЗ Тедрос Аданом Гебрейесус призвал врачей всех стран обратить особое внимание на сообщения о том, что у некоторых детей, заразившихся коронавирусом, проявляются симптомы, схожие с еще одним заболеванием — синдромом Кавасаки (мультисистемным воспалительным синдромом). Действительно, в сообщениях из Европы и Северной Америки говорилось, что некоторое число детей поступало в отделения интенсивной терапии с мультисистемным воспалительным состоянием, с некоторыми симптомами, похожими на синдром Кавасаки и синдром токсического шока.
Синдром Кавасаки был впервые описан в 1967 году японским педиатром по имени Томисаку Кавасаки. Он обычно поражает детей до пяти лет. При этом синдроме у пациента начинается воспаление кровеносных сосудов (васкулит) и лихорадка. Болезнь Кавасаки имеет четко выраженный набор симптомов, включая постоянно высокую температуру, покраснение глаз и области вокруг рта, сыпь на теле и покраснение и отек ног и рук.
13 мая нынешнего года в авторитетном медицинском издании The Lancet было опубликовано исследование итальянских врачей, которые сообщили, что в провинции Бергамо, одной из наиболее пострадавших от эпидемии коронавируса, была зафиксирована вспышка синдрома Кавасаки или схожего с ним синдрома.
Важно, что в большинстве случаев дети также имели положительный результат теста на антитела к КОВИД-19, предполагая, что синдром последовал за вирусной инфекцией.
Болезнь Кавасаки имеет тенденцию проявляться в группах генетически похожих детей и может выглядеть немного по-разному в зависимости от генетики, лежащей в основе группы. Это говорит о том, что различные триггеры могут вызывать воспалительную реакцию у детей с определенной генетической предрасположенностью.
Вполне возможно, что атипичная пневмония SARS-COV-2, вызванная вирусом COVID-19, является одним из таких триггеров. Это важный вопрос, требующий пристального изучения.
– Александр Давидович, как вы думаете, почему у всех COVID-19 проявляется по-разному?
– Тут очень важна проблема факторов риска. Всё дело в том, что, помимо видимых болезней типа сахарного диабета или гипертонии, существуют болезни невидимые, о которых мы зачастую даже не подозреваем. В последние годы большое распространение получило учение о генетической тромбофилии. Во всем мире это примерно до 20 процентов людей, которые являются носителями той или иной формы генетической тромбофилии. С этим можно жить сто лет, но если возникает инфекция, травма, делается операция – больной может погибнуть от тромбоэмболии, даже если операция выполнена на высочайшем техническом уровне. Причиной тому – скрытая генетическая тромбофилия – мутация, которая делает её носителя подверженным высокому риску тромбообразования.
Высокая контагиозность вируса и большое количество заболевших поневоле «позволяет» вирусу выявить людей с изначальной явной или скрытой предрасположенностью к тромбозам. Это пациенты не только с генетической тромбофилией или антифосфолипидным синдромом, но и с сахарным диабетом, ожирением, ревматическими болезнями и другими патологическими состояниями, ассоциированными с повышенным свертыванием и/или воспалением.
– Какие методы профилактики и лечения covid-19 вы считаете перспективными?
– Помимо уже названных, это противовирусная терапия, терапия специфическими иммуноглобулинами, противотромботическая терапия и лечение, направленное на снижение воспаления (так называемые антицитокиновые препараты). Многое нам предстоит ещё понять об этом новом для нас заболевании, но постепенно мы движемся в сторону лучшего объяснения многих его механизмов. Вы знаете, я всегда много работал, но, пожалуй, никогда ещё я не был так занят исследовательской и практической работой, как сейчас. Уверен, что она даст свои важные результаты.
Беседу вела Наталия Лескова.
Как работает свертывание крови?
Формирование тромба в кровотоке. Кровеносный сосуд заполнен клетками крови значительно плотнее, чем показано на этом рисунке, так что ситуация там напоминает давку при входе на эскалатор в метро. Маленькие и относительно немногочисленные белые клетки — тромбоциты: справа можно видеть, как они активируются, меняют форму и прикрепляются к стенке сосуда, формируя агрегат — тромб.
Автор
Редакторы
Свертывание крови — крайне сложный и во многом еще загадочный биохимический процесс, который запускается при повреждении кровеносной системы и ведет к превращению плазмы крови в студенистый сгусток, затыкающий рану и останавливающий кровотечение. Нарушения этой системы крайне опасны и могут привести к кровотечению, тромбозу или другим патологиям, которые совместно отвечают за львиную долю смертности и инвалидности в современном мире. Здесь мы рассмотрим устройство этой системы и расскажем о самых современных достижениях в ее изучении.
Каждый, кто хоть раз в жизни получал царапину или рану, приобретал тем самым замечательную возможность наблюдать превращение крови из жидкости в вязкую нетекучую массу, приводящее к остановке кровотечения. Этот процесс называется свертыванием крови и управляется сложной системой биохимических реакций.
Иметь какую-нибудь систему остановки кровотечения — абсолютно необходимо для любого многоклеточного организма, имеющего жидкую внутреннюю среду. Свертывание крови является жизненно необходимым и для нас: мутации в генах основных белков свертывания, как правило, летальны. Увы, среди множества систем нашего организма, нарушения в работе которых представляют опасность для здоровья, свертывание крови также занимает абсолютное первое место как главная непосредственная причина смерти: люди болеют разными болезнями, но умирают почти всегда от нарушений свертывания крови. Рак, сепсис, травма, атеросклероз, инфаркт, инсульт — для широчайшего круга заболеваний непосредственной причиной смерти является неспособность системы свертывания поддерживать баланс между жидким и твердым состояниями крови в организме.
Если причина известна, почему же с ней нельзя бороться? Разумеется, бороться можно и нужно: ученые постоянно создают новые методы диагностики и терапии нарушений свертывания. Но проблема в том, что система свертывания очень сложна. А наука о регуляции сложных систем учит, что управлять такими системами нужно особым образом. Их реакция на внешнее воздействие нелинейна и непредсказуема, и для того, чтобы добиться нужного результата, нужно знать, куда приложить усилие. Простейшая аналогия: чтобы запустить в воздух бумажный самолетик, его достаточно бросить в нужную сторону; в то же время для взлета авиалайнера потребуется нажать в кабине пилота на правильные кнопки в нужное время и в нужной последовательности. А если попытаться авиалайнер запустить броском, как бумажный самолетик, то это закончится плохо. Так и с системой свертывания: чтобы успешно лечить, нужно знать «управляющие точки».
Вплоть до самого последнего времени свертывание крови успешно сопротивлялось попыткам исследователей понять его работу, и лишь в последние годы тут произошел качественный скачок. В данной статье мы расскажем об этой замечательной системе: как она устроена, почему ее так сложно изучать, и — самое главное — поведаем о последних открытиях в понимании того, как она работает.
Как устроено свертывание крови
Остановка кровотечения основана на той же идее, что используют домохозяйки для приготовления холодца — превращении жидкости в гель (коллоидную систему, где формируется сеть молекул, способная удержать в своих ячейках тысячекратно превосходящую ее по весу жидкость за счет водородных связей с молекулами воды). Кстати, та же идея используется в одноразовых детских подгузниках, в которые помещается разбухающий при смачивании материал. С физической точки зрения, там нужно решать ту же самую задачу, что и в свертывании — борьбу с протечками при минимальном приложении усилий.
Свертывание крови является центральным звеном гемостаза (остановки кровотечения). Вторым звеном гемостаза являются особые клетки — тромбоциты, — способные прикрепляться друг к другу и к месту повреждения, чтобы создать останавливающую кровь пробку.
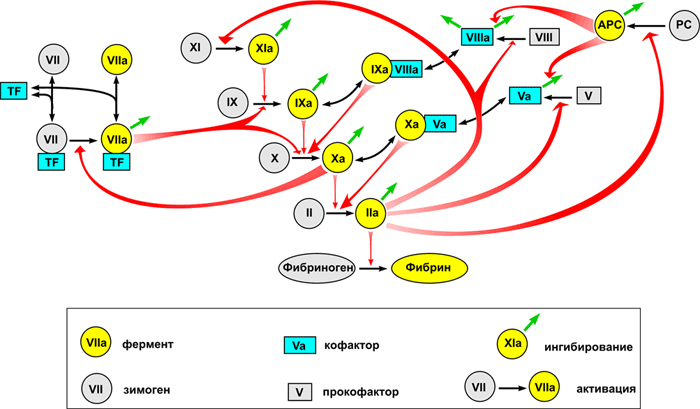
Общее представление о биохимии свертывания можно получить из рисунка 1, внизу которого показана реакция превращения растворимого белка фибриногена в фибрин, который затем полимеризуется в сетку. Эта реакция представляет собой единственную часть каскада, имеющую непосредственный физический смысл и решающую четкую физическую задачу. Роль остальных реакций — исключительно регуляторная: обеспечить превращение фибриногена в фибрин только в нужном месте и в нужное время.
Рисунок 1. Основные реакции свертывания крови. Система свертывания представляет собой каскад — последовательность реакций, где продукт каждой реакции выступает катализатором следующей. Главный «вход» в этот каскад находится в его средней части, на уровне факторов IX и X: белок тканевый фактор (обозначен на схеме как TF) связывает фактор VIIa, и получившийся ферментативный комплекс активирует факторы IX и X. Результатом работы каскада является белок фибрин, способный полимеризоваться и образовывать сгусток (гель). Подавляющее большинство реакций активации — это реакции протеолиза, т.е. частичного расщепления белка, увеличивающего его активность. Почти каждый фактор свертывания обязательно тем или иным образом ингибируется: обратная связь необходима для стабильной работы системы.
Обозначения: Реакции превращения факторов свертывания в активные формы показаны односторонними тонкими черными стрелками. При этом фигурные красные стрелки показывают, под действием каких именно ферментов происходит активация. Реакции потери активности в результате ингибирования показаны тонкими зелеными стрелками (для простоты стрелки изображены как просто «уход», т.е. не показано, с какими именно ингибиторами происходит связывание). Обратимые реакции формирования комплексов показаны двусторонними тонкими черными стрелками. Белки свертывания обозначены либо названиями, либо римскими цифрами, либо аббревиатурами (TF — тканевый фактор, PC — протеин С, APC — активированный протеин С). Чтобы избежать перегруженности, на схеме не показаны: связывание тромбина с тромбомодулином, активация и секреция тромбоцитов, контактная активация свертывания.
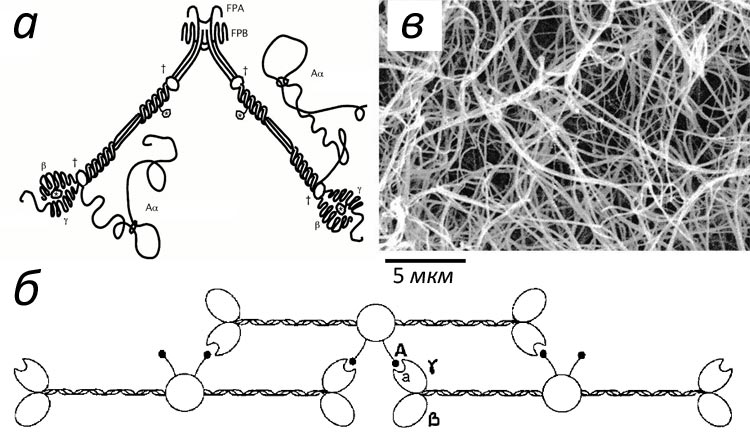
Фибриноген напоминает стержень длиной 50 нм и толщиной 5 нм (рис. 2а). Активация позволяет его молекулам склеиваться в фибриновую нить (рис 2б), а затем в волокно, способное ветвиться и образовывать трехмерную сеть (рис. 2в).
Рисунок 2. Фибриновый гель. а — Схематическое устройство молекулы фибриногена. Основа ее составлена из трех пар зеркально расположенных полипептидных цепей α, β, γ. В центре молекулы можно видеть области связывания, которые становятся доступными при отрезании тромбином фибринопептидов А и Б (FPA и FPB на рисунке). б — Механизм сборки фибринового волокна: молекулы крепятся друг к другу «внахлест» по принципу головка-к-серединке, образуя двухцепочечное волокно. в — Электронная микрофотография геля: фибриновые волокна могут склеиваться и расщепляться, образуя сложную трехмерную структуру.
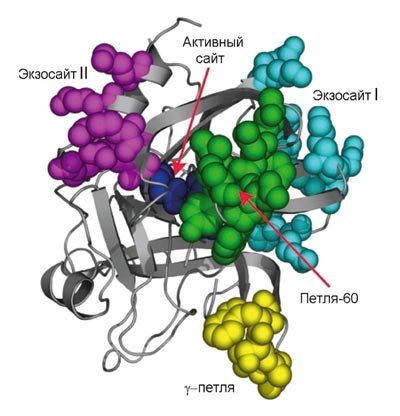
Рисунок 3. Трехмерная структура молекулы тромбина. На схеме показаны активный сайт и части молекулы, ответственные за связывание тромбина с субстратами и кофакторами. (Активный сайт — часть молекулы, непосредственно распознающее место расщепления и осуществляющее ферментативный катализ.) Выступающие части молекулы (экзосайты) позволяют осуществлять «переключение» молекулы тромбина, делая его мультифункциональным белком, способным работать в разных режимах. Например, связывание тромбомодулина с экзосайтом I физически перекрывает доступ к тромбину прокоагулянтным субстратам (фибриноген, фактор V) и аллостерически стимулирует активность по отношению к протеину C.
Активатор фибриногена тромбин (рис. 3) принадлежит к семейству сериновых протеиназ — ферментов, способных осуществлять расщепление пептидных связей в белках. Он является родственником пищеварительных ферментов трипсина и химотрипсина. Протеиназы синтезируются в неактивной форме, называемой зимогеном. Чтобы их активировать, необходимо расщепить пептидную связь, удерживающую часть белка, которая закрывает активный сайт. Так, тромбин синтезируется в виде протромбина, который может быть активирован. Как видно из рис. 1 (где протромбин обозначен как фактор II), это катализируется фактором Xa.
Вообще, белки свертывания называют факторами и нумеруют римскими цифрами в порядке официального открытия. Индекс «а» означает активную форму, а его отсутствие — неактивный предшественник. Для давно открытых белков, таких как фибрин и тромбин, используют и собственные имена. Некоторые номера (III, IV, VI) по историческим причинам не используются.
Активатором свертывания служит белок, называемый тканевым фактором, присутствующий в мембранах клеток всех тканей, за исключением эндотелия и крови. Таким образом, кровь остается жидкой только благодаря тому, что в норме она защищена тонкой защитной оболочкой эндотелия. При любом нарушении целостности сосуда тканевой фактор связывает из плазмы фактор VIIa, а их комплекс — называемый внешней теназой (tenase, или Xase, от слова ten — десять, т.е. номер активируемого фактора) — активирует фактор X.
Тромбин также активирует факторы V, VIII, XI, что ведет к ускорению его собственного производства: фактор XIa активирует фактор IX, а факторы VIIIa и Va связывают факторы IXa и Xa, соответственно, увеличивая их активность на порядки (комплекс факторов IXa и VIIIa называется внутренней теназой). Дефицит этих белков ведет к тяжелым нарушениям: так, отсутствие факторов VIII, IX или XI вызывает тяжелейшую болезнь гемофилию (знаменитую «царскую болезнь», которой болел царевич Алексей Романов); а дефицит факторов X, VII, V или протромбина несовместим с жизнью.
Такое устройство системы называется положительной обратной связью: тромбин активирует белки, которые ускоряют его собственное производство. И здесь возникает интересный вопрос, а зачем они нужны? Почему нельзя сразу сделать реакцию быстрой, почему природа делает ее исходно медленной, а потом придумывает способ ее дополнительного ускорения? Зачем в системе свертывания дублирование? Например, фактор X может активироваться как комплексом VIIa—TF (внешняя теназа), так и комплексом IXa—VIIIa (внутренняя теназа); это выглядит совершенно бессмысленным.
В крови также присутствуют ингибиторы протеиназ свертывания. Основными являются антитромбин III и ингибитор пути тканевого фактора. Кроме этого, тромбин способен активировать сериновую протеиназу протеин С, которая расщепляет факторы свертывания Va и VIIIa, заставляя их полностью терять свою активность.
Протеин С — предшественник сериновой протеиназы, очень похожей на факторы IX, X, VII и протромбин. Он активируется тромбином, как и фактор XI. Однако при активации получившаяся сериновая протеиназа использует свою ферментативную активность не для того, чтобы активировать другие белки, а для того, чтобы их инактивировать. Активированный протеин С производит несколько протеолитических расщеплений в факторах свертывания Va и VIIIa, заставляя их полностью терять свою кофакторную активность. Таким образом, тромбин — продукт каскада свертывания — ингибирует свое собственное производство: это называется отрицательной обратной связью. И опять у нас регуляторный вопрос: зачем тромбин одновременно ускоряет и замедляет собственную активацию?
Эволюционные истоки свертывания
Формирование защитных систем крови началось у многоклеточных свыше миллиарда лет назад — собственно, как раз в связи с появлением крови. Сама система свертывания является результатом преодоления другой исторической вехи — возникновения позвоночных около пятисот миллионов лет назад. Скорее всего, эта система возникла из иммунитета. Появление очередной системы иммунных реакций, которая боролась с бактериями путем обволакивания их фибриновым гелем, привело к случайному побочному результату: кровотечение стало прекращаться быстрее. Это позволило увеличивать давление и силу потоков в кровеносной системе, а улучшение сосудистой системы, то есть улучшение транспорта всех веществ, открыло новые горизонты развития. Кто знает, не было ли появление свертывания тем преимуществом, которое позволило позвоночным занять свое нынешнее место в биосфере Земли?
У ряда членистогих (таких, как рак-мечехвост) свертывание также существует, но оно возникло независимо и осталось на иммунологических ролях. Насекомые, как и прочие беспозвоночные, обычно обходятся более слабой разновидностью системы остановки кровотечения, основанной на агрегации тромбоцитов (точнее, амебоцитов — дальних родственников тромбоцитов). Этот механизм вполне функционален, но накладывает принципиальные ограничения на эффективность сосудистой системы, — так же, как трахейная форма дыхания ограничивает максимально возможный размер насекомого.
К сожалению, существа с промежуточными формами системы свертывания почти все вымерли. Единственным исключением являются бесчелюстные рыбы: геномный анализ системы свертывания у миноги показал, что она содержит гораздо меньше компонентов (то есть, устроена заметно проще) [6]. Начиная же с челюстных рыб и до млекопитающих системы свертывания очень похожи. Системы клеточного гемостаза также работают по схожим принципам, несмотря на то, что мелкие, безъядерные тромбоциты характерны только для млекопитающих. У остальных позвоночных тромбоциты — крупные клетки, имеющие ядро.
Подводя итог, система свертывания изучена очень хорошо. В ней уже пятнадцать лет не открывали новых белков или реакций, что для современной биохимии составляет вечность. Конечно, нельзя совсем исключить вероятность такого открытия, но пока что не существует ни одного явления, которое мы не могли бы объяснить при помощи имеющихся сведений. Скорее наоборот, система выглядит гораздо сложнее, чем нужно: мы напомним, что из всего этого (довольно громоздкого!) каскада собственно желированием занимается только одна реакция, а все остальные нужны для какой-то непонятной регуляции.
Именно поэтому сейчас исследователи-коагулологи, работающие в самых разных областях — от клинической гемостазиологии до математической биофизики, — активно переходят от вопроса «Как устроено свертывание?» к вопросам «Почему свертывание устроено именно так?», «Как оно работает?» и, наконец, «Как нам нужно воздействовать на свертывание, чтобы добиться желаемого эффекта?». Первое, что необходимо сделать для ответа — научиться исследовать свертывание целиком, а не только отдельные реакции.
Как исследовать свертывание?
Для изучения свертывания создаются различные модели — экспериментальные и математические. Что именно они позволяют получить?
С одной стороны, кажется, что самым лучшим приближением для изучения объекта является сам объект. В данном случае — человек или животное. Это позволяет учитывать все факторы, включая ток крови по сосудам, взаимодействия со стенками сосудов и многое другое. Однако в этом случае сложность задачи превосходит разумные границы. Модели свертывания позволяют упростить объект исследования, не упуская его существенных особенностей.
Попытаемся составить представление о том, каким требованиям должны отвечать эти модели, чтобы корректно отражать процесс свертывания in vivo.
В экспериментальной модели должны присутствовать те же биохимические реакции, что и в организме. Должны присутствовать не только белки системы свертывания, но и прочие участники процесса свертывания — клетки крови, эндотелия и субэндотелия. Система должна учитывать пространственную неоднородность свертывания in vivo: активацию от поврежденного участка эндотелия, распространение активных факторов, присутствие тока крови.
Рассмотрение моделей свертывания естественно начать с методов исследования свертывания in vivo. Основа практически всех используемых подходов такого рода заключается в нанесении подопытному животному контролируемого повреждения с тем, чтобы вызвать гемостатическую или тромботическую реакцию. Данная реакция исследуется различными методами:
Рисунок 4. Формирование тромба in vivo в модели тромбоза, индуцированного лазером. Эта картинка воспроизведена из исторической работы, где ученые впервые смогли пронаблюдать развитие тромба «вживую». Для этого в кровь мыши впрыснули концентрат флуоресцентно меченных антител к белкам свертывания и тромбоцитам, и, поместив животное под объектив конфокального микроскопа (позволяющего осуществлять трехмерное сканирование), выбрали доступную для оптического наблюдения артериолу под кожей и повредили эндотелий лазером. Антитела начали присоединяться к растущему тромбу, сделав возможным его наблюдение.
Классическая постановка эксперимента по свертыванию in vitro заключается в том, что плазма крови (или цельная кровь) смешивается в некоторой емкости с активатором, после чего производится наблюдение за процессом свертывания. По методу наблюдения экспериментальные методики можно разделить на следующие типы:
Второй подход дает несравненно больше информации. Теоретически, зная концентрации всех факторов в произвольный момент времени, можно получить полную информацию о системе. На практике исследование даже двух белков одновременно дорого и связано с большими техническими трудностями.
Наконец, свертывание в организме протекает неоднородно. Формирование сгустка запускается на поврежденной стенке, распространяется с участием активированных тромбоцитов в объеме плазмы, останавливается с помощью эндотелия сосудов. Адекватно изучить эти процессы с помощью классических методов невозможно. Вторым важным фактором является наличие потока крови в сосудах.
Осознание этих проблем привело к появлению, начиная с 1970-х годов, разнообразных проточных экспериментальных систем in vitro. Несколько больше времени потребовалось на осознание пространственных аспектов проблемы. Только в 1990-е годы стали появляться методы, учитывающие пространственную неоднородность и диффузию факторов свертывания, и только в последнее десятилетие они стали активно использоваться в научных лабораториях (рис. 5).
Рисунок 5. Пространственный рост фибринового сгустка в норме и патологии. Свертывание в тонком слое плазмы крови активировалось иммобилизованным на стенке тканевым фактором. На фотографиях активатор расположен слева. Серая расширяющаяся полоса — растущий фибриновый сгусток.
Наряду с экспериментальными подходами для исследований гемостаза и тромбоза также используются математические модели (этот метод исследований часто называется in silico [8]). Математическое моделирование в биологии позволяет устанавливать глубокие и сложные взаимосвязи между биологической теорией и опытом. Проведение эксперимента имеет определенные границы и сопряжено с рядом трудностей. Кроме того, некоторые теоретически возможные эксперименты неосуществимы или запредельно дороги вследствие ограничений экспериментальной техники. Моделирование упрощает проведение экспериментов, так как можно заранее подобрать необходимые условия для экспериментов in vitro и in vivo, при которых интересующий эффект будет наблюдаем.
Регуляция системы свертывания
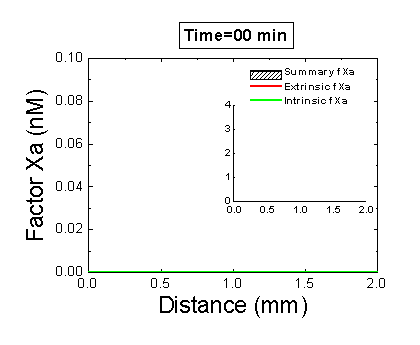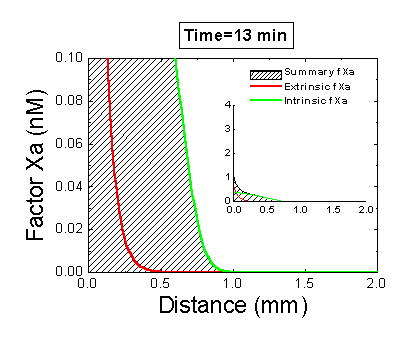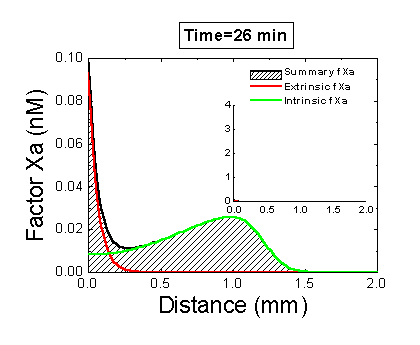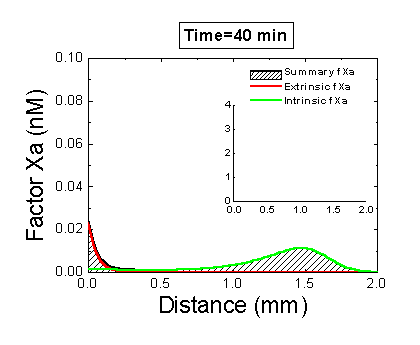
Рисунок 6. Вклад внешней и внутренней теназы в формирование фибринового сгустка в пространстве. Мы использовали математическую модель, чтобы исследовать, как далеко может простираться влияние активатора свертывания (тканевого фактора) в пространстве. Для этого мы посчитали распределение фактора Xa (который определяет распределение тромбина, который определяет распределение фибрина). На анимации показаны распределения фактора Xa, произведенного внешней теназой (комплексом VIIa–TF) или внутренней теназой (комплексом IXa–VIIIa), а также общее количество фактора Xa (заштрихованная область). (Вставка показывает то же самое на более крупной шкале концентраций.) Можно видеть, что произведенный на активаторе фактор Xa не может проникнуть далеко от активатора из-за высокой скорости ингибирования в плазме. Напротив, комплекс IXa–VIIIa работает вдали от активатора (т.к. фактор IXa медленнее ингибируется и потому имеет большее расстояние эффективной диффузии от активатора), и обеспечивает распространение фактора Xa в пространстве.
Сделаем следующий логический шаг и попробуем ответить на вопрос — а как описанная выше система работает?
Каскадное устройство системы свертывания
Запуск свертывания и роль положительных обратных связей
Как упоминалось в первой части статьи, многие реакции свертывания медленны. Так, факторы IXa и Xa сами по себе являются очень плохими ферментами и для эффективного функционирования нуждаются в кофакторах (факторах VIIIa и Va, соответственно). Эти кофакторы активируются тромбином: такое устройство, когда фермент активирует собственное производство, называется петлей положительной обратной связи.
Как было показано нами экспериментально и теоретически, положительная обратная связь активации фактора V тромбином формирует порог по активации — свойство системы не реагировать на малую активацию, но быстро срабатывать при появлении большой. Подобное умение переключаться представляется весьма ценным для свертывания: это позволяет предотвратить «ложное срабатывание» системы.
Роль внутреннего пути в пространственной динамике свертывания
Одной из интригующих загадок, преследовавших биохимиков на протяжении многих лет после открытия основных белков свертывания, была роль фактора XII в гемостазе. Его дефицит обнаруживался в простейших тестах свертывания, увеличивая время, необходимое для образования сгустка, однако, в отличие от дефицита фактора XI, не сопровождался нарушениями свертывания.
Один из наиболее правдоподобных вариантов разгадки роли внутреннего пути был предложен нами с помощью пространственно неоднородных экспериментальных систем. Было обнаружено, что положительные обратные связи имеют большое значение именно для распространения свертывания. Эффективная активация фактора X внешней теназой на активаторе не поможет сформировать сгусток вдали от активатора, так как фактор Xa быстро ингибируется в плазме и не может далеко отойти от активатора. Зато фактор IXa, который ингибируется на порядок медленнее, вполне на это способен (и ему помогает фактор VIIIa, который активируется тромбином). А там, куда сложно дойти и ему, начинает работать фактор XI, также активируемый тромбином. Таким образом, наличие петель положительных обратных связей помогает создать трехмерную структуру сгустка.
Путь протеина С как возможный механизм локализации тромбообразования
Активация протеина С тромбином сама по себе медленна, но резко ускоряется при связывании тромбина с трансмембранным белком тромбомодулином, синтезируемым клетками эндотелия. Активированный протеин С способен разрушать факторы Va и VIIIa, на порядки замедляя работу системы свертывания. Ключом к пониманию роли данной реакции стали пространственно-неоднородные экспериментальные подходы. Наши эксперименты позволили предположить, что она останавливает пространственный рост тромба, ограничивая его размер.
Подведение итогов
В последние годы сложность системы свертывания постепенно становится менее загадочной. Открытие всех существенных компонентов системы, разработка математических моделей и использование новых экспериментальных подходов позволили приоткрыть завесу тайны. Структура каскада свертывания расшифровывается, и сейчас, как мы видели выше, практически для каждой существенной части системы выявлена или предложена роль, которую она играет в регуляции всего процесса.
На рисунке 7 представлена наиболее современная попытка пересмотреть структуру системы свертывания. Это та же схема, что и на рис. 1, где разноцветным затенением выделены части системы, отвечающие за разные задачи, как обсуждалось выше. Не все в этой схеме является надежно установленным. Например, наше теоретическое предсказание, что активация фактора VII фактором Xa позволяет свертыванию пороговым образом отвечать на скорость потока, остается пока еще непроверенным в эксперименте.
Рисунок 7. Модульная структура системы свертывания: роль отдельных реакций свертывания в функционировании системы.
Вполне возможно, что эта картина еще не вполне полна. Тем не менее, прогресс в этой области в последние годы вселяет надежду, что в обозримом будущем оставшиеся неразгаданные участки на схеме свертывания обретут осмысленную физиологическую функцию. И тогда можно будет говорить о рождении новой концепции свертывания крови, пришедшей на смену старинной каскадной модели, которая верно служила медицине на протяжении многих десятилетий.
Статья написана при участии А.Н. Баландиной и Ф.И. Атауллаханова и была в первоначальном варианте опубликована в «Природе» [10].

 Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии
Беседа с академиком А.Д. Макацария, крупнейшим специалистом в области клинической гемостазиологии