жидкий стул при лучевой терапии что делать
Радиационный гастроэнтерит и колит (K52.0)
Версия: Справочник заболеваний MedElement
Общая информация
Краткое описание
Автоматизация клиники: быстро и недорого!
— Подключено 300 клиник из 4 стран
Автоматизация клиники: быстро и недорого!
Мне интересно! Свяжитесь со мной
Классификация
Классификация лучевых повреждений кишечника (Бардычев М.С., Цыб А.Ф.)
1. По срокам:
— ранние;
— поздние.
2. По локализации:
— ректиты;
— ректосигмоидиты;
— энтероколиты.
3. По характеру патологического процесса:
— катаральные;
— эрозивно-десквамативные;
— инфильтративно-язвенные;
— некрозы стенки кишки.
4. Осложненные формы:
— ректовагинальные, ректовезикальные свищи;
— рубцовые стенозы кишки.
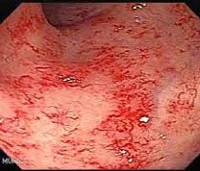
Виды радиационных поражений слизистой прямой кишки вследствие лучевой терапии рака шейки матки:
Этиология и патогенез
Лучевое поражение кишечника наиболее часто встречается у больных, подвергающихся лучевой терапии при опухолях малого таза (матки, цервикального канала, предстательной железы, яичек, прямой кишки, мочевого пузыря) или лимфатических узлов.
Эпидемиология
Признак распространенности: Редко
Почти все пациенты с радиационным энтеритом и колитом являются лицами, получавшими лучевую терапию по медицинским показаниям.
Факторы и группы риска
Дополнительные к основным факторы риска:
— гипертензия;
— воспалительные заболевания органов малого таза;
— сахарный диабет;
— сопутствующая химиотерапия;
— астеническое телосложение;
— наличие в анамнезе хирургических вмешательств на органах брюшной полости или малого таза.
Клиническая картина
Клинические критерии диагностики
Cимптомы, течение
Ранее лучевое поражение кишечника
Развивается в течение первых 3 месяцев после облучения. Клинические проявления неспецифичны и могут напоминать другие воспалительные заболевания тонкой и толстой кишок. Ранее лучевое повреждение может пройти бесследно.
В процессе проведения лучевой терапии или после ее завершения возможны следующие проявления:
— тошнота;
— рвота;
— снижение аппетита;
— похудание;
— диарея и боли в животе.
Выраженность симптомов зависит от суммарной дозы облучения, распространенности и локализации патологического процесса.
Позднее лучевое поражение кишечника
Развивается в течение 4-12 месяцев после лучевой терапии.
Первые признаки:
— упорные запоры или частый жидкий стул с ложными позывами;
— боли в животе различной интенсивности;
— снижение аппетита, постоянная тошнота (у основной массы больных присутствует дефицит массы тела).
При катаральных формах лучевых повреждений кишечника в кале присутствует примесь слизи.
При эрозивно-десквамативных и язвенно-некротических изменениях пораженных участков кишки в кишечном отделяемом присутствует кровь. Максимальная интенсивность кровопотери (массивные кишечные кровотечения) отмечается у пациентов с язвенно-некротическим энтероколитом.
Вследствие профузного кровотечения или длительно выявляемой примеси крови в кале, у больных развивается железодефицитная анемия (нередко тяжелой степени).
Клиническая картина хронического радиационного колита и проктита:
— язвенно-деструктивные изменения слизистой оболочки;
— проявления избыточного бактериального роста.
Диагностика
Рентгенодиагностика
Диагностика лучевого энтерита, помимо анамнеза, включает полную и последовательную визуализацию верхнего отдела желудочно-кишечного тракта. С помощью рентгеноскопии желудка с досмотром тонкой кишки или энтерографии оценивают протяженность поражения и определяют наличие стриктур или свищей.
КТ брюшной полости позволяет исключить метастазы опухолей, по поводу которых проводилась лучевая терапия, абсцессы и скопление жидкости в брюшной полости.
Лабораторная диагностика
Дифференциальный диагноз
Осложнения
Приблизительно у трети пациентов осложнения требуют хирургического лечения.
Лечение
Консервативное лечение
1. Питание:
1.1 Медикаментозная терапия тяжелого хронического радиационного энтерита основывается на полном парентеральном питании, особенно при наличии протяженной стриктуры и синдрома короткой кишки.
1.2 При переходе к обычному питанию, рекомендуется диета аналогичная таковой при неспецифическом язвенном колите. Из рациона рекомендуется исключить молоко и молочные продукты (кроме йогурта, сыра, пахты), хлеб с отрубями и злаки, орехи (в том числе кокосы), сухофрукты, семечки, жареные или жирные продукты, свежие фрукты и сырые овощи, жареную кукурузу, чипсы, специи, шоколад, кофе, чай, газированные напитки, а также напитки, содержащие кофеин или алкоголь.
1.3 Необходимо принимать не менее трех литров жидкости в день.
2. Медикаментозное лечение
2. 1 Симптоматическая терапия:
2.1.1 Для устранения диареи, вызванной желчными солями, назначают холестирамин; для уменьшения частоты стула и улучшения всасывания желчных кислот применяется лоперамид.
Прогноз
Острое радиационное поражение кишки полностью обратимо (макроскопически и гистологически) без специального лечения. Поражения кишки могут регенерировать, несмотря на продолжающееся облучение. Если повреждения достаточно выражены, необходимо прекратить лечение, по крайней мере на некоторое время.
При хроническом радиационном проктите у 70% пациентов заболевание протекает умеренно, без потребности в переливании крови, у 5% наблюдается тяжелое течение с развитием осложнений.
Лучевой энтерит с атрофическими и эрозивно-язвенными изменениями слизистой оболочки тонкой кишки ведет к потере трудоспособности и является прогностически неблагоприятным. Прогрессирующее течение радиационного энтерита, требующее хирургического вмешательства, наблюдается у трети пациентов.
Осложнения противоопухолевой терапии на желудочно-кишечный тракт
В данной статье рассматриваются следующие осложнения противоопухолевого лечения со стороны желудочно-кишечного тракта:
Снижение массы тела (недостаточность питания)
Снижение массы тела у онкологического пациента возникает вследствие многих факторов: необходимо учитывать лечение пациента сейчас и в прошлом, состояние больного, объем операционных вмешательств и т.д.
Причины потери массы тела:
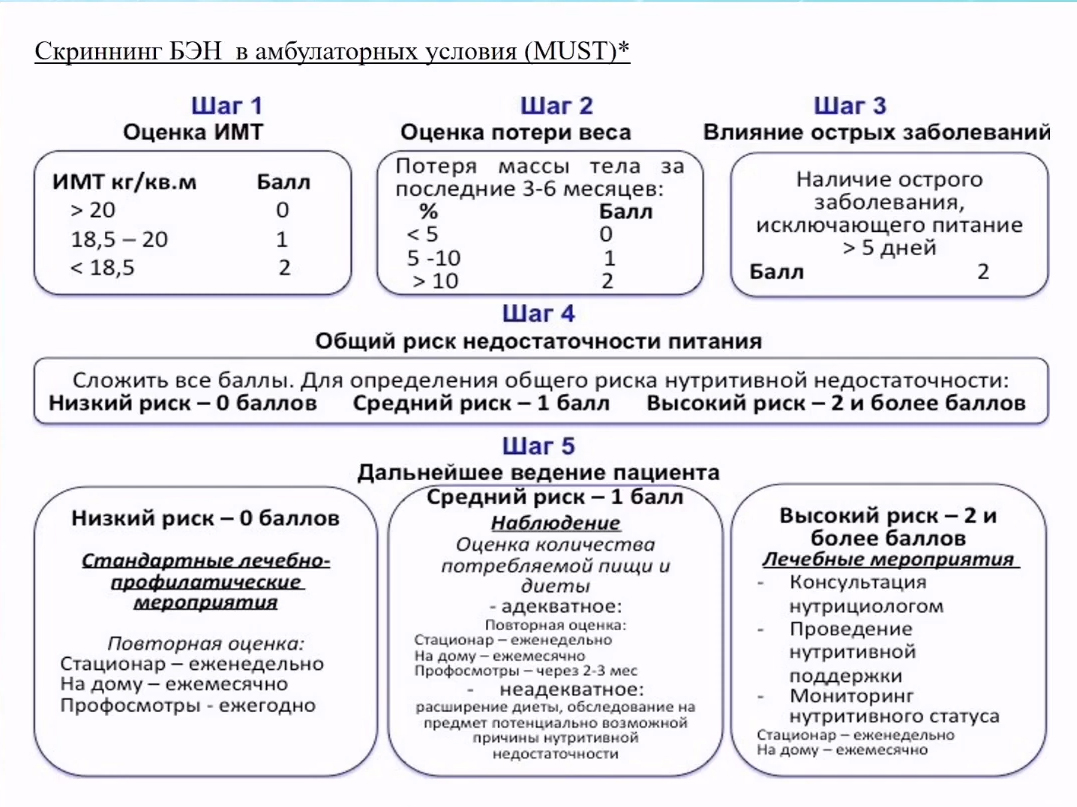
Оценка недостаточности питания
В амбулаторной практике используются различные шкалы для оценки недостаточности питания.
Оценка ситуации должна включать в себя как минимум следующие вопросы:
Алгоритм назначения нутриционной поддержки
Данный алгоритм должен разрабатываться совместно со специалистом, поскольку пациент не может самостоятельно подобрать для себя адекватную терапию, которая поспособствует улучшению самочувствия и облегчению симптоматики.
Для алгоритма назначения нутриционной поддержки необходимо ответить на следующие вопросы:
Для расчета энергетических потребностей пациента необходимо оценить имеющуюся недостаточность питания, риски прогрессирования недостаточности питания.
Осуществляется выбор оптимального пути введения лечебного питания. Возможны следующие варианты: сиппинг (лечебное питание, которое пациент может употреблять самостоятельно), зондовое питание, комбинированная нутриционовая поддержка (совмещение парентерального и энтерального питания). Отдельно стоит рассматривать ситуации, когда у пациента есть стома (гастростома, энтеростома, эзофагостома): в этом случае введение препаратов лечебного питания может осуществляться через нее.
Определяется режим кормления, режим введения препаратов лечебного питания.
Определяются сроки нутриционной поддержки пациента.
Осуществляется выбор препаратов для конкретной ситуации.
Методы оценки эффективности проводимой нутриционной поддержки
Эти методы часто используются в рутинной практике. Они позволяют оценить изменение состава тела на фоне нутриционной поддержки, оценить объем жировой массы, внеклеточной и внутриклеточной жидкости, косвенно оценить количество мышечной массы.
Эти методы редко используются в рутинной практике. Однако их достоинство в доступности – врач может осуществить оценку состояния тела прямо во время приема.
Пострезекционные синдромы
Синдромы оперированного желудка
К ним относятся – депминг-синдром, гипогликемический синдром, анемический синдром, синдром приводящей петли, рефлюкс-эзофагит, недостаточность питания, моторные нарушения культи желудка, анастомоза.
Чаще всего с этими синдромами сталкиваются пациенты, которые перенесли операции на желудке, пищеводе или поджелудочной железе. Данные симптомы могут развиваться, как в раннем, так и в более отсроченном периоде.
Демпинг-синдром. Как правило, проявляется слабостью, потливостью после приема пищи, головокружением, зачастую возникает при приеме углеводистой пищи. Развивается, как в раннем, так и в позднем послеоперационном периоде. Синдром обусловлен быстрой эвакуацией пищи из пищевода в тонкую кишку с последующим развитием гипергликемии, то есть пища быстро попадает из пищевода в тонкую кишку, что вызывает повышение уровня глюкозы (сахара) в крови.
Обычно регулируется подбором режима питания и рациона, а также медикаментозными препаратами.
Пациентам, страдающим демпинг-синдромом, необходимо вести пищевой дневник. Это поможет отследить причины синдрома (определенное время суток, определенная еда и т.д.).
Гипогликемический синдром. Проявляется недостаточным уровнем сахара в крови. Является разновидностью позднего демпинг-синдрома.
Анемия. Обусловлена дефицитом железа и витамина В-12 после удаления желудка. Данное состояние необходимо корректировать и компенсировать препаратами.
Рефлюкс-эзофагит. Это заброс пищи из тонкой кишки в пищевод. Самыми частыми проявлениями рефлюкс-эзофагита является изжога, горечь во рту, тяжесть после приема пищи, ощущение жжения по ходу пищевода. Реже симптом проявляется жжением в области языка, кислым привкусом во рту. Корректируется режимом питания, новыми жизненными привычками и назначением медикаментозной терапии.
Недостаточность питания или потеря массы тела. Данный синдром требует коррекции рациона и режима питания, а также назначения дополнительной нутриционной поддержки.
Важно знать, сколько массы пациент потерял до операции, после операции, во время химио/лучевой терапии. Исходя из этого подбираются препараты лечебного питания.
Нарушение культи желудка, анастомоза (т.е. места соединения органов). Осложнение, которое относится к моторно-эвакуаторным нарушениям. Корректируется медикаментозно.
Болевой синдром. Может быть обусловлен разными факторами. При обращении к врачу важно описать, когда возникают боли, связаны ли они с приемом пищи, через какое время и в каком месте после приема пищи возникают, проходят самостоятельно или требуют применения препаратов, сопровождаются ли тошнотой, рвотой, нарушением стула.
Астения. Состояние общей слабости и утомляемости.
Эти и другие симптомы, которые могут беспокоить пациента в послеоперационном периоде или на фоне проводимого лечения. Любые жалобы требуют обращения к врачу.
Диагностика синдромов оперированного желудка
Обследования позволяют подобрать терапию, дать точные рекомендации по образу жизни.
Как установить причину рефлюкса (заброса пищи обратно в пищевод)?
В сложных случаях для оценки характера рефлюктата и оценки того, что именно забрасывается в пищевод, используется суточная импеданс-pH-метрия. Данное исследование особенно актуально для пациентов, которые перенесли гастрэктомию (удаление желудка), резекцию пищевода.
Обследование выполняется в тех клинических ситуациях, когда пациент получает медикаментозное лечение, но улучшения не наблюдаются. Либо, когда жалобы не соответствуют характеру проведенного оперативного вмешательства.
Консервативная терапия после оперативного вмешательства на желудке
Последствия оперативного вмешательства на поджелудочной железе
Хирургические вмешательства на поджелудочной железе зачастую влекут за собой недостаточность выработки ряда ферментов и гормонов в организме. Нехватка данных веществ может привести к потере массы тела, вторичному диабету, диарее, синдрому избыточного бактериального роста. Вторичной проблемой становится боль в животе.
Чтобы оценить недостаточность ферментов проводится анализ кала на панкреатическую эластазу.
Основное лечение патологии заключается в заместительной ферментативной терапии, подбор питания.
Нарушение стула на фоне лечения (диарея/запор)
Диарея
Основные факторы, которые вызывают диарею (в зависимости от них подбирается терапия):
Любой из вышеперечисленных симптомов требует обращения к врачу для назначения терапии.
Если на фоне диареи, у пациента отмечается подъемы температуры, интоксикация, то необходимо дополнительное обследование на псевдомембранозный колит.
Диарея и недержание кала
После операций на органах, расположенных в малом тазу, у пациента может наблюдаться комбинация сразу двух синдромов – диареи и недержания кала. Чаще всего данное расстройство наблюдается у пациентов гинекологического профиля.
У больного может наблюдаться неоформленный или полуоформленный стул, а также фрагментная дефекация в течение дня, трудности с удержанием кала и газов после возникновения позывов на дефекацию. Иногда бывает ночное недержание кала.
Чтобы оценить состояние анального сфинктера специалисты назначают сфинктерометрию.
При лечении патологии применяется комбинация методов – лекарственная терапия, физиотерапия, физические упражнения.
Запор / задержка стула
Симптом может сопровождаться такими жалобами, как напряжение и/или боли в животе, натуживание, вздутие живота, твердый кал, ощущение неполного опорожнения кишечника, необходимость ручного пособия при опорожнении, отсутствие позывов на дефекацию или ложные позывы на дефекацию без опорожнения кишечника.
Причинами запора/задержки стула могут послужить:
Если пациент наблюдает у себя запор или задержку стула, необходима консультация специалиста.
Методы диагностики, которые помогут установить причину запоров:
Если на фоне лечения задержка стула длится от 4 суток, а также отмечаются повышенное газообразование, тошнота и/или рвота, боли в кишечнике, то необходима срочная консультация специалиста!
Терапия запора/задержки стула
Традиционным методом лечения является медикаментозная терапия. В случае спаечного процесса может потребоваться хирургическое лечение.
Отметим, что противоболевая терапия может усугубить ситуацию.
Лучевые поражения кишечника
Лучевые поражения кишечника проявляются в виде колитов – воспалительного заболевания слизистой оболочки кишечника. Колиты преимущественно развиваются у пациентов, получающих терапию на область малого таза (матка, цервикальный канал, простата, прямая кишка, мочевой пузырь).
Колиты могут возникнуть на любом этапе лечения: во время начала лучевой терапии и в течении 3 месяцев после окончания лечения. Существуют и позднеотстроченные лучевые колиты, которые возникают в течение первого года после проведенной лучевой терапии.
Симптомы
К основным симптомам лучевого поражения кишечника относят: нарушение стула, диарея, ложные позывы к дефекации, боли по ходу кишечника и боли в заднем проходе, в зависимости от зоны, куда пациент получает лучевую терапию. При достаточно выраженном воспалении появляются следующие симптомы — недержание кала и газов, диспепсия, метеоризм, рвота, тошнота, снижение массы тела на фоне диареи.
Если в начале лучевой терапии, во время нее, после нее у пациента отмечается выделение крови с каловыми массами – стоит немедленно обратиться к врачу! Он назначит необходимые обследования и лечение.
Диагностика лучевых поражений кишечника
Исследования, которые позволяют определить степень поражения и назначить терапию:
Терапия
При лучевых поражениях желудочно-кишечного тракта терапия зависит от локализации патологического процесса. В основном используются:
Срок лечения определяется специалистом. Стоит отметить, что лучевой колит невозможно вылечить за 2-3 недели, терапия должна быть длительной и систематической.
Авторская статья:
Захарова П.А.
Гастроэнтеролог, гепатолог НМИЦ онкологии им. Н.Н. Петрова
Лучевой энтероколит
Лучевой энтероколит — это воспалительное поражение кишечника, связанное с радиационными воздействиями. Проявляется диареей, запорами, другими диспепсическими явлениями, патологическими примесями в кале, болями в животе, снижением веса, астенией. Диагностируется с помощью рентгеноконтрастного исследования тонкой, толстой кишки, колоноскопии, копрограммы, дыхательных тестов. Для лечения используют кортикостероиды, препараты 5-АМК, прокинетики, ингибиторы опиатных рецепторов, анионообменные смолы, антибиотики, пробиотики, ферментные средства, регенеранты в сочетании с диетотерапией. Оперативное лечение проводится при возникновении хирургических осложнений.
МКБ-10
Общие сведения
Впервые характерные изменения кишечника после проведенной радиотерапии злокачественного новообразования были описаны в 1917 г. К.Францем и Дж.Ортом. По мере расширения показаний к проведению лучевой терапии, как радикального и паллиативного метода лечения онкологических заболеваний, совершенствования применяемых методик, число пациентов, получающих радиотерапию, увеличилось до 60% всех онкобольных. По результатам наблюдений специалистов в сфере практической проктологии, гастроэнтерологии и онкологии, у 3-17% больных, получивших радиационную нагрузку, развиваются ранние (острые) и поздние (хронические) формы лучевого энтероколита. Неятрогенное повреждение кишечника ионизирующими излучениями в настоящее время фиксируется крайне редко.
Причины лучевого энтероколита
Пострадиационное воспаление кишечника обычно развивается у пациентов, принимающих радиотерапию по поводу злокачественных новообразований брюшной полости, забрюшинного пространства, малого таза. Прямое повреждающее воздействие на различные участки тонкой и толстой кишки возникает вследствие лучевого лечения рака желудка, поджелудочной железы, шейки матки, яичников, предстательной железы, яичек, мочевого пузыря, прямой кишки, почечных карцином, опухолей надпочечников, ретроперитонеальных лимфом и пораженных метастазами лимфоузлов. Радиационная толерантность тонкого кишечника достигает 35 Гр, толстого — 40 Гр. При более высокой лучевой нагрузке наступают отсроченные патологические изменения. Острая обратимая реакция в процессе терапии ионизирующим излучением может развиться и при меньших дозах.
Вероятность возникновения радиационного энтероколита повышается при наличии воспалительных заболеваний кишечника, послеоперационных спаек, ограничивающих подвижность петель тонкой кишки, у лиц пожилого возраста, пациентов, которым назначена химиотерапия. Дополнительными факторами риска являются сопутствующие заболевания (артериальная гипертензия, сахарный диабет), астеническое телосложение, использование устаревшей радиационной техники, неправильный расчет лучевой нагрузки, несоблюдение техники облучения. Развитие клиники радиационного энтероколита возможно в рамках острой лучевой болезни при равномерном внешнем облучении дозой более 20 Гр во время ядерных катастроф, при халатном отношении к технике безопасности во время работы с источниками ионизирующих излучений.
Патогенез
Механизм развития лучевого энтероколита зависит от времени возникновения заболевания. Раннее радиационное поражение, возникающее непосредственно в процессе радиотерапии или в течение первых трех месяцев после курса лечения, основано на цитотоксическом действии ионизирующего излучения. Десквамация, преходящая атрофия, гибель энтероцитов и колоноцитов сочетаются с неспецифической воспалительной реакцией. Укорочение ворсинок, отек, гиперемия, выраженная нейтрофильная инфильтрация собственной пластинки кишки нарушают пристеночное пищеварение, процессы расщепления нутриентов, всасывания воды, усиливают или угнетают перистальтику кишечника. Благодаря быстрому делению оставшихся эпителиальных клеток слизистая кишки полностью восстанавливается, явления энтероколита купируются.
При сверхвысоких дозах лучевой нагрузки развиваются стойкие поздние поражения, обусловленные патоморфологическими изменениями мелких подслизистых сосудов. Нарушение кровообращения в кишечной стенке, вызванное микротромбированием и гиалинозом артериол, приводит к развитию хронической ишемии и связанной с ней гипорегенераторной атрофии кишечных эпителиоцитов. При значительном истончении слизистой уплощается ее рельеф, повышается кишечная проницаемость, замедляется моторика, нарушается абсорбция основных питательных веществ, желчных кислот, возникают участки язв и эрозий, в тяжелых случаях происходит некротическая деструкция. Ситуацию усугубляет гипоксический реактивный фиброз мышечного слоя, осложняющийся рубцовым стенозированием просвета кишечника.
Классификация
Систематизация форм лучевого энтероколита учитывает время возникновения расстройства, выраженность и локализацию патоморфологических изменений кишечной стенки. Такой подход позволяет более точно спрогнозировать исход и подобрать адекватное лечение. Выделяют следующие варианты лучевого повреждения кишечника:
Симптомы лучевого энтероколита
Клиническая картина острой формы заболевания сходна с признаками кишечного воспаления инфекционной этиологии. У пациентов наблюдается тошнота и рвота, потеря аппетита, учащенный стул с примесями слизи, боли в животе различной локализации. Значительное нарушение всасывания жиров проявляется выделением зловонных каловых масс светлого цвета с жирным блеском. При прогрессировании лучевой воспалительной реакции боли усиливаются, могут присоединяться ложные болезненные позывы к дефекации, в кале появляется кровь. Поздние радиационные энтероколиты характеризуются дискомфортом и умеренными болями в левой подвздошной области, других участках живота, чередованием запоров и диареи, потерей массы тела. Отмечаются нарушения общего состояния — головные боли, головокружения, слабость, снижение трудоспособности.
Осложнения
При язвенно-некротическом варианте лучевого энтероколита возникают потери крови с калом, которые со временем провоцируют формирование тяжелой железодефицитной анемии. Иногда развиваются профузные кровотечения, представляющие опасность для жизни больного. При лучевом энтероколите может происходить некроз всех слоев кишечной стенки, что приводит к перфорации и развитию местного или разлитого перитонита.
В случае хронического течения заболевания формируются рубцовые стриктуры, которые могут осложняться динамической или механической кишечной непроходимостью. Нарушение всасывания витаминов группы В сопровождается возникновением В12-дефицитной анемии, периферической полинейропатии. Ретиноловая недостаточность проявляется нарушением сумеречного зрения, слепотой, сухостью кожи и слизистых. При значительном недостатке эргокальциферола возможны остеопороз, кариес.
Диагностика
Постановка диагноза лучевого энтероколита не представляет затруднений при наличии в анамнезе сведений о радиационных воздействиях. Диагностический поиск направлен на тщательное обследование органов пищеварения с целью исключения других причин поражения кишечника. Наиболее информативными являются следующие инструментальные и лабораторные исследования:
При хроническом воспалении с помощью мезентериальной ангиографии определяется поражение артериол, приводящее к ишемии. Для исключения других возможных причин энтероколита (непереносимости лактозы, СИБР) применяют функциональные Н2-дыхательные тесты. Для лучевого энтероколитического синдрома типично снижение количества гемоглобина и эритроцитов, микроцитоз, уменьшение содержания ретикулоцитов в клиническом анализе крови.
Дифференциальная диагностика проводится с воспалительными заболеваниями кишечника (терминальным илеитом, неспецифическим язвенным колитом), энтероколитами вирусной или бактериальной этиологии, амебиазом, целиакией, спру, первичной лактазной недостаточностью, синдромом избыточного бактериального роста (СИБР), злокачественными новообразованиями пищеварительного тракта. Кроме наблюдения у врача-проктолога или гастроэнтеролога, пациенту может потребоваться консультация онколога, радиолога, инфекциониста, гематолога, общего хирурга.
Лечение лучевого энтероколита
Терапевтическая тактика в целом напоминает схему ведения пациентов с болезнью Крона, язвенным колитом. Независимо от варианта энтероколитического лучевого синдрома, проводится коррекция питания. Больным рекомендован рацион с высоким содержанием белка (100-120 г/сут.), достаточным количеством углеводов, жиров, макро- и микроэлементов, витаминов. При тяжело протекающих поздних энтероколитах возможен перевод пациента на энтерально-зондовое и парентеральное питание. При умеренно выраженной симптоматике достаточным оказывается симптоматическое лечение. Пострадиационную диарею эффективно купируют анионообменные смолы и блокаторы опиоидных рецепторов.
Для стимуляции моторики применяют прокинетики, которые для редукции возросшего количества микроорганизмов комбинируют с нитроимидазолами и тетрациклинами. Слабительные могут назначаться при отсутствии кишечной обструкции. Чтобы стимулировать восстановление эпителия, используют нестероидные анаболики, регенеранты и репаранты. Назначение антагонистов H2-рецепторов или ингибиторов протонной помпы позволяет ускорить заживление участков с эрозиями и язвами. При нарушении процессов пищеварения показаны ферментные препараты. Для профилактика возможного дисбиоза используются пробиотики. При среднетяжелом и тяжелом течении оправдано проведение патогенетической медикаментозной терапии, включающей:
Терапевтическую резистентность тяжелого энтероколита позволяет снизить проведение гипербарической оксигенации. До 20-30% пациентов с поздним радиационным воспалением, выраженными стриктурами и стенозом нуждаются в оперативном лечении. В зависимости от ситуации проводятся сегментарная резекция тонкой кишки, энтероэнтеростомия, энтероколостомия, энтеростомия (еюностомия или илеостомия), резекции ободочной кишки, стомирование толстого кишечника, наложение различных типов толстокишечных анастомозов.
Прогноз и профилактика
У большинства больных с острым воспалением наблюдается полное выздоровление с восстановлением целостности слизистой оболочки. У 70-80% пациентов с хроническим процессом удается добиться стойкой клинической ремиссии консервативными методами. Прогностически неблагоприятной является язвенно-некротическая форма лучевого энтероколита, которая может приводить к серьезным осложнениям и ограничению трудоспособности пациентов. Профилактика радиационных поражений кишечника заключается в индивидуальном подборе курсовой и разовой дозы облучения, соблюдении перерывов между сеансами лучевой терапии, применении радиопротекторов.