Зонд у новорожденных что
Зонд у новорожденных что
Определения:
1. Энтеральное питание определяют как доставку питательных веществ дистальнее ротовой полости.
2. Желудочный зонд — зонд, установленный в желудок через нос или рот.
3. Транспилорический зонд — зонд, проведенный через привратник в двенадцатиперстную или тощую кишку.
Цели:
1. Обеспечение пути питания.
2. Для введения лекарственных средств.
3. Для взятия образцов желудочного или кишечного содержимого.
4. Для декомпрессии и опустошения желудка.
Общие замечания:
1. Координация сосания и глотания развивается у недоношенных детей, родившихся после 32-й недели гестации.
2. У недоношенных энтеральное питание стимулирует секрецию гормонов, которые влияют на развитие желудочно-кишечного тракта.
3. Раннее начало питания сопровождается улучшением роста костной ткани, переносимости глюкозы, активизацией желчеотделения и меньшим риском нозокомиальной инфекции.
4. Раннее энтеральное питание приводит к уменьшению стоимости лечения и времени пребывания в больнице.
5. Неправильное расположение желудочного или транспилорического зонда (частота 21-43%) может привести к значительному увеличению частоты осложнений и смертности.
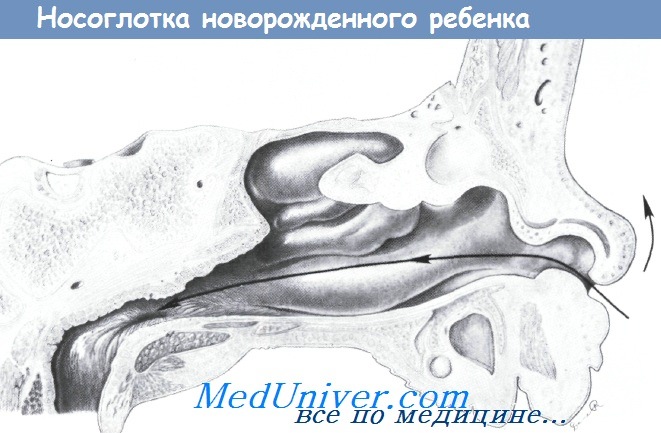
Естественный ход при установке зонда по направлению к носовым раковинам, где они могут препятствовать прохождению зонда и создавать впечатление обструкции.
Приподняв ноздри, можно направить зонд по направлению к затылку, что обеспечит меньшую травматизацию носовых ходов.
Показания для назо- или орогастрального зонда:
1. Отсутствие сосательного рефлекса и/или координации сосания и глотания.
2. Измененный рвотный рефлекс.
3. Невозможность усвоить необходмый объем питания естественным путем.
4. Симптомы со стороны дыхательной системы, препятствующие питанию через рот.
Противопоказания. Недавно перенесенная пластика или перфорация пищевода.
Ограничения:
1. Диаметр ноздрей.
2. Тип и объем респираторной терапии.
3. Врожденные пороки развития носоглотки.
Видео промывания желудка через назогастральный зонд у взрослого
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Зонд у новорожденных что
Оборудование для установки назо- или орогастрального зонда у новорожденного:
1. Оборудование для аспирации.
2. Монитор для слежения за сердечной деятельностью.
3. Зонды для новорожденных.
а. 3,5 или 5 Fr для новорожденных с массой тела менее 1000 г.
б. 5 или 8 Fr для новорожденных с массой тела более 1000 г.
4. Пластырь, защитная пленка для кожи на основе пектина.
5. Стерильная вода или физиологический раствор.
6. Шприцы по 5 и 20 мл.
7. Стетоскоп.
8. Перчатки.
9. Индикаторная бумага для определения рН.
5. Проводят диагностические мероприятия в отношении возможной перфорации пищевода после введения, если имеется следующее.
а. Аспирируется кровь.
б. Увеличивается секреция слюны.
в. Возникает дыхательная недостаточность.
г. Наблюдается пневмоторакс.
6. Немедленно прекращают процедуру, если имеется ухудшение функции дыхания.
7. Следует убедиться, что отверстие зонда расположено ниже уровня желудка новорожденного.
Особые обстоятельства:
1. Питание при имеющемся катетере пупочной вены следует проводить осторожно, поскольку для рекомендаций имеется недостаточно данных.
2. Между кормлениями зонд должен быть открыт, если проводят ИВЛ с постоянным положительным давлением в дыхательных путях (ППДДП).
3. На рН желудка метод проведения питания не влияет (постоянное и периодическое). Назначение препаратов, снижающих кислотность желудка, например антагонистов Н2-рецепторов гистамина или ингибиторов протонного насоса, не увеличивает рН желудочного сока, но рН редко превышает 6.

Естественный ход при установке зонда по направлению к носовым раковинам, где они могут препятствовать прохождению зонда и создавать впечатление обструкции.
Приподняв ноздри, можно направить зонд по направлению к затылку, что обеспечит меньшую травматизацию носовых ходов.
Методика установки назо- или орогастрального зонда у новорожденного
1. Моют руки и надевают перчатки, соблюдая правила асептики.
2. Очищают носовые ходы или ротоглотку новорожденного путем осторожного отсасывания, если необходимо.
3. Мониторируют ЧСС новорожденного и следят за появлением аритмии или дыхательной недостаточности во время процедуры.
4. Кладут новорожденного на спину с приподнятым головным концом кровати.
5. Определяют глубину введения путем измерения расстояния от носа до уха и до середины расстояния между мечевидным отростком и пупком. Отмечают длину зонда с помощью пластыря.
6. Смачивают кончик зонда стерильной водой или физиологическим раствором.
7. Вводят зонд в рот.
а. Прижимают переднюю часть языка указательным пальцем и стабилизируют положение головы тремя пальцами.
б. Вводят зонд по пальцу до ротоглотки.
8. Введение через нос (избегают применять этот путь у новорожденных с очень низкой массой тела, у которых назогастральные зонды могут вызывать нарушение дыхания и центральное апноэ):
а. Стабилизируют положение головы. Поднимают кончик носа, чтобы расширить ноздри.
б. Вводят кончик зонда, направляя его к затылку, а не к верхней части головы.
в. Осторожно продвигают зонд в ротоглотку.
г. Наблюдают за появлением брадикардии.
9. Если возможно, используют соску-пустышку для стимуляции сосания и глотания.
10. Немного наклоняют голову вперед.
11. Продвигают зонд на заранее определенную глубину:
а. Нельзя прилагать усилия при возникающем сопротивлении.
б. Останавливают процедуру, если возникают дыхательная недостаточность, кашель, активное сопротивление введению зонда, апноэ, брадикардия или цианоз.
12. Определяют расположение кончика зонда. Введение воздуха для проверки положения не является надежным методом, поскольку звук прохождения воздуха в дыхательные пути может передаваться в желудочно-кишечный тракт:
а. Аспирируют имеющееся содержимое; описывают и измеряют количество; определяют кислотность с помощью индикаторной бумаги для определения рН.
(1) Желудочное содержимое может быть чистым, желтовато-коричневым, бледно-зеленым, содержать молоко или быть окрашенным кровью.
(2) Величина рН жидкости из желудка должна быть меньше 6.
(3) Если рН аспирата из желудка больше 6 или аспират не получен, то положение зонда следует проверить с помощью рентгенографического исследования.
б. Подозревают перфорацию или неправильное положение, если при аспирации не получают воздуха или жидкости или если возникает дыхательная недостаточность, по зонду поступает кровь или зонд сложно установить.
13. Фиксируют установленный зонд к лицу с помощью пластыря. У недоношенных новорожденных пластырь накладывают поверх защитной пленки на основе пектина для предотвращения повреждения кожи.
а. Для кормления присоединяют шприц.
б. Для гравитационного дренирования присоединяют уловитель для образцов и располагают его ниже уровня желудка.
в. Для декомпрессии предпочтительно соединить трубку «Replogle» с постоянным отсосом с малым потоком воздуха.
14. Зажимают или закрывают зонд во время удаления для предотвращения попадания содержимого в глотку.
15. Фиксируют в истории болезни реакцию пациента, любые наблюдавшиеся изменения и результаты проверки положения зонда.
Видео промывания желудка через назогастральный зонд у взрослого
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Вскармливание недоношенных детей
Недоношенные дети представляют собой особую группу пациентов, для которых характерны признаки физиологической незрелости, что определяет особые условия выхаживания. В Российской Федерации доля недоношенных детей среди всех новорожденных в среднем состав
Недоношенные дети представляют собой особую группу пациентов, для которых характерны признаки физиологической незрелости, что определяет особые условия выхаживания. В Российской Федерации доля недоношенных детей среди всех новорожденных в среднем составляет 6–8%. Дети, родившиеся преждевременно, должны постоянно находиться в центре внимания врачей-педиатров, поскольку именно среди них отмечается наиболее высокий процент перинатальной патологии и значительно чаще выявляются отклонения в последующем развитии [1].
Чем больше степень недоношенности, тем с более существенными проблемами, связанными с последующим развитием ребенка, приходится сталкиваться: они могут варьировать от минимальных мозговых дисфункций (проблемы поведения и обучения, синдром гиперактивности с нарушением внимания) до тяжелых нарушений, приводящих к инвалидизации. Некоторые нарушения носят необратимый характер. Компенсаторные возможности детского организма достаточно велики, но они проявляются в полной мере лишь на фоне активной реабилитации, хорошего ухода, полноценного питания [2]. Проведенная реабилитация может оказаться успешной и привести к минимизации последствий недоношенности, в противном случае возникают различные отклонения в развитии ребенка. В этом плане роль адекватного питания недоношенного ребенка — как на самых ранних этапах его развития, так и на протяжении всего первого года жизни — трудно переоценить. В последние годы достигнут определенный прогресс как в совершенствовании методов вскармливания глубоконедоношенных детей (парентеральное и зондовое питание), так и в совершенствовании рецептуры специальных адаптированных смесей для недоношенных детей, в частности в результате введения в их состав нуклеотидов, длинноцепочечных полиненасыщенных жирных кислот, ряда участвующих в метаболизме нервной ткани аминокислот, оказывающих позитивное влияние на развитие головного мозга и органов зрения [3].
Наиболее высокие темпы роста отмечаются у плода во время неосложненной беременности. Но у недоношенных и маловесных детей период внутриутробного развития сокращается, вследствие чего «выпадает» заметная часть этого важного этапа, который протекает внеутробно. Это отражается на последующем развитии ребенка.
Недоношенными считаются дети, родившиеся при сроке беременности менее 37 недель (259 дней). Вследствие преждевременных родов ребенок рождается недостаточно зрелым и имеет проблемы, связанные с адаптацией к условиям внеутробной жизни. Ситуацию осложняют такие проблемы, как незрелость пищеварительной системы и ограниченные запасы питательных веществ в организме.
Поступление питательных веществ в организм до и после рождения. В процессе внутриутробного развития плод постоянно получает питательные вещества через пуповину. Глюкоза, аминокислоты и жирные кислоты обеспечивают элементное питание. После родов питание (грудное молоко) начинает поступать перорально, в виде более сложных соединений (лактоза — белки — липиды), требующих ферментативного расщепления.
Недоношенные дети, для которых после стабилизации их клинического состояния характерен так называемый «догоняющий рост» (английский термин — catch up growth), имеют высокие потребности в питательных веществах [4]. Между тем способность к их усвоению не всегда соответствует суммарным потребностям недоношенного ребенка в питательных веществах и энергии.
Назначение питания и выбор режима вскармливания у недоношенных детей продиктованы учетом особенностей пищеварительной системы и метаболизма основных нутриентов [5]. У таких младенцев снижен или полностью отсутствует сосательный и глотательный рефлекс, понижена секреция желудочного сока, отмечается недостаточная выработка панкреатических протеаз, липазы и кишечных дисахаридаз (особенно лактазы), но при этом достаточно высока активность пептидаз кишечника. Снижена способность желчи эмульгировать жирные кислоты. Обсеменение госпитальной микрофлорой в сочетании с замедленной и нерегулярной перистальтикой кишечника обусловливает высокую частоту дисбиотических нарушений. В связи с гипогалактией у значительной части преждевременно родивших женщин нередко отсутствует возможность обеспечить ребенка материнским молоком [6].
Особенности состава грудного молока после преждевременных родов. Еще в 1980-е гг. в ряде исследований было показано, что грудное молоко женщин, родивших раньше срока, имеет более высокую энергетическую ценность и содержит больше белка (1,2–1,6 г в 100 мл), а в аминокислотном составе отмечается более высокая концентрация незаменимых аминокислот. Содержание жиров в таком молоке также более высокое, к тому же в нем выше уровень эссенциальных жирных кислот. При одинаковом общем уровне углеводов в молоке содержится меньше лактозы и больше олигосахаридов. Для состава грудного молока у женщин после преждевременных родов характерно и более высокое содержание ряда защитных факторов, в частности лизоцима. Женское молоко легко усваивается и хорошо переносится недоношенными детьми, что позволяет достичь полного объема энтерального питания в более ранние сроки по сравнению с искусственным вскармливанием.
К несомненным преимуществам грудного молока относятся факторы иммунной защиты, в нем присутствуют бифидогенные компоненты (олигосахариды), положительно влияющие на формирование кишечной микрофлоры. Грудное молоко содержит гормоны, способствующие созреванию кишечника [7].
Последние исследования свидетельствуют о наличии различий в содержании факторов иммунологической защиты (в частности, секреторного иммуноглобулина (Ig) A) в грудном молоке женщин, родивших в разные сроки беременности (табл. 1).
Однако ряд исследований свидетельствует о том, что грудное молоко не полностью обеспечивает высокие потребности недоношенных детей в энергии и белке, в ряде витаминов (жирорастворимые — А, Д, Е, К и водорастворимые — витамин С, фолиевая кислота) и минеральных веществах (кальций, фосфор, магний) [9].
Тем не менее нет никаких сомнений в том, что именно женское молоко является оптимальным питанием для недоношенных детей, поэтому все усилия медицинского персонала должны быть направлены на сохранение грудного вскармливания в максимально возможном объеме, учитывая особую биологическую ценность материнского нативного (свежесцеженного) молока для недоношенного ребенка и важную роль контакта матери с новорожденным во время кормления.
Установлено, что температурная обработка отрицательно сказывается на питательной ценности женского молока: при вскармливании пастеризованным грудным молоком прибавка в массе тела на первом месяце жизни является недостаточной и составляет в среднем 9,6 ± 0,4 г/кг/сут [10].
Доказано, что молоко преждевременно родивших женщин может удовлетворить потребности в пищевых веществах недоношенных детей с массой тела более 1700–2000 г. В то же время недоношенные дети с меньшей массой тела после окончания раннего неонатального периода постепенно начинают испытывать дефицит в белке, кальции, фосфоре, магнии, натрии, меди, цинке и витаминах В2, В6, С, D, Е, К, фолиевой кислоте и нуждаются в оптимизации питания — обогащении рационов [11].
Методы кормления недоношенных детей
В условиях родильного дома и в отделениях неонатологии в настоящее время используются следующие методы кормления недоношенных детей и их сочетания.
На рисунке представлена последовательность использования методов кормления недоношенных детей.
В зависимости от гестационного возраста, массы тела ребенка и клинического статуса недоношенные дети в ряде случаев нуждаются в полном парентеральном питании. Для того чтобы поддерживать перистальтическую и секреторную деятельность ЖКТ, постепенно и в возрастающем объеме вводится энтеральное питание. Сначала питание вводится через зонд, а затем постепенно заменяется кормлением из бутылочки с использованием грудного молока или специальных смесей для недоношенных детей.
У детей с массой тела 1800–2000 г проводят пробное кормление из бутылочки. При неудовлетворительной активности сосания осуществляется зондовое кормление (чаще порционным методом) в полном или частичном объеме [10, 12].
Новорожденные дети с массой тела более 2000 г при оценке по шкале Апгар 7 баллов и выше могут быть приложены к груди матери в первые сутки жизни. Обычно в родильном доме или стационаре устанавливается 7–8-разовый режим кормления. Для недоношенных детей неприемлемым является свободный режим кормления в связи с их неспособностью регулировать объем высосанного молока и высокой частотой перинатальной патологии, однако возможно ночное кормление. При грудном вскармливании необходимо внимательно следить за появлением признаков усталости — периорального и периорбитального цианоза, одышки и др. Наличие данной симптоматики является показанием к более редкому прикладыванию к груди или к частичному докорму сцеженным молоком из бутылочки, либо к полному переходу к кормлению из бутылочки [10].
Таким образом, выбор способа вскармливания должен быть строго индивидуальным, определяться степенью физиологической зрелости ребенка, клиническим состоянием пациента и соответственно меняться по мере его улучшения.
При расчете питания для недоношенных детей следует пользоваться только «калорийным» методом, предполагающим следующий расчет питания [12] в зависимости от возраста ребенка: 1-й день — 30 ккал/кг; 2-й день — 40 ккал/кг; 3-й день — 50 ккал/кг; 4-й день — 60 ккал/кг; 5-й день — 80 ккал/кг; 6-й день — 80 ккал/кг; 7-й день — 90 ккал/кг; 10–14-й дни — 100–120 ккал/кг; 30-й день — 130 ккал/кг (искусственное), 140 ккал/кг (грудное) молоко.
По мере улучшения клинического состояния ребенка и при установлении наличия стабильной прибавки массы тела, а также при наличии активного сосательного рефлекса ребенка переводят на грудное вскармливание или кормят сцеженным грудным молоком в сочетании со специальной смесью для недоношенных детей.
Специальные смеси для недоношенных детей
Как показывает клинический опыт, у большинства матерей после преждевременных родов отмечается гипогалактия. Ситуация усугубляется тем, что у детей снижен или отсутствует сосательный рефлекс, что еще в большей мере способствует угасанию лактации. В связи с этим возникает необходимость использования специальных смесей для недоношенных детей. При их разработке учтены особые потребности таких младенцев в энергии и пищевых веществах и, безусловно, принимается во внимание недостаточная зрелость пищеварительной системы, которая является лимитирующим фактором усвоения ряда важнейших нутриентов (лактозы, жиров, жирорастворимых витаминов и т. д.) [13].
Соотношение казеина и сывороточных белков приближено к таковому в грудном молоке; в составе современных смесей для недоношенных детей оно составляет 40 : 60.
В состав наиболее полно отвечающих потребностям ребенка современных специальных смесей (например, Фрисопре) включены нуклеотиды, что способствует более быстрому соматическому росту и укрепляет иммунную систему детей. Сведения о содержании нуклеотидов в грудном и коровьем молоке, а также европейские рекомендации по их содержанию в детских молочных смесях, принятые в 1996 г., представлены в таблице 2.
В организме нуклеотиды выполняют роль регуляторов различных процессов биосинтеза. В свою очередь, они могут синтезироваться в тканях организма и (в обычных условиях) не относятся к незаменимым нутриентам. Но этот синтез является энергоемким и его объем ограничен, примером чего является напряженный синтез нуклеотидов в слизистой оболочке кишечника новорожденных. Поэтому в определенных условиях, особенно при интенсивном росте, большое значение начинают приобретать пищевые нуклеотиды [14].
Нуклеотиды положительно влияют на созревание клеток кишечного эпителия и способствуют лучшему формированию кишечных ворсинок. Оказывая позитивное влияние на формирование кишечной микрофлоры, нуклеотиды тем самым улучшают процессы усвоения пищевых веществ. Это приводит к нормализации консистенции и частоты стула [14].
Включение в состав смеси Фрисопре глутаминовой кислоты и аргинина активизирует процессы созревания слизистой оболочки кишечника и повышает эффективность усвоения пищевых веществ. Аргинин вводится в состав смеси также в целях повышения биологической ценности белка и дополнительно способствует созреванию иммунной системы.
Аминокислота триптофан стимулирует продукцию серотонина, который, в свою очередь, необходим для развития головного мозга и является предшественником синтеза мелатонина, регулирующего смену суточных ритмов сна и бодрствования [15].
Таурин — не связанная с белком свободная аминокислота — играет важную роль в развитии нервной ткани и головного мозга. Таурин необходим для синтеза новых тканей и способствует активной клеточной пролиферации, что особенно важно в перинатальном периоде. Таурин также принимает участие в защите клеточных мембран от экзогенных токсинов, участвует в формировании зрительных элементов сетчатки глаза и в синтезе желчных кислот.
Исключительно важное значение имеет и жирнокислотный состав смесей для недоношенных детей, прежде всего в связи с тем, что у них ограничен эндогенный синтез важнейших длинноцепочечных полиненасыщенных жирных кислот — арахидоновой и докозагексаеновой [16]. Последние введены в состав некоторых продуктов (Фрисопре, Пре НАН, Хумана 0-ГА) и играют существенную роль в структуре и функции биологических мембран, являются эссенциальными компонентами фосфолипидов головного мозга, фоторецепторов сетчатой оболочки глаз [17].
В состав жирового компонента ряда продуктов (Хумана 0-ГА, Пре-Нутрилак, Фрисопре, Пре НАН) входят среднецепочечные триглицериды, которые обеспечивают усвоение жира без действия липазы, высокую абсорбцию жира в кишечнике, лучшее усвоение кальция и цинка [16].
В углеводном компоненте содержание лактозы несколько снижено во избежание избыточной нагрузки на ЖКТ маловесных детей (для которых характерна ограниченная способность к усвоению молочного сахара). Кроме лактозы, в ряде продуктов (Хумана 0-ГА, Пре-Нутрилак, Пре НАН) присутствует полимер глюкозы — декстрин-мальтоза, а в некоторых — полисахариды в составе глюкозного сиропа (Фрисопре, Пре-Нутрилон) [16].
Энергетическая ценность смесей для недоношенных детей, как правило, несколько выше и находится в пределах 75–80 ккал/100 мл, хотя некоторые продукты предлагается использовать в двух стандартных разведениях, получая при этом либо более, либо менее концентрированное питание (например: Пре НАН, Энфамил, Фрисолак Прематур).
Обязательным компонентом молочных смесей для недоношенных детей является витаминоподобное вещество L-карнитин, участвующий в метаболизме жирных кислот.
Введение в состав смеси пищевых волокон (галактоолигосахаридов) обеспечивает хорошие бифидогенные свойства продукта Фрисопре, способствует росту собственных бифидобактерий в кишечнике ребенка, что особенно важно для незрелых детей, учитывая высокую частоту дисбиотических нарушений.
На втором месяце жизни калорийность рациона ребенка зависит от массы тела при рождении: у ребенка, родившегося с массой тела более 1500 г, калорийность рациона снижается ежемесячно на 5 ккал/кг до норм, принятых для зрелых детей и составляющих 115 ккал/кг. Снижение калорийности рациона глубоко недоношенных детей (масса тела при рождении менее 1500 г) осуществляется в более поздние сроки — после 3-месячного возраста.
Введение специализированного продукта в рацион ребенка следует осуществлять постепенно, в течение 5–7 дней, с учетом индивидуальной переносимости. Искусственное вскармливание такой смесью следует продолжать до достижения ребенком веса около 3000 г, после чего ребенка постепенно (в течение 1 мес) переводят на стандартную смесь. В дальнейшем, при необходимости (глубокая недоношенность, малая прибавка в массе тела), смеси для недоношенных детей могут оставаться в рационе малыша на протяжении нескольких месяцев в небольшом объеме (1–2 кормления). При этом обязательным является расчет рационов питания не только по калорийности, но и по содержанию в нем основных пищевых веществ (особенно белка).
Литература
В. А. Скворцова, доктор медицинских наук
Т. Э. Боровик, доктор медицинских наук, профессор
Г. В. Яцык, доктор медицинских наук, профессор
С. Г. Грибакин, доктор медицинских наук
А. В. Андреева
О. Л. Лукоянова, кандидат медицинских наук
Т. Р. Чумбадзе
НЦЗД, компания «Аника», Москва
Назогастральный зонд: постановка, правила кормления, профилактика осложнений
Время чтения: 4 мин.
Предлагаем вашему вниманию вторую часть лекции об аспирации, дисфагии и технике постановки назогастрального зонда. Автор — заведующая отделением длительной респираторной поддержки и отделением паллиативной помощи № 3, врач анестезиолог-реаниматолог, врач-реабилитолог Московского многопрофильного центра паллиативной помощи ДЗМ Варвара Брусницына.
В первой части рассказывалось об оценке дисфагии, риске аспирации и профилактике аспирации у паллиативных пациентов. Вы также можете посмотреть запись вебинара, посвященного этим взаимосвязанным темам, по ссылке.
Постановка назогастрального зонда. 12 шагов
1. Убедитесь, что у вас есть все необходимое для постановки зонда. С этим обычно нет проблем в стационаре, но, если вы ставите зонд у пациента дома, проследите, чтобы укладка была аккуратно укомплектована. Это важно для пациента, который долго болеет, и для его родственников.
Укладка должна включать в себя:
2. Выбирайте минимальный размер зонда — F6/F8/F10/F12/F14/F16/F18/F20/F22/F24. С маленьким зондом пациенту легче, но такой зонд может засориться, и тогда придется его менять.
3. Поместите зонд в морозильную камеру на 1,5 часа. Это сделает его жестче и упростит процедуру установки. В экстренной ситуации конец зонда можно поместить в лоток со льдом. Холод не очень приятен пациенту, но лучше за один раз поставить жесткий, холодный зонд, чем мучить человека несколькими попытками с пластичным.
4. Используйте полиуретановые зонды. Они прозрачны и термопластичны. Устойчивы к воздействию желудочных кислот. Из-за того, что они мягкие, пролежней от них практически не бывает. Ставятся с помощью внутреннего металлического бужа, который потом вытаскивается. Можно устанавливать на срок до 30 дней.
5. Разговаривайте с пациентом и его близкими. Объясняйте каждое действие. Даже если пациент не в сознании, возьмите его за руку, погладьте, скажите ободряющие слова, успокойте. Поверьте, вам самим станет от этого легче.
6. Определите наиболее подходящую для введения зонда половину носа. Если пациент в сознании, прижмите сначала одно крыло носа и попросите его дышать другим, закрыв рот. Затем повторите эти действия с другим крылом носа.
7. Определите расстояние, на которое следует ввести зонд (расстояние от кончика носа до мочки уха и вниз по передней брюшной стенке — так, чтобы последнее отверстие зонда было ниже мечевидного отростка). Помогите пациенту принять высокое положение Фаулера. Грудь пациента прикройте полотенцем.
8. Обработайте слепой конец зонда анестетиком или проведите местную анестезию полости носа и глотки орошением 10%-го спрея лидокаина. Попросите пациента слегка запрокинуть назад голову, введите зонд через нижний носовой ход на расстояние 15-18 см и попросите пациента наклонить голову вперед.
9. Попросите пациента попытаться сделать глотательное движение, для облегчения которого можно дать ему столовую ложку воды. Сразу, как только зонд введен на расстояние от кончика носа до мочки уха, ВАЖНО убедиться, что пациент может говорить и свободно дышать — то есть, зонд не попал в трахею. После этого мягко продвигайте зонд до нужной отметки.
10. Убедитесь в правильном местоположении зонда в желудке: введите в желудок около 20 мл воздуха с помощью шприца Жанэ, прослушивая при этом эпигастральную область. Или присоедините шприц к зонду: при подтягивании поршня на себя в зонд должно начать поступать содержимое желудка (вода и желудочный сок).
11. Закрепите зонд пластырем. Пожалуйста, используйте максимально щадящий пластырь.
12. Закройте зонд заглушкой и обязательно запишите на прикроватной табличке, в какую ноздрю и когда был введен зонд.
Планово зонд надо заменить через 2-2,5 недели. Но если зонд не загрязнился и проблем с ним не возникает, не стоит это делать так часто. Полиуретановые зонды могут использоваться до 6 недель. Если врач предполагает стояние зонда более 6 недель, стоит подумать о гастростоме.
Как и чем кормить через назогастральный зонд?
Вариантов кормления через зонд несколько. Каждый из них имеет свои преимущества и недостатки:
Кормить пациента через зонд можно измельченным в блендере естественным питанием отдельно или в сочетании с зондовым энтеральным питанием (или только зондовым энтеральным питанием).
