Что будет если инсулин ввести внутривенно
УЗ «Могилевская городская больница скорой медицинской помощи»
Тема 6. Способы и техника введения инсулина
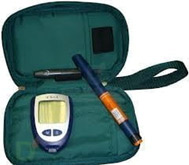
Инсулин вводится подкожно. Вводить инсулин можно с помощью:
В Республике Беларусь инсулин чаще всего вводится с помощью инсулиновых шприцев.
Объемы инсулиновых шприцев: 0,3 мл, 0,5 мл и 1 мл. На шприц нанесены деления и цифры. Цифры означают количество единиц (от 10 до 100 ЕД). На картинке – шприц объемом 1 мл, в 1 мл – 100 ЕД, одно маленькое деление соответствует 2 ЕД инсулина.
Шприц должен соответствовать концентрации инсулина. Сейчас почти все инсулины с концентрацией 100 ЕД/мл и им соответствуют шприцы 0,1 мл – 10 ЕД (на шприце 1 мл маркировка 100 ЕД; 0,5 мл – 50 ЕД; 0,3 мл – 30 ЕД). Но раньше выпускался инсулин с концентрацией 40 ЕД/мл и для него существовали соответствующие шприцы (40 ЕД – 1 мл). Если в такой шприц набрать инсулин с концентрацией 100 ЕД/мл, то доза будет превышена в 2,5 раза. В нашей стране в настоящее время такие шприцы не выпускаются.
Кроме того, в аналоге инсулина туджео 300 ЕД в мл. Туджео вводится шприц-ручкой. Но если вдруг понадобится вводить туджео шприцем и набрать дозу инсулиновым шприцем на 100 ЕД/мл, то набранная доза будет больше нужной дозы в 3 раза.
Длина иглы в инсулиновом шприце от 6 до 13 мм. Толщина иглы обозначается буквой «G» (G31 – G26). Чем больше номер, тем тоньше игла (т.е. игла G31 будет тоньше, чем G26).
Выбор оптимальной длины и толщины иголки зависит от индивидуальных параметров организма и подбирается экспериментально.
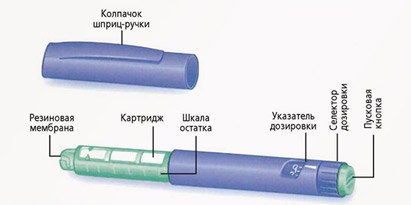
Шприц-ручки
Шприц ручка это устройство, в которое вставляется инсулин в специальных флаконах – картриджах. Устанавливается необходимая доза инсулина и вводится в виде инъекции (укола), как и шприцем. Иглы в шприц-ручках съемные и должны меняться после каждой инъекции инсулина. Иглы являются универсальными и подходят ко всем шприц-ручкам. После инъекции инсулина иглу надо снять. Нельзя хранить ручку с накрученной иглой. Из иглы может подтекать инсулин и в картридж может попадать воздух.
Иглы бывают длиной от 4 до 12 мм и толщиной G32 – G29. Как и в инсулиновом шприце, чем больше номер, тем тоньше игла.
Шприц-ручки бывают одноразовые и многоразовые.
Например, лантус выпускается в виде одноразовой ручки (Лантус СолоСтар) и в картриджах для многоразовой ручки (Лантус Пенфилл).
Одноразовая ручка содержит 300 ЕД инсулина (1 мл – 100 ЕД, в одной ручке 3 мл). Когда инсулин заканчивается, ручка выбрасывается. В многоразовых шприц-ручках вставляется инсулин в сменных картриджах. Один картридж (кроме Туджео) также содержит 300 ЕД инсулина (1 мл – 100 ЕД, 1 картридж – 3 мл). В Туджео в 1 мл содержится 300 ЕД.
В Республике Беларусь инсулин в картриджах выписывается только определенным категориям пациентов, указанным в приказе Минздрава (дети, беременные и др.).
Также ручки бывают электронными и механическими. Еще ручки отличаются по шагу, которым можно вводить инсулин (0,1 ЕД; 0,5 ЕД; 1 ЕД).
Для каждого инсулина – своя шприц-ручка!
Подробнее узнать о шприц-ручках можно на сайте www.test-poloska.ru.
Инъекционный порт
Смысл порта – сокращение количества инъекций. При его использовании выполняется 1 прокол при установке самого айпорта (специальным устройством под кожу вводится канюля), а далее укол инсулина делается не под кожу, а в резиновую мембрану айпорта. Инъекционный порт устанавливается на 72 часа или на 75 инъекций. Канюля айпорта бывает 6 и 9 мм (для детей – 6 мм, для взрослых – 9 мм). В айпорт нельзя одновременно вводить короткий и длинный инсулин. Разница между инъекциями должна быть не менее 60 минут. Причем сначала надо вводить короткий инсулин и только через 60 минут в айпорт можно ввести инсулин длительного действия. После введения в айпорт инсулина длительного действия ввести в него короткий инсулин можно не ранее чем через 3 часа. Поэтому часто инсулин короткого действия вводят в айпорт, а длительного – обычной инъекцией.
Инъекции в мембрану айпорта можно выполнять шприцами и ручками. Но иглы должны быть не менее 6 мм.
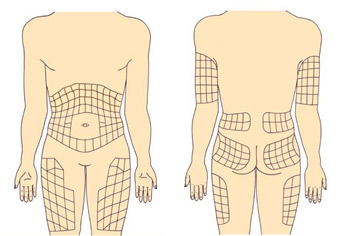
Рекомендуемые места введения инсулина
Инсулин можно вводить в область передненаружной поверхности бедер, ягодицы, наружную поверхность плеч, живот. В области живота инсулин не вводится вокруг зоны пупка (отступить 2 см по диаметру), в область срединной линии живота, от ребер вниз надо отступить 2 см.
В зависимости от того, куда ввели инсулин, отличается время действия генно-инженерного инсулина (аналогов это не касается). Самое быстрое действие инсулина наступает при введении в живот, поэтому в живот вводится инсулин короткого действия. Инсулин длительного действия вводится в бедра, ягодицы.
Вводить в плечи инсулин желательно, только если инъекцию выполняет кто-то другой.
Инсулин будет быстрее всасываться в условиях повышенного кровообращения (после бани, горячего душа, массажа места инъекции, физической нагрузки). Замедляет действие инсулин охлаждение, спазм сосудов, обезвоживание.
Нельзя вводить инсулин в одно и то же место, места введения инсулина необходимо чередовать (левое-правое бедро или плечо, левая – правая половина живота), расстояние между инъекциями инсулина должно быть не менее 2 см. Инсулин не вводится в область рубцов, стрий (растяжек).
Необходимо регулярно осматривать и прощупывать места инъекций. При неправильной технике инъекций (многократные инъекции в одно место, введение холодного инсулина, многократное использование игл и пр.) в местах введения инсулина могут образовываться уплотнения («шишки») – гипертрофическая липодистрофия. Реже в местах введения инсулина может происходить истончение подкожно-жировой клетчатки («впадины») – атрофическая липодистрофия. В места липодистрофий инсулин вводить нельзя! Если ввести инсулин в места липодистрофий, он не будет оказывать действия, также инсулин может там накапливаться и действовать непредсказуемо. В места липодистрофий теряется чувствительность, поэтому часто пациенты вводят туда инсулин, потому что там «небольно». Так делать нельзя.
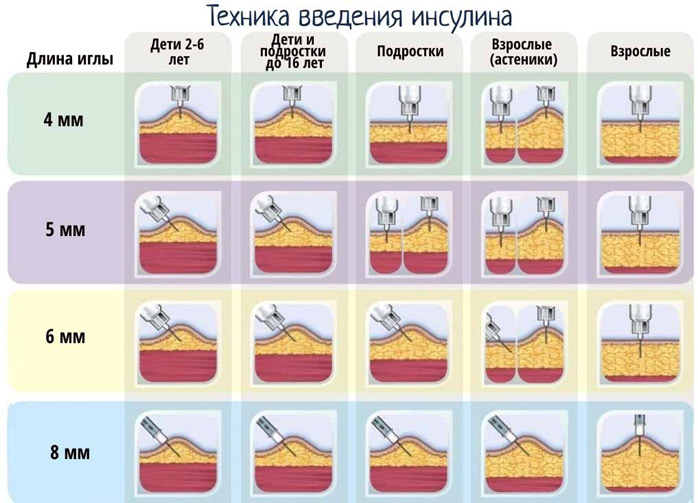
Техника введения инсулина
Если Вы вводите продленный НПХ-инсулин («мутный» длинный инсулин), то перед употреблением его надо перемешать, перекатывая между ладонями не менее 10 раз (нельзя трясти флакон).
Если инсулин вводится шприцем, то в шприц надо набрать воздух соответственно количеству единиц инсулина (если вводите 10 ЕД инсулина, необходимо набрать 10 ЕД воздуха). Затем ввести набранный воздух из шприца во флакон с инсулином и набрать нужное количество инсулина. Удалить пузырьки воздуха из шприца (иглу вверх, постучать по шприцу), выпустить из шприца лишний воздух и 0,5-1 ЕД инсулина.
Если инсулин вводится шприц-ручкой, то надо набрать и выпустить 0,5-1 ЕД инсулина, держа при этом ручку иглой вверх.
Инъекции выполняются на чистом участке кожи чистыми руками. Если Вы соблюдаете правила личной гигиены, ежедневно принимаете душ, нет необходимости дезинфицировать кожу перед каждым уколом.
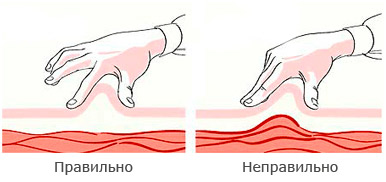
Необходимо сформировать кожную складку (в складку нельзя захватывать мышцы, должна захватываться только кожа). Инъекции инсулина должны осуществляться в подкожный жир, а не внутрикожно или внутримышечно. Складку надо брать двумя пальцами, а не всей кистью (чтобы не захватить мышцы).
Игла вводится в зависимости от толщины подкожно-жировой клетчатки вводится под прямым углом или под углом 45 0 в основание складки, срезом иглы вверх.
После введения иглы надо плавно нажать на поршень шприца или шприц-ручки (шприц-ручку обхватить 4 пальцами, нажимать большим пальцем), ввести инсулин и удерживать шприц под кожей не менее 10 секунд (считать до 20). Чем больше доза, тем дольше надо держать иглу. После этого достать иглу (складку не отпускать!), подождать немного (досчитать до 3) и отпустить складку.
Хранение инсулина
Запас инсулина должен храниться в холодильнике при температуре от 2 до 8 0 С. Инсулин нельзя замораживать! Если инсулин был заморожен, его нельзя использовать. В самолете инсулин нельзя сдавать в багаж, т.к. там он может замерзнуть.
Флакон, из которого вводится инсулин может храниться при комнатной температуре (до 25 0 С) до 4 недель. Следует избегать попадания прямых солнечных лучей на инсулин.
Если инсулин достали из холодильника, он должен находиться при комнатной температуре не менее 1 часа.
В поездках, на пляже запас инсулина надо хранить в специальных термочехлах для хранения инсулина. Также термочехлы надо использовать при отрицательной температуре окружающего воздуха. При отрицательной температуре окружающего воздуха инсулин надо перевозить, положив его ближе к телу, а не в сумке.
Нельзя использовать инсулин при изменении цвета, появлении хлопьев, осадка.
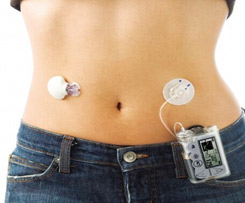
Инсулиновая помпа
Инсулиновая помпа представляет собой устройство, с помощью которого осуществляется постоянная подкожная инфузия инсулина. При этом вводится ультракороткий инсулин с заданной скоростью в качестве базального инсулина и дополнительно вводятся болюсы инсулина на еду.
При этом можно изменять скорость введения базального инсулина по часам (эффективно при синдроме утренней зари), применять различные болюсы введения короткого инсулина (эффективно для компенсации различной еды). Помпа не заменяет мониторинг глюкозы (мониторинг это одна статья расходов, помпа – другая). Также надо понимать, что помпа не является искусственной поджелудочной железой, решение о вводимых дозах инсулина принимает не помпа, а пациент. При использовании помпы надо уметь точно считать углеводы, знать свои коэффициенты. Помпу есть смысл ставить, когда имеется понятие о компенсации диабета. При отсутствии знаний помпа сама по себе не решит проблемы компенсации.
В проводных помпах инсулин находится в специальном резервуаре в помпе. Помпа фиксируется на одежде, на теле подкожно устанавливается канюля (тефлоновая или стальная), инсулин подается от помпы к канюле через специальный катетер. Резервуар, канюлю и катетер надо менять каждые 3 дня.
В Республике Беларусь сертифицированы проводные помпы компании «Медтроник», которые продает компания Zarga, на сайте которой можно ознакомиться с действующими ценами.
Основные проблемы, которые возникают при использовании помпы:
Неотложные состояния при сахарном диабете
Неотложные состояния при сахарном диабете (СД) различаются по этиологии и патогенезу.
Выделяют следующие клинико-метаболические варианты острых осложнений в диабетологии:
— диабетический кетоацидоз и кетоацидотическая кома,
— гиперосмолярная кома и гиперосмолярное гипергликемическое состояние,
— молочнокислый ацидоз (лактат-ацидоз),
— гипогликемия и гипогликемическая кома.
ДИАБЕТИЧЕСКИЙ КЕТОАЦИДОЗ И КЕТОАЦИДОТИЧЕСКАЯ КОМА
Диабетический кетоацидоз (ДКА) – это критическое, ургентное состояние при СД, которое развивается вследствие абсолютного дефицита инсулина или выраженной относительной инсулиновой недостаточности, при несвоевременной диагностике и лечении, приводящее к развитию кетоацидотической комы с тяжелыми гормонально-метаболическими нарушениями органов и систем. ДКА, как правило, развивается при декомпенсации СД 1 типа, но вместе с тем редко может развиваться и при СД 2 типа. Это имеет подтверждение в исследованиях отечественных и зарубежных авторов (В. В. Потемкин, 2008, А. М. Мкртумян, 2008).
Причиной ДКА является абсолютный дефицит инсулина. Той или иной выраженности ДКА определяется у большинства пациентов на момент манифестации СД-1 (10—20 % всех случаев ДКА).
У пациента с установленным диагнозом СД-1 ДКА может развиться при прекращении введения инсулина, зачастую самим пациентом (13 % случаев ДКА), на фоне сопутствующих заболеваний, в первую очередь, инфекционных, при отсутствии увеличения дозы инсулина (30-40 %).
До 20 % случаев развития ДКА у молодых пациентов с СД-1 связаны с психологическими проблемами и/или нарушениями пищевого поведения (боязнь прибавки веса, боязнь гипогликемии, подростковые проблемы). Достаточно частой причиной ДКА в ряде стран является отмена инсулина самим пациентом из-за дороговизны препаратов для некоторых слоев населения (табл. 7. 11).
Вследствие нарастания кетонемии появляется тошнота, рвота, анорексия. Дефицит инсулина и повышенная секреция контринсулярных гормонов способствует распаду белков (катаболизм – протеолиз) в печени и образованию из них глюкозы в реакциях глюконеогенеза, а также аммиака, мочевины, что приводит к азотемии. Гипергликемия, гиперкетонемия, гиперазотемия приводят к нарушениям водно-электролитного обмена, повышению осмотического диуреза, выведению натрия, калия, фосфора, хлора. При полиурии вначале преобладает выделение натрия, поскольку он содержится во внеклеточной жидкости, а затем позднее присоединяется выход калия из клеток и повышенное его выделение с мочой. Развивается выраженное обезвоживание организма, уменьшается объём циркулирующей крови.
Таким образом, при кетоацидотической коме происходят глубокие метаболические нарушения, декомпенсация углеводного, липидного, белкового, электролитного обмена.
Токсическое воздействие кетоновых тел на клетки центральной нервной системы, угнетение ферментных систем, снижение утилизации глюкозы клетками мозга, кислородное голодание ведёт к нарушению сознания, развитию кетоацидотической комы.
Развитие ДКА в зависимости от вызвавшей его причины может занимать от нескольких недель до суток. В большинстве случаев ДКА предшествуют симптомы декомпенсации диабета, но иногда они могут не успеть развиться. Клинические симптомы ДКА включают полиурию, полидипсию, похудение, разлитые боли в животе («диабетический псевдоперитонит»), дегидратацию, выраженную слабость, запах ацетона изо рта (или фруктовый запах), постепенное помутнение сознания. Истинная кома при ДКА в последнее время в силу ранней диагностики развивается относительно редко. При физикальном обследовании выявляются признаки обезвоживания, тургора кожи и плотности глазных яблок, тахикардия, гипотония. В далеко зашедших случаях развивается дыхание Куссмауля. Более чем у 25% пациентов с ДКА развивается рвота, которая по цвету может напоминать кофейную гущу.
Базируется на данных клинической картины, указаниях на наличие у пациента СД-1, а также данных лабораторного исследования. Для ДКА характерна гипергликемия (в ряде случаев незначительная), кетонурия, метаболический ацидоз, гиперосмолярность.
Лабораторная диагностика острых осложнений сахарного диабета
Эффективная осмо-лярность, мОсм/кг
При обследовании пациентов с острой декомпенсацией СД необходимо определение уровня гликемии, креатинина и мочевины, электролитов, на основании чего производится расчет эффективной осмолярности. Кроме того, необходима оценка кислотно-основного состояния. Эффективная осмолярность (ЭО) рассчитывается по следующей формуле:
2 X [Na+ (мЭкв/л) + глюкоза (ммоль/л) ].
У большинства пациентов с ДКА определяется лейкоцитоз, выраженность которого пропорциональна уровню кетоновых тел в крови. Уровень натрия, как правило, снижен вследствие осмотического оттока жидкости из интрацеллюлярных пространств в экстрацел-люлярные в ответ на гипергликемию. Реже уровень натрия может быть снижен ложноположительно как следствие выраженной гипертриглицеридемии. Уровень калия сыворотки исходно может быть повышен вследствие его перемещения из экстрацеллюлярных пространств.
Базируется на данных клинической картины, указаниях на наличие у пациента СД-1, а также данных лабораторного исследования. Для ДКА характерна гипергликемия (в ряде случаев незначительная), кетонурия, метаболический ацидоз, гиперосмолярность
Лабораторная диагностика острых осложнений сахарного диабета
Эффективная осмо-лярность, мОсм/кг
У большинства пациентов с ДКА определяется лейкоцитоз, выраженность которого пропорциональна уровню кетоновых тел в крови. Уровень натрия, как правило, снижен вследствие осмотического оттока жидкости из интрацеллюлярных пространств в экстрацел-люлярные в ответ на гипергликемию. Реже уровень натрия может быть снижен ложноположительно как следствие выраженной гипертриглицеридемии. Уровень калия сыворотки исходно может быть повышен вследствие его перемещения из экстрацеллюлярных пространств.
Другие причины потери сознания у пациентов с СД. Дифференциальная диагностика с гиперосмолярной комой, как правило, не вызывает затруднений (развивается у пожилых пациентов с СД-2) и не имеет большого клинического значения, т. к. принципы лечения обоих состояний сходны. При невозможности оперативно выяснить причину потери сознания пациента с СД ему показано введение глюкозы, т. к. гипогликемические состояния встречаются значительно чаще, а быстрая положительная динамика на фоне введения глюкозы сама по себе позволяет выяснить причину потери сознаний.
Лечение
Диабетический кетоацидоз, прекоматозное состояние и кома требуют немедленной госпитализации больного для проведения экстренной медицинской помощи. Необходимо срочное определение гликемии, глюкозурии, кетонемии и кетонурии, кислотно-щелочного равновесия, содержания натрия и калия, креатинина, мочевины, клинического анализа крови и мочи, ЭКГ, неврологическое обследование. На догоспитальном этапе или в приемном отделении после определения гликемии, глюкозурии, ацетонурии начинают внутривенно капельно инфузию 0, 9 % раствора хлорида натрия, при выраженной дегидратации до 1 л/час, инсулин короткого действия 20 ЕД в/м. Дальнейшее лечение осуществляют в реанимационном отделении или в отделении интенсивной терапии. Лечение ДКА легкой степени при сохраненном сознании и отсутствии тяжелой сопутствующей патологии можно проводить в эндокринологическом или терапевтическом отделении. В отделении реанимации и интенсивной терапии необходимо проводить мониторинг лабораторных показателей в целях предупреждения осложнений терапии – гипогликемии, гипокалиемии и гипонатриемии. Предлагаются следующие схемы лабораторного мониторинга:
Исследование глюкозы крови 1 раз в час, до снижения гликемии ниже 14 ммоль/л, затем 1 раз в 3 часа
Контроль ацетона мочи и кетоновых тел – 2 раза в первые 2 суток, затем 1 раз в сутки
Фосфор – только у пациентов при недостаточности питания и хроническом алкоголизме
Остаточный азот, мочевина, креатинин сыворотки – исходно и через 3 дня
Гематокрит, газоанализ и рН – 1-2 раза в сутки до нормализации кислотно-основного состояния Терапия ДКА направлена на коррекцию основных патофизиологических нарушений. Основные компоненты лечебных мероприятий при кетоацидотической коме включают: устранение инсулиновой недостаточности, восстановление электролитного баланса и кислотно-основного равновесия, лечение сопутствующих заболеваний, которые могут быть причиной ДКА.
В настоящее время доказана целесообразность режима малых доз инсулина при лечении кетоацидотической комы, так как при введении больших доз инсулина имеется опасность развития гипогликемии, гипокалиемии, отёка мозга. Введение малых, физиологических доз инсулина проводится одновременно с регидратацией. При ДКА проводится внутривенная (в/в) инсулинотерапия в виде длительных инфузий. Для достижения оптимальных концентраций инсулина в крови необходима непрерывная инфузия малых доз инсулина – 0, 1 ЕД/кг/час, 4-10 ЕД инсулина в час (в среднем 6 ЕД/час). Это позволяет снизить липолиз, кетогенез и продукцию глюкозы печенью, таким образом воздействовать на главные звенья патогенеза ДКА. Начальная доза ИКД составляет 0, 15 ЕД/кг массы тела (в среднем 10-12 ЕД) и вводится в/в болюсно. Необходимую дозу инсулина набирают в инсулиновый шприц, добирают 0, 9 % NaCl до 1 мл вводят очень медленно (2-3 мин). Затем переходят на в/в введение ИКД по 0, 1 ЕД/кг/час (5-8 ЕД/час) с помощью инфузомата (первый вариант). Инфузионнную смесь готовят следующим образом: 50 ЕД ИКД+2 мл 20% раствора альбумина или 1 мл крови пациента для предотвращения сорбции инсулина в системе, и доводят общий объем до 50 мл 0, 9% NaCl. При отсутствии инфузомата используется второй вариант инсулинотерапии. С этой целью инфузионный раствор готовят из расчета 100 ЕД ИКД на каждые 100 мл 0, 9% раствора NaCl, концентрации ИКД будет составлять 1 ЕД/мл. Для предотвращения сорбции инсулина необходимо добавить 4 мл 20% альбумина на 100 мл раствора. Недостатком данного метода является трудность в титровании малых доз инсулина 12 по числу капель или мл смеси, а также возможность перегрузки жидкостью. Если инфузомата нет, более удобен в использовании 3 вариант. ИКД вводят в/в болюсно 1 раз в час шприцем в “резинку” инфузионной системы. Пример: в инсулиновый шприц набирают 6 ЕД ИКД, набирают в шприц 2 мл и добирают до 2 мл 0, 9% раствора NaCl и вводят медленно в течение 2-3 минут. Длительность фармакодинамического эффекта ИКД при этом составляет до 60 минут. Преимуществом этого способа введения является отсутствие сорбции инсулина, не нужно добавлять в раствор альбумин или кровь, а также более точен учет и коррекция введенной дозы ИКД. Внутримышечная (в/м) инсулинотерапия проводится при невозможности в/в доступа, в отсутствии нарушений гемодинамики и при легкой форме ДКА. Доза ИКД примерно 0, 4 ЕД/кг, из них половина вводится в/в, половина – в/м, затем введение ИКД осуществляется по 5-10 ЕД/час. Недостатками введения ИКД в/м является снижение его всасывания при нарушении микроциркуляции (коллапс, прекома, кома) и дискомфорт для больного (24 в/м инъекции в сутки). При этом, если через 2 часа после начала в/м введения ИКД гликемия не снижается, необходимо переходить на в/в введение. Скорость снижения гликемии при лечении ДКА должна быть не более 4 ммоль/час. Более резкое снижение гликемии создает опасность обратного осмотического градиента между внутри- и внеклеточным пространством, осмотического дисбаланса и отека мозга. В первые сутки не следует снижать гликемию ниже 13 ммоль/л. При отсутствии снижения гликемии в первые 2-3 часа следует провести коррекцию дозы инсулина – удвоить следующую дозу ИКД до 0, 2 ЕД/кг и проверить адекватность гидратации. Если снижение гликемии составило около 4 ммоль/л в час или достигнуто снижение гликемии до 14-15 ммоль/л, необходимо уменьшить следующую дозу ИКД вдвое (0, 05 ЕД/кг), примерно 2-4 ЕД/час. При снижении гликемии ниже 4 ммоль/час рекомендуется пропустить следующую дозу ИКД и продолжить ежечасно определять гликемию. После улучшения 13 состояния, стабилизации гемодинамики, уровень гликемии не более 11-12 ммоль/л и рН>7, 3 переходят на п/к введение ИКД каждые 4-6 часов с коррекцией дозы в зависимости от гликемии в сочетании с инсулином продленного действия 1-2 раза в сутки с начальной дозы 10-12 ЕД.
Адекватная регидратация восполняет не только водный и электролитный дефицит, но и приводит к снижению гликемии, улучшает периферическую гемодинамику и почечный кровоток. При исходно нормальном уровне натрия (менее 145 мэкв/л) для регидратации применяется изотонический (0, 9%) раствор хлорида натрия, при гипернатриемии (>150 мэкв/л) используют гипотонический раствор NaCl. Скорость регидратации составляет 1 литр в 1-й час (с учетом жидкости, введенной на догоспитальном этапе), затем по 0, 5 л во 2-й и 3-й час, по 0, 25-0, 5 л в последующие часы. Скорость регидратации корректируется в зависимости от показателей центрального венозного давления и клинической картины. Объем вводимой за час жидкости не должен превышать часовой диурез более чем на 500-1000 мл. Общее количество жидкости, введенной в первые 12 часов терапии, не должно превышать 10% массы тела.
При достижении уровня глюкозы крови 13-14 ммоль/л, переходят на введение 5-10% раствора глюкозы.
Восстановление электролитных нарушений
Важным разделом терапии кетоацитодической комы является коррекция электролитных нарушений. Развитие дефицита калия в организме, снижение его внутриклеточного содержания при кетоацитодической коме обусловлено повышенной экскрецией калия с потом, вследствие осмотического диуреза. Инсулиновая терапия, регидратация, снижение гликемии, уменьшение ацидоза способствуют поступлению калия в клетку вместе с глюкозой, в обмен на ионы водорода. Явления гипокалиемии проявляются обычно через 3-4 часа после начала инсулинотерапии и введения жидкости, при тенденции к нормолизации рН. Развитие гипокалиемии может приводить к тяжелым осложнениям со стороны сердечно-сосудистой системы – тахикардия, снижение АД, нарушения ритма; дыхательной системы, а также атонии желудка, кишечника, мочевого пузыря. Если уровень К+ плазмы неизвестен, в/в инфузию калия начинают не позднее, чем через 2 часа после начала инсулинотерапии, под контролем ЭКГ и диуреза. В/в инфузию калия начинают одновременно с введением инсулина по следующей схеме: