Что будет если нагреть металл
Что будет если нагреть металл
Нагрев металлов перед ковкой является важной и ответственной операцией, от которой во многом зависит не только качество будущих деталей, но также производительность труда, работа оборудования, стойкость инструмента и себестоимость продукции.
В процессе нагрева изменяется строение металла, его свойства, состояние поверхностных слоев и др. Каждый сплав имеет температурный интервал обработки давлением и определенный режим нагрева. Нарушение указанных параметров нагрева ведет к снижению качества деталей, а возможно и к разрушению металла. Поэтому для будущего специалиста необходимо изучение явлений, происходящих в металле при нагревании.
Влияние усадки на форму и размеры поковки особенно сказывается при ковке заготовок деталей сложной формы с длинными отростками, так как усадка может привести к сильному короблению поковки. Очень важно учитывать усадку металла при изготовлении рабочих ручьев штампов для объемной штамповки, особенно при точной объемной штамповке дорогостоящих сплавов.
Образование окалины ведет к потерям металла, увеличению припусков на механическую обработку, снижает производительность труда и, являясь твердым веществам, снижает стойкость инструмента при обработке давлением и обработке резанием.
Неравномерность нагрева и выравнивание температуры по сечению заготовки. Прогрев заготовки по сечению осуществляется за счет теплопередачи от наружных слоев к внутренним. Чем меньше коэффициент теплопередачи металла, больше скорость нагрева* и площадь поперечного сечения заготовки, тем больше разность температур между наружными и внутренними слоями заготовки. Под действием высокой температуры наружные слои расширяются больше внутренних и между ними возникают большие напряжения, которые могут привести даже к разрушению. Большинство заготовок из углеродистых конструкционных сталей сечением до 100 мм «не боится» быстрого нагрева и поэтому их можно закладывать холодными в печь с температурой до 1300’С.
Высокоуглеродистые и высоколегированные стали и многие сложные сплавы имеют низкую теплопроводность и во избежание образования трещин требуют медленного нагрева. Такие стали и сплавы загружают сначала в печь, имеющую невысокую температуру, некоторое время выдерживают при этой температуре и только после прогрева всего сечения начинают дальнейший подъем температуры.
После того как наружные слои заготовки нагреются до ковочной температуры, заготовки оставляют еще некоторое время в печи для выравнивания температуры металла по всему сечению. Это время называется временем выдержки.
Ковать неравномерно нагретую заготовку опасно из-за неравномерной по его сечению деформации металла и возможного его разрушения. При объемной штамповке и ковке в подкладных штампах неравномерный нагрев приводит к незаполнению рабочего ручья штампа и к снижению стойкости инструмента.
Аналогично нагреву охлаждение поковок из легированных сталей также должно выполняться с небольшой скоростью. При быстром охлаждении возникают термические напряжения, из-за которых могут появиться трещины в поковках и привести к браку.
* Скорость нагрева представляет собой увеличение температуры заготовки в единицу времени (за одну минуту или за один час, ‘С/ч).
С понижением температуры растворимость углерода в Fey уменьшается.
* В цементите углерода содержится 6,67%.
При 723С выпадает такое количество цементита, что концентрация углерода в аустените составит 0,8%. В доэвтектоидных сталях (С
Опции темы
Такая температура абсолютно некритична. Наоборот, даже пружины, после процесса закалки, подвергают нормализации, чтобы не было излишней хрупкости.
Если мне не изменяет склероз, то при нагреве и резком охлаждении углерод напрягает кристаллическую структуру (т.к. не успевает выделиться) образуется мартензит. Закалить можно только сталь (где углерод есть). Греть газовой горелкой. Охлаждать можно и холодной водой, но желательно энергично водить деталью в воде, для «сдувания» окрижающего деталь пара. Разнизу кристаллической решетки с помешиванием и без в микроскоп видно.
Похоже, речь идёт о плоской пружине.
если после полировки нагреть железяку
Если после полировки нагреть деталь до красного свечения и опустить в холодное масло, то она точно станет железякой. Причём, на воздухе произойдёт нагар верхнего слоя и полировке сильно поплохеет.
Если, после снятия нагрузки, пружина не возвращается в исходное состояние, то или сталь плохая или нарушены режимы термообработки.
чем лучше греть небольшую деталь (до 15 см) в домашних (балконных) условиях? какой тип масла выбрать и не произойдет воспламенения масла?
В домашних условиях, лучше греть кастрюлю с супом. Термообработкой в домашних условиях, никто серьёзно не занимается.
Греть газовой горелкой.
Греть можно. Опытные термисты так делают. Только при длине детали в 150мм, возможен неравномерный нагрев. Что приведёт к напряжению в металле. После закалки, деталь желательно отпустить. Отпустить, это не значить уронить себе на ноги, а в печи, желательно в муфельной.
Может ли металл быть газом?
Да, металлы могут быть газами, в зависимости от того, насколько высока их температура кипения. Но действительно ли газообразные металлы считаются металлами?
Закройте на мгновение глаза и позвольте слову «металл» всплыть в вашей голове. А теперь ответьте: какой первый образ приходит вам на ум, когда вы думаете о «металле»?
Может ли металл быть газом?
Да, конечно! Хотя металлы обычно находятся в твердом состоянии при комнатной температуре (вероятно, поэтому мы ассоциируем слово «металл» с твердыми объектами), металлы также могут быть газами.
Дело в том, что состояния вещества универсальны: металл может быть твердым, жидким или газообразным. Но это состояние определяется на основе правильных условий температуры и давления.
Например, металл, скажем, свинец, имеет температуру кипения 1740 градусов по Цельсию. Теперь вы знаете, что свинец в своем «естественном состоянии» представляет собой твердое вещество. Но когда вы начнете его нагревать, он сначала превратится в жидкость при 327 градусах Цельсия, а если вы продолжите подавать больше тепла, он превратится в газ при 1740 градусах Цельсия.
Свинец превращается в пар при 1740 градусах Цельсия.
Но учтите, что пары ртути очень вредны. По данным Всемирной организации здравоохранения, «вдыхание паров ртути может оказывать вредное воздействие на нервную, пищеварительную и иммунную системы, легкие и почки и может быть фатальным. Неорганические соли ртути разъедают кожу, глаза и желудочно-кишечный тракт, а при попадании внутрь могут вызывать токсическое воздействие на почки«.
А теперь давайте обсудим еще один аспект этой саги о превращении металла в газ.
Остается ли металл металлом, когда он превращается в газ?
Мы установили, что металлы могут превращаться в газы, если их нагреть до точки кипения. Но если металл нагревается до точки кипения и становится газом, остается ли он металлом? Другими словами, может ли металл находиться в газообразном состоянии и при этом оставаться металлом?
Но почему металлы твердые? Что в них такого особенного, что делает их твердыми?
Почему металлы вообще твердые?
Металлы твердые при комнатной температуре из-за того, как их последовательные атомы упаковываются внутри.
Видите ли, вся материя состоит из атомов. Состояние вещества зависит от того, насколько близко или далеко друг от друга находятся эти атомы.
Если составляющие атомы вещества находятся далеко друг от друга, то это вещество будет существовать в виде газа при комнатной температуре. Атомы в жидком состоянии относительно ближе друг к другу, но в твердых телах атомы упакованы вместе в плотные кристаллы.
Из-за сильных сил, которые удерживают эти атомы близко друг к другу, твердые тела жесткие и имеют определенную форму и размер (в отличие от жидкости и газа).
Металлы твердые при комнатной температуре, потому что входящие в их состав атомы металлов упаковываются близко друг к другу, придавая им жесткий или «затвердевший» внешний вид. Это также является причиной того, что металлы имеют высокую температуру плавления и не существуют в жидком состоянии при комнатной температуре.
В целом, металлы могут превращаться в газ, но как только они превращаются в газ, они не сохраняют своих металлических свойств.
Превращения, происходящие в железе и стали при нагреве и охлаждении
Строение стали
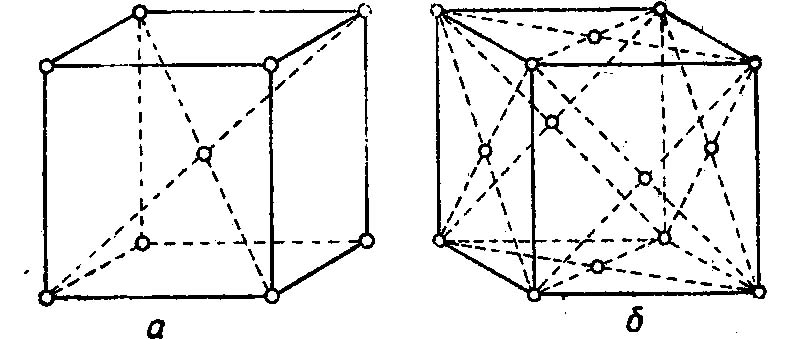
Внимательно всмотревшись в излом металла, ясно можно увидеть, что он представляет собой нагромождение (совокупность) отдельных кристаллов (зерен), крепко сцепленных между собой. Мельчайшей частицей металла, как и всякого другого вещества, является атом. В элементарных ячейках, из которых состоят кристаллы железа, атомы расположены в определенном порядке. Это расположение изменяется в зависимости от температуры нагрева. При любой температуре ниже 910° атомы в ячейках кристаллов располагаются в виде куба, образуя так называемую кристаллическую решетку альфа-железа. В этом кубе восемь атомов расположены в углах решетки и один в центре.
При нагреве свыше 910° происходит перегруппировка атомов и кристаллическая решетка представляет собою форму куба с четырнадцатью атомами; условно ее называют решеткой гамма-железа. При температуре 1390° решетка гамма-железа перестраивается в решетку с девятью атомами, носящую название дельта-железо. Эта решетка отличается от решетки альфа-железа несколько большим расстоянием между центрами атомов и сохраняется до момента расплавления железа, т. е. до 1535° (Рис. 1).
Перестройка кристаллической решетки при медленном охлаждении происходит в обратном порядке: дельта-железо при 1390° превращается в гамма-железо, а гамма-железо при 898° превращается в альфа-железо.
Рис. 1. Строение кристаллической решетки: а — альфа и дельта железа; б — гамма железа.
Критические точки превращения
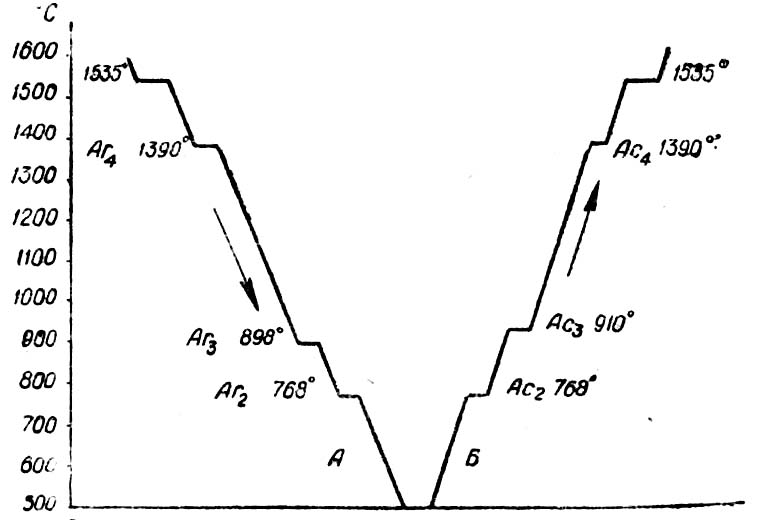
На рис.2 показаны кривые охлаждения и нагревания чистого железа. Как видно из этих кривых, в процессе перестройки одной решетки в другую, а также при расплавлении и затвердевании железа происходят температурные остановки, являющиеся результатом выделения дополнительного количества тепла при охлаждении и поглощении дополнительного количества тепла при нагревании.
Рис. 2. Кривые охлаждения и нагрева чистого железа.
Температурные остановки, при которых происходят перестройки решеток, называются критическими температурами или критическими точками и обозначаются Аrпри охлаждении и Ас при нагревании. В точках Аr2и Ас2,не происходит перестройка атомной решетки, а изменяются магнитные свойства железа. При температуре выше 768° железо теряет способность притягиваться магнитом. При очень малой скорости нагревания и охлаждения критические точки А с3и Аr3не совпадают друг с другом на 12°. При увеличении скорости охлаждения несовпадение критических точек увеличивается, так как температура значительно снижается и железо переохлаждается. Это явление, носит название гистерезис.
При нагревании и охлаждении стали происходит также перестройка атомной решетки, но температуры критических точек не постоянны. Они зависят от содержания углерода и легирующих примесей в стали, а также от скорости нагревания и охлаждения.
На рис. 3 представлена диаграмма состояния углеродистой стали при медленном охлаждении и нагревании.
Рис.3. Диаграмма состояния углеродистых сталей.
Структура стали
Структурой стали называется внутреннее ее строение. Углерод в стали находится в виде химического соединения с железом, и это соединение называется — цементит. Кроме цементита, в стали имеется феррит, представляющий собой почти чистое железо. В зависимости от содержания углерода большая или меньшая часть феррита находится в механической смеси с цементитом, образуя новую структуру — перлит. Если небольшой кусок металла прошлифовать, отполировать и протравить в специальном реактиве, то под микроскопом можно различить структуры. Ниже приводится описание структур железоуглеродистых сплавов.
Аустенит представляет собою твердый раствор углерода и других элементов в гамма-железе. Наибольшее содержание углерода, которое может раствориться в ау-стените — это 2%. Аустенит образуется при затвердевании жидкой стали и при нагреве твердой стали выше критических температур.
В обычных сталях аустенит устойчив только лишь при температуре выше критических точек. При охлаждении, даже самом быстром, с этих температур аустенит превращается в другие структуры. При комнатной температуре аустенит полностью сохраняется в ряде марок нержавеющих сталей, в высокомарганцовистой стали и в незначительном количестве остается при закалке некоторых марок инструментальной и конструкционной сталей.
Аустенит мягок, пластичен, тягуч, мало упруг. Твердость его по Бринелю находится в пределах 170—220.
Аустенит немагнитен, обладает невысокой электропроводностью.
Феррит представляет собой твердый раствор углерода и других элементов в альфа-железе. Наибольшее содержание углерода, которое может раствориться в феррите, это 0,04%. Феррит устойчив при температурах ниже критической точки AC1. Он выделяется из аустенита при медленном охлаждении последнего ниже A6i. Феррит мягок, сильно тягуч. Твердость HB= 60—100. Феррит магнитен до 768°. Свыше этой температуры он теряет магнитные свойства.
Цементит представляет собой химическое соединение железа с углеродом Fe3C—карбид железа. Цементит содержит углерода 6,67%. Выделяется из жидкого и твердого раствора при медленном охлаждении. Цементит весьма тверд и хрупок. Твердость его НB= 800—820. Он магнитен до 210°. Выше этой температуры цементит теряет магнитные свойства.
Перлит представляет собой механическую смесь феррита и цементита. Он образуется из аустенита при медленном его охлаждении. Температура превращения аустенита в перлит 723°С. При весьма медленном переходе через эту температуру цементит образуется в виде зерен (глобулей), и тогда перлит называется зернистым. При более быстром охлаждении цементит приобретает форму пластинок, и такой перлит называется пластинчатым. При весьма быстром охлаждении в результате значительного переохлаждения аустенита вместо перлита получаются другие структуры, о которых речь будет ниже.
Перлит магнитен, прочен и пластичен. Твердость его находится в пределах от 160 до 230 кг/мм 2 по Бринелю. При обработке резанием наиболее чистую поверхность дает структура зернистого перлита.
Мартенсит образуется в результате весьма быстрого охлаждения (закалки) аустенита. При быстром охлаждении успевает произойти перестройка кристаллической решетки гамма-железа в решетку альфа-железа, выделение же углерода в карбид железа не успевает произойти, и он весь остается растворенным в решетке альфа-железа. Так как нормально альфа-железо может растворить в себе не более 0,04% углерода, то такой раствор называют пересыщенным. Он отличается весьма большой твердостью (свыше Rc= 60) и хрупкостью. Следует указать, что решетка альфа-железа, получающаяся в результате закалки, имеет искаженную форму. Так, размеры ее граней не одинаковы — в одном направлении они удлинены за счет других (см. рис. 4). Такая решетка называется тетрагональной. Чем больше в стали углерода, тем больше тетрагональность решетки и тем более велики внутренние напряжения. При нагревании до температур 100—200° тетрагональность мартенсита уменьшается, форма кристаллической его решетки приближается к форме правильного куба, и вместе с этим уменьшаются внутренние напряжения. Мартенсит магнитен.
Рис. 4. Строение кристаллической решетки стали, закаленной на мартенсит.
Троостит представляет собой высокодисперсную (мелкораздробленную) смесь феррита и карбидов. Он образуется при охлаждении аустенита с замедленной против закалки скоростью или в результате нагрева (отпуска) мартенсита в пределах 250—400°.
При нагреве закаленной стали происходит постепенное выделение углерода из кристаллической решетки с образованием карбидов. Троостит менее прочен, более пластичен, чем мартенсит. Твердость его НB330—400. При охлаждении аустенита в горячих средах в интервале 250—400° (изотермическое превращение аустенита) происходит образование игольчатого троостита, несколько более прочного, чем обычный троостит.
Сорбит представляет собой дисперсную смесь феррита и карбидов. Он образуется при охлаждении аустенита с небольшой скоростью или при нагреве (отпуске) мартенсита до 400—650°. Карбиды сорбита более крупные, чем троостита. Сорбит пластичен, вязок и магнитен. Твердость НВ 270—320.
Ледебурит представляет собой эвтектическую смесь аустенита и цементита. Он содержит углерода 4 3% Образуется ледебурит при затвердевании жидкого сплава с содержанием углерода свыше 2%. Ледебурит хрупок.
На рис. 5. представлены фотоснимки структур стали с различным содержанием углерода.
Структура стали с содержанием углерода 0,83% состоит из сплошного перлита и называется эвтектоидной; при меньшем содержании углерода структура стали состоит из перлита и феррита и носит название доэвтектоидной, а при большем содержании углерода — из перлита и цементита и называется заэвтектоидной. Температура 723°, при которой перлит переходит в аустенит, также называется критической и обозначается Ас.
Для того чтобы доэвтектоидную и эвтектоидную сталь полностью отжечь, нормализовать или закалить, их нужно нагреть до такой температуры, при которой они перешли бы в аустенитное состояние.
Рис. 5. Микроструктура отожженной углеродистой стали:
Превращения, происходящие в стали при нагревании
По диаграмме на рис. 3 можно проследить за изменениями структуры трех разных марок стали при нагревании:
Линия на диаграмме, обозначенная буквами GS, соответствует окончанию растворения феррита в аустените в доэвтектоидных сталях, а линия SE соответствует окончанию растворения цементита в аустените в заэвтектоидных сталях.
Следует указать, что заэвтектоидные стали при операциях термической обработки не нагревают выше линии Аcт(такая высокая температура нагрева приведет к перегреву и ухудшению свойств стали), а ограничиваются нагревом выше первой критической точки ACl, что полностью обеспечивает получение необходимых свойств.
Превращения, происходящие в стали при медленном охлаждении
В сталях, нагретых до аустенитного состояния, при весьма медленном охлаждении произойдут обратные превращения, а именно:
а) в стали с содержанием углерода 0,83% аустенит превратится в перлит;
б) в стали с содержанием углерода 0,4% сначала из аустенита начнет выделяться феррит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит и
в) в стали с содержанием углерода 1,2% сначала из аустенита выделится цементит, а затем в районе температуры 700° оставшийся аустенит превратится в перлит.
Даже при весьма медленном охлаждении температура распада аустенита не совпадает с теми температурами, при которых аустенит образовался при нагревании. Чем скорость охлаждения больше, тем больше становится гистерезис, т. е. разница между критическими температурами (точками) при нагревании и охлаждении.
Превращения, происходящие в стали при быстром охлаждении
Рис. 6. Микроструктура закаленной стали:
а — игольчатый мартенсит;
В легированных сталях, благодаря присутствию специальных элементов, для образования мартенсита не требуется столь большой скорости охлаждения, как для углеродистых сталей, и мартенсит образуется при охлаждении в масле, а для быстрорежущих сталей — и при охлаждении на воздухе.
Троостит и сорбит можно получить не только в результате ускоренного охлаждения, нои путем нагрева закаленной стали, имеющей структуру мартенсита, до температуры ниже Aс1, т. е. путем отпуска стали. В этом случае троостит получается при нагреве стали до 400°, а сорбит—при нагреве до 650°. При нагреве до промежуточных температур получаются смешанные структуры: при нагреве от 250—400° — мартенсит и троостит и при нагреве от 400—650° — троостит и сорбит. В производственных условиях троостит и сорбит получают путем отпуска закаленной стали.
Превращения, происходящие в стали при охлаждении в среде, имеющей температуру выше 200° (изотермическое превращение)
Если деталь, нагретую выше критической точки, поместить в среду, имеющую температуру от 700 до примерно 200°, и выдержать в ней до выравнивания температуры по всему сечению, то аустенит превратится в ту структуру, которая соответствует превращению при данной температуре.
О поведении стали при изотермической обработке, выборе температуры и времени выдержки судят по кривым изотермического превращения, построенным для разных марок стали.
Рис. 7. Диаграмма изотермического превращения аустенита углеродистой стали.
На рис. 7 дан вид диаграммы изотермического превращения в стали. На горизонтальной оси отложено время начала и конца превращения, а на вертикальной— температура, при которой оно происходит. Линия А с соответствует переходу аустенита в перлит, а линия Мн — образованию мартенсита из аустенита. На кривой I начинаются, а на кривой II заканчиваются структурные превращения.
Если углеродистую инструментальную сталь, нагретую до 800°, поместить в масло, расплавленную соль или щелочь при температуре 250°, в ней образуется игольчатый троостит с высокой твердостью Rc=45—55. Если эту же сталь охладить в среде, имеющей температуру свыше 600°, в ней образуется перлит и такая сталь легко обрабатывается на станках. При охлаждении стали в среде с промежуточными температурами образуются структуры троостита и сорбита с соответствующей твердостью.
Изотермический отжиг нашел большое применение при термической обработке инструментальных сталей как процесс, резко уменьшающий время по сравнению с другими видами отжига.
Изотермическая закалка в инструментальном деле применяется редко из-за недостаточной для инструмента твердости, достигаемой при этом процессе.
Источник:
Остапенко Н.Н.,Крапивницкий Н.Н. Технология металлов. М. Высшая школа,1970г.
Каменичный И.С. Практика термической обработки инструмента. Киев, 1959 г.
3 способа самостоятельной закалки металла
Расскажем о трех способах закалки металла в домашних условиях, охлаждении и контроле качества. Как правильно провести закалку стали в масле и на открытом огне. Какое масло выбрать. Особенности закалки алюминия и меди.
Как можно закалить металл в домашних условиях, наверное, знает каждый мастер, работающий со слесарным или столярным инструментом. Считается, что для этого достаточно разогреть изделие докрасна, а затем охладить его в емкости с водой
Однако в домашней мастерской этим способом можно получить только твердый и хрупкий металл, который вполне подходит для стамесок и ножей, но непригоден для молотков, кернеров или зубил. Режимы термообработки зависят от марки стали и требуемых параметров изделия после закалки, а к ним относятся не только твердость, но и прочность, износостойкость, пластичность и вязкость.
В домашних мастерских, как правило, отсутствуют измерительные приборы, с помощью которых можно узнать температуру детали. Поэтому для того, чтобы закалить деталь, границы нагрева и отпуска приходится распознавать по цвету металла или его побежалости.
Кроме того, перед тем как закалить какое-либо изделие, мастер должен определить (хотя бы приблизительно) марку стали или сплава, из которого оно изготовлено.
Со временем накапливаются и знания, и навыки, но начинающему термисту даже для того, чтобы в домашних условиях успешно закалить сверло, резец или какой-нибудь крепеж, сначала придется пополнить свой теоретический багаж, пообщаться с опытными специалистами и сделать несколько пробных закалок.
Способы бытовой закалки металла
Чтобы закалить изделие из металла в домашних условиях, в первую очередь следует определиться со способом его разогрева до необходимой температуры, а также подобрать емкости для охлаждающих жидкостей.
Кроме того, необходимо выбрать домашнее помещение или место во дворе, где можно заниматься закалкой с соблюдением всех требований техники безопасности. Для нагревания можно использовать источники с открытым пламенем. Но таким способом удастся разогреть и закалить только небольшие по объему детали.
К тому же открытое пламя вызывает окисление и обезуглероживание, которые негативно влияют на поверхностный слой металла. Температуру нагрева домашние мастера, как правило, определяют по цвету нагретой заготовки.
На рисунке ниже приведена цветовая таблица, без которой невозможно правильно закалить изделие из углеродистой стали. Для легированных сталей температурный диапазон обычно сдвинут в сторону увеличения на 20÷50 °C.
Для наддува в кузнечном горне обычно используют промышленный фен, а в качестве топлива подойдет древесный уголь, который продается в любом супермаркете. Небольшую закрытую печь легко изготовить из пары десятков шамотных кирпичей. При этом в зависимости от метода закалки металла в ней можно не только закалить, но и провести отпуск с прогревом всего объема изделия.
Проще всего с емкостями для охлаждения и зажимным инструментом. Для закалочной жидкости подойдет любой негорючий сосуд достаточного размера, а удерживать и перемещать деталь можно щипцами или крючьями с ручками подходящей длины. На видео ниже показано, как в домашних условиях можно закалить топор с использованием самодельного горна и двух емкостей с разными охлаждающими средами.
Закалка на открытом огне
В качестве источника нагрева в таких случаях можно использовать газовую горелку, паяльную лампу или даже конфорку домашней газовой плиты. Главный недостаток такой закалки — это сложность равномерного прогрева изделия по всему объему, т. к. пламя создает высокую температуру на узком, ограниченном участке.
Этот способ подойдет, когда необходимо закалить торец удлиненного изделия, например режущую часть сверла или лезвие стамески, или же небольшую деталь размером в несколько сантиметров.
Еще одна проблема, с которой может столкнуться домашний мастер, решивший закалить углеродистую сталь открытым пламенем, — это сильное окисление и выгорание углерода в поверхностном слое железа, которые приводят к деградации его структуры.
Распространенные среды для самостоятельного каления
Для закалки сталей в домашних условиях обычно используют следующие охлаждающие среды: воздух, воду и водные растворы, минеральное масло. В качестве водных растворов обычно используют 10-15%-й хлористого натрия (поваренной соли), а минеральное масло в домашних мастерских — это чаще всего обычная моторная отработка.
Чтобы закалить отдельные части изделия с разной твердостью, используют закалку с последовательным охлаждением в двух средах. Каждая из этих закалочных сред характеризуется своей скоростью охлаждения, от которой напрямую зависит структура обрабатываемого металла.
К примеру, воздух охлаждает сталь со скоростью 5÷10 °C в секунду, масло — 140÷150 °C, а вода (в зависимости от температуры) — 700÷1400 °C.
Чтобы правильно и без проблем закалить свое изделие, необходимо знать марку металла, из которого оно изготовлено, т. к. от этого зависит как температура нагрева, так и способ охлаждения. Народные умельцы для своих изделий в качестве исходных материалов чаще всего используют б/у изделия из быстрорежущих и инструментальных сталей, которые можно закалить в домашней мастерской.
Ниже в таблице приведены рекомендуемые температурные режимы и среды охлаждения для различных сталей.
Закалка металла в масле
На производстве для закалки обычно используют индустриальное масло И-20 или современные закалочные масла типа «Термойл», «Термо» или «Волтекс». В домашних мастерских народные умельцы пользуются тем, что имеется в наличии. Чаще всего это новое или отработанное моторное масло.
Чтобы безопасно закалить деталь в таком масле в домашних условиях, нужно помнить, что у него по сравнению с промышленными закалочными жидкостями гораздо более низкая температура вспышки, и при погружении в него раскаленного металла оно на короткий срок загорается с выделением едкого дыма.
Поэтому закалочная емкость, применяемая в домашней мастерской, должна иметь минимальную открытую поверхность и использоваться только на открытом воздухе или в проветриваемом помещении. Помимо обычных ведер и жестяных банок, одна из самых распространенных конструкций такой емкости, которой пользуются домашние мастера — это удлиненный отрезок трубы подходящего диаметра с приваренным днищем.
Изготовление камеры для закаливания металла
В такой печи достигается температура свыше 1200 °C, поэтому в ней можно закалить изделия не только из углеродистой или инструментальной, но и из высоколегированной стали. При изготовлении домашних печей из шамотной глины сначала делают картонный каркас по форме и размеру рабочей камеры, который затем покрывают слоем шамота.
Поверх его наматывают нагревательную спираль, а затем накладывают основной теплоизолирующий слой. При такой конструкции область нагрева изолирована от нагревательного элемента, что важно, когда необходимо закалить сталь, чувствительную к окислам и выгоранию углерода.
Самой же распространенной конструкцией домашних закалочных печей являются установки, тепловые корпуса которых выполнены из шамотного кирпича или аналогичных ему огнеупоров. Рабочая температура у таких материалов более 1400 °C, поэтому в подобных печах можно закалить практически любой вид стали и многие тугоплавкие сплавы.
Конструктивно такая домашняя печь похожа на обычную печь на дровах, только имеет гораздо меньшие размеры. Нагрев металла в ней осуществляется с помощью электрической спирали, уложенной в пазы по периметру внутреннего пространства.
Если необходимо качественно закалить сталь, ее необходимо нагреть до точно заданной температуры, поэтому большинство таких домашних самоделок оснащено терморегуляторами (их свободно можно приобрести на «Алиэкспресс»).
На видео ниже показано устройство такой домашней печи с торцевой загрузкой и терморегулятором, который позволяет закалить сталь с точным соблюдением температурных режимов. Ее тепловой корпус изготовлен из муллитокремнеземистых огнеупорных плит ШПТ-450.
Как самостоятельно провести отпуск
Для большинства сталей (углеродистых и низколегированных), которые можно закалить в домашней мастерской, отпуск проводится при температурах в интервале от 150 до 250 °C (см. таблицу выше). В отличие от закалки такой нагрев не требует специального оборудования, поэтому многие домашние мастера используют для этих целей духовки бытовых плит с терморегуляторами.
Определить температуру нагрева при отпуске можно по цвету побежалости — разноцветной оксидной пленки, возникающей на поверхности стали при нагреве (см. рис. ниже). Если закалить сталь «на мартенсит», т. е. с быстрым охлаждением в воде, то получится очень твердая, но хрупкая структура. Поэтому отпуск является обязательной процедурой при термической обработке режущего инструмента.
Проверка качества закалки
Если на поверхности остаются бороздки, то это значит, что закалить сталь до нужного значения не получилось и ее твердость ниже этой величины. Если же надфиль скользит по поверхности закаленного металла, то его твердость в норме.
Еще один способ проверки качества домашней закалки — это царапание закаленной сталью поверхности бутылочного стекла (см. фото ниже). Кроме твердости, в домашних условиях при наличии определенных навыков можно проверить и структуру металла. Для этого необходимо закалить несколько образцов одинаковой стали в разных режимах, а затем на глаз сравнить структуру и размер зерна.
Особенности закалки алюминия
Такая потребность у домашнего мастера может возникнуть после сварки между собой деталей из алюминиевых сплавов, т. к. в этом случае они очень часто теряют жесткость в области, прилегающей к сварному шву. Но в домашних условиях закалить алюминий очень сложно, т. к. для этого нужно точно знать тип сплава и выдерживать термические параметры с точностью как минимум ±5 °C.
Охлаждение тоже требует определенных навыков, т. к. при неточном соблюдении технологии изделие может повести. Если же все-таки хочется освоить этот вид термообработки для использования в домашних условиях, то в первую очередь необходимо обзавестись печью с точным терморегулятором, а также быть готовым к тому, что каждый раз придется закаливать поочередно несколько образцов для подбора нужных параметров термического процесса.
Особенности закалки меди
Технологии термообработки стали и меди имеют принципиальные отличия. Нагрев меди до красного каления (свыше 600 °C) и быстрое охлаждение в воде приводит к ее отпусканию (т. е. она становится мягкой).
Закалить медь в домашних условиях сложнее, чем отпустить, т. к. для этого ее нужно нагреть всего до 400 °C, при которых она не имеет свечения. После нагрева до указанной температуры медное изделие медленно остужается на воздухе, после чего оно приобретает твердость, как после нагартовки.
Если все-таки есть насущная потребность закалить какое-то количество медных деталей в условиях домашней мастерской, придется обзавестись пирометром для контроля температуры нагрева.
Мы описали два способа проверки качества закалки в домашних условиях. А какие знаете вы? Поделитесь, пожалуйста, информацией в комментариях к этой статье.