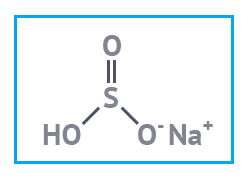
дитионит натрия что это такое
210,146 г / моль (дигидрат)
цвета, хлопья светло-лимонного цвета
1,58 г / см 3 (дигидрат)
21,9 г / 100 мл (дигидрат, 20 ° C)
СОДЕРЖАНИЕ
Состав
Подготовка
Метод боргидрида натрия подчиняется следующей стехиометрии:
Свойства и реакции
Гидролиз
Дитионит натрия стабилен в сухом состоянии, но водные растворы портятся из-за следующей реакции:
Окислительно-восстановительные реакции
Дитионит натрия реагирует с кислородом:
Эти реакции демонстрируют сложное pH-зависимое равновесие с участием бисульфита, тиосульфата и диоксида серы.
С органическими карбонилами
В присутствии альдегидов дитионит натрия реагирует либо с образованием α-гидроксисульфинатов при комнатной температуре, либо с восстановлением альдегида до соответствующего спирта при температуре выше 85 ° C. Некоторые кетоны также восстанавливаются в аналогичных условиях.
Приложения
Промышленность
Водорастворимый дитионит натрия используется в качестве восстановителя в некоторых промышленных процессах окрашивания. В случае серных красителей и кубовых красителей нерастворимый в воде краситель может быть восстановлен до водорастворимой соли щелочного металла (например, красителя индиго ).
Дитионит натрия также может использоваться для водоподготовки, газоочистки, очистки и отпарки. Он также применялся в качестве сульфирующего агента. Помимо текстильной промышленности, этот состав используется в отраслях, связанных с кожей, продуктами питания, полимерами, фотографией и многими другими, часто в качестве обесцвечивающего агента. Он даже используется внутри страны в качестве обесцвечивающего средства для белого белья, когда на него случайно попали пятна из-за того, что окрашенное белье попало в цикл стирки при высокой температуре. Обычно он выпускается в пакетиках по 5 граммов и называется гидросульфитом после устаревшего названия соли.
Лаборатория
Фотография
Безопасность
Широкое использование дитионита натрия частично объясняется его низкой токсичностью LD 50 при 2,5 г / кг (крысы, перорально).
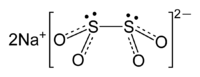
Дитионит натрия
| Дитионит натрия | |
 | |
 | |
| Общие | |
|---|---|
| Систематическое наименование | Дитионит натрия |
| Традиционные названия | Тетраоксодисульфат натрия |
| Химическая формула | Na2S2O4 |
| Физические свойства | |
| Состояние (ст. усл.) | бесцветные (белые) кристаллы |
| Молярная масса | 174,11 г/моль |
| Плотность | 2,19 г/см³ |
| Термические свойства | |
| Химические свойства | |
| Растворимость в воде | 24,1 г/100 мл |
| Классификация | |
| Рег. номер CAS | 7775-14-6 |
| Рег. номер PubChem | 24489 |
| Регистрационный номер EC | 231-890-0 |
| RTECS | JP2100000 |
Дитионит натрия — неорганическое соединение, соль щелочного металла натрия с формулой Na2S2O4, бесцветные (белые) кристаллы, растворимые в воде, образует кристаллогидрат. Ранее для него использовали неправильное название гидросульфит натрия.
Содержание
Получение
Физические свойства
Дитионит натрия образует бесцветные (белые) кристаллы.
Химические свойства
Применение
Находит применение как сильный восстановитель в химии и производстве красителей.
Литература
Ссылки
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Hg2 2+ | Pb 2+ | Sn 2+ | Cu + | Cu 2+ | |
| OH − | P | P | P | — | P | М | Н | М | Н | Н | Н | — | Н | Н | Н | Н | Н | — | — | Н | Н | Н | Н | |
| F − | P | Н | P | P | Р | М | Н | Н | М | Р | Н | Н | Н | Р | Р | М | Р | Р | М | М | Н | Р | Н | Р |
| Cl − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | Н | М | — | Н | Р |
| Br − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | Н | М | Р | H | Р |
| I − | P | P | P | P | Р | Р | Р | Р | Р | Р | ? | Р | — | Р | Р | Р | Р | Н | Н | Н | Н | М | Н | — |
| S 2− | P | P | P | P | — | Р | М | Н | Р | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| SO3 2− | P | P | P | P | Р | М | М | М | Н | ? | ? | М | ? | Н | Н | Н | М | Н | Н | Н | Н | ? | Н | ? |
| SO4 2− | P | P | P | P | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Н | Р | Р | Р |
| NO3 − | P | P | P | P | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | — | Р | Р |
| NO2 − | P | P | P | P | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? | ? | ? |
| PO4 3− | P | Н | P | P | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | ? | Н | Н | Н | Н |
| CO3 2− | М | Р | P | P | Р | Н | Н | Н | Н | — | — | Н | — | Н | Н | — | Н | Н | — | Н | — | — | ? | — |
| CH3COO − | P | Р | P | P | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | М | Р | — | Р | Р |
| CN − | P | Р | P | P | Р | Р | Р | Р | Р | ? | Н | Н | — | Н | Н | Н | Н | Н | Р | Н | Р | — | — | Н |
| SiO3 2− | H | Н | P | P | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | ? | Н | ? | ? | ? |
Полезное
Смотреть что такое «Дитионит натрия» в других словарях:
Натрия фосфаты — Известны следующие фосфаты натрия: Дигидрофосфат натрия NaH2PO4 Гидрофосфат натрия Na2HPO4 Ортофосфат натрия Na3PO4 Применение Употребляются для буферных растворов различного назначения, как эмульгаторы в пищевой промышленности … Википедия
Гидрокарбонат натрия — Гидрокарбонат натрия … Википедия
Тетраборат натрия — Минерал Tincalconite … Википедия
Хлорид натрия — Хлорид натрия … Википедия
Нитропруссид натрия — Статья инструкция. Текст данной статьи практически полностью повторяет инструкцию по применению лекарственного средства, предоставляемую его производителем. Это нарушает правило о недопустимости инструкций в энциклопедических статьях. Кроме того … Википедия
Бромид натрия — Бромид натрия … Википедия
Гидроксид натрия — Гидроксид натрия … Википедия
Карбонат натрия — Карбонат натрия … Википедия
Тиосульфат натрия — Тиосульфат натрия … Википедия
Нитрит натрия — Основные свойства … Википедия
Натрия тиосульфат (Sodium thiosulphate)
Владелец регистрационного удостоверения:
Лекарственная форма
Форма выпуска, упаковка и состав препарата Натрия тиосульфат
Раствор для в/в введения 30%.
| 1 мл | 1 амп. | |
| натрия тиосульфат | 300 мг | 3 г |
Фармакологическое действие
Фармакокинетика
После в/в введения натрия тиосульфат распределяется во внеклеточную жидкость. V d составляет 0.15 л/кг. 20-50% экзогенно введенного натрия тиосульфата выводится почками в неизмененном виде.
Т 1/2 после в/в введения 1 г натрия тиосульфата составляет приблизительно 20 мин.
Показания активных веществ препарата Натрия тиосульфат
Открыть список кодов МКБ-10
| Код МКБ-10 | Показание |
| M13.9 | Артрит неуточненный |
| M79.2 | Невралгия и неврит неуточненные |
| T50.9 | Другими и неуточненными лекарственными средствами, медикаментами и биологическими веществами |
| T56 | Токсическое действие металлов |
| T56.0 | Свинца и его соединений |
| T56.1 | Ртути и ее соединений |
| T57.0 | Мышьяка и его соединений |
| T65.0 | Токсическое действие цианидов |
| T78.4 | Аллергия неуточненная |
Режим дозирования
Применяют в/в. Дозу определяют индивидуально, в зависимости от показаний и клинической ситуации.
Побочное действие
Со стороны сердечно-сосудистой системы : снижение АД.
Со стороны нервной системы: головная боль, дезориентация, соленый привкус во рту, ощущение тепла по всему телу.
Со стороны пищеварительной системы: тошнота, рвота.
Со стороны свертывающей системы крови : удлинение времени кровотечения.
Прочие : аллергические реакции.
Противопоказания к применению
Повышенная чувствительность к натрия тиосульфату.
С осторожностью: почечная недостаточность (замедленное выведение образующихся соединений), пожилой возраст (вследствие возможного нарушения функции почек); детский и подростковый возраст до 18 лет
Применение при беременности и кормлении грудью
При беременности возможно применение по показаниям в тех случаях, когда предполагаемая польза для матери превышает потенциальный риск для плода.
Отсутствуют какие-либо данные по времени безопасного возобновления грудного вскармливания после введения натрия тиосульфата. В период грудного вскармливания следует применять с осторожностью, по жизненным показаниям.
Применение при нарушениях функции почек
Применение у детей
Применение у пожилых пациентов
С осторожностью следует применять у пожилых пациентов.
Особые указания
При отравлении цианидами рекомендуется одновременное назначение натрия нитрита, при этом натрия тиосульфат вводят после натрия нитрита.
При интоксикации цианидами следует избегать промедления при введении антидота (возможен быстрый летальный исход). Необходимо тщательно наблюдать за пациентом в течение 24-48 ч ввиду возможного возврата симптомов отравления цианидами. В случае возобновления симптомов введение натрия тиосульфата следует повторить в половинной дозе.
В период лечения необходимо контролировать показатель гемоглобина и гематокрита.
При наличии метгемоглобинемии измерения насыщения кислородом с использованием стандартных методик пульсоксиметрии и расчетных значений насыщения кислородом на основе измеренного РО 2 ненадежны.
Влияние на способность к управлению транспортными средствами и механизмами
В период лечения необходимо соблюдать осторожность при управлении автомобилем и занятиях потенциально опасными видами деятельности, требующими концентрации внимания и быстроты психомоторных реакций.
Лекарственное взаимодействие
Категорически нельзя допускать контакта натрия тиосульфата с нитратами, перманганатом калия.
Химически несовместим с гидроксикобаламином, ввиду чего их нельзя вводить через одно и то же устройство для в/в введения.
Не сообщалось о химической несовместимости натрия тиосульфата и натрия нитрита, вводимых последовательно через одну и ту же линию для в/в введения.
Натрий гидросульфит — широко востребованный в промышленности реактив
Гидросульфит натрия — неорганическое соединение, 
В природе не встречается. Получают его в результате воздействия газообразной двуокиси серы на водный раствор карбоната или гидрокарбоната (сода) натрия. Полученный раствор потом подвергается кристаллизации.
Свойства
Кристаллическое вещество белого цвета, иногда с легким желтоватым или сероватым оттенком. С резким запахом двуокиси серы. Водорастворимо. Не растворяется в спиртах, маслах, жирах. Водный раствор имеет светло-желтый цвет, иногда с коричневым оттенком. Горит, не взрывается. При нагревании выше +65 °С разлагается с выделением ядовитого сернистого ангидрида.