Глюкозиды что это сердечные гликозиды
СЕРДЕЧНЫЕ ГЛИКОЗИДЫ
Сердечные гликозиды — кардиотоннческие средства из группы стероидных О-гликозидов. В природе Сердечные гликозиды содержатся в растениях 45 видов, относящихся к различным семействам (кутровым, лилейным, лютиковым, бобовым и др.), а также в кожном яде некоторых жаб.
Растения, содержащие Сердечные гликозиды, использовали в качестве лекарственных средств и ритуальных ядов еще в глубокой древности. Простые и галеновы препараты наперстянки впервые внедрены в медицинскую практику во второй половине 18 в. английским врачом Уайтерингом (W. Withering). Большой вклад в изучение Сердечных гликозидов внесли русские ученые Е. В. Пеликан, С. П. Боткин, Н. Д. Стражеско и др.
К С. г., наиболее широко используемым в современной мед. практике, относятся препараты наперстянки (см.), напр, дигитоксин (см.), дигоксин (см.), ацетилдигитоксин (см.), целанид (см.), лантозид и др., строфанта — строфантин (см.), ландыша (см.) — коргликон и настойка ландыша, горицвета (см.) — адонизид и экстракт горицвета сухой.
Содержание
Химическое строение сердечных гликозидов
Молекула Сердечных гликозидов состоит из генинов (агликонов) и гликонов. Генины представляют собой стероидные спирты из группы производных циклопентанпергидрофенантрена, у к-рого в положении C17 имеется ненасыщенное лактонное кольцо. С наличием в структуре С. г. генинов связаны основные фармакол. свойства этих веществ. Кольца циклопентанпергидрофенантренового ядра обозначают латинскими буквами А, В, С и D. Для генинов фармакологически активных С. г. характерно наличие цис-связи между кольцами А и В, С и D, а также транссвязи между кольцами В и С. Кроме того, в молекуле генинов имеется метильная группа в положении C13 и гидроксильная группа в положении C14.
В зависимости от радикала при C10 различают генины с альдегидной, спиртовой и метильной группами. Радикалы при C5 и C17 могут быть представлены водородом или гидроксильной группой, а при C16 — различными хим. группами (рис. 1). Изменения любого из перечнеленных радикалов в генинах определяют водорастворимость и липофильность, а следовательно, полноту всасывания, скорость наступления и продолжительность действия соответствующих С. г. В зависимости от структуры лактонного кольца (рис. 2) генины подразделяют на карденолиды (с пятичленным непредельным 7-лактонным кольцом) и буфадиенолиды (с шестичленным, дважды ненасыщенным В-лактонным кольцом).
При насыщении лактонного кольца уменьшается активность и ускоряется развитие фармакологического действия С. г., а раскрытие этого кольца сопровождается инактивацией генинов.
Под гликонами в молекуле С. г. подразумевают остатки циклических сахаров, связанные через кислородный мостик с генинами в положении С3. Применяемые в медицине С. г. содержат от одного до четырех остатков сахаров, т. е. являются моно-, дио-, трио- или тетразидами. С увеличением количества остатков сахаров биол. активность С. г. понижается. В зависимости от характера гликона С. г. подразделяют по следующим критериям. По таутомерной форме моносахаридов, входящих в гликон, С. г. делят на пиранозиды (шестичленное кольцо) и фуранозиды (пятичленное кольцо). По а- или р-конфигурации полуацетального гидроксила, связанного с генином, различают альфа- и бета-гликозиды. В зависимости от природы сахарного остатка С. г. разделяют на пентазиды, гексозиды и биозиды. В состав гликонов С. г. может входить более 30 моносахаридов, многие из к-рых входят только в состав сердечных гликозидов (D-дигиталоза, D-дигиток-соза, D-цимароза и др.), а другие широко распространены в природе (D-глюкоза, L-рамноза, D-фукоза и др.). От характера гликона зависит растворимость, активность и токсичность С. г., а также степень их фиксации в тканях.
При гидролизе от молекулы С. г. отщепляются остатки сахаров. Этим объясняется образование так наз. вторичных гликозидов из первичных (генуинных), содержащихся в растительном сырье.
Свойства и механизм действия сердечных гликозидов
Сердечные гликозиды оказывают прямое избирательное действие на миокард и вызывают положительный инотропный эффект (усиление сердечных сокращений), отрицательный хронотропный эффект (урежение частоты сердцебиений), отрицательный дромотропный эффект (уменьшение проводимости) и положительный батмотропный эффект (повышение возбудимости всех элементов проводящей системы сердца, за исключением синусного узла). При применении С. г. в терапевтических дозах проявляются первые три эффекта этих препаратов и лишь частично положительный батмотропный эффект. Дромо- и батмотропный эффекты наиболее выражены при интоксикации С. г.
В основе положительного инотропного действия С. г. лежит смещение вверх кривой сила — скорость. В результате этого увеличивается способность сердца выполнять работу при данном давлении наполнения, систолическом давлении в желудочках, ударном объеме и данной изгоняемой фракции крови, укорачивается систола и уменьшается конечно-систолический объем желудочков. Положительное инотропное действие С. г. клинически выражено лишь в условиях сердечной недостаточности, когда ударный объем ограничен вследствие снижения сократимости. У здоровых лиц признаки положительного инотропного эффекта С. г. можно выявить только с помощью специальных гемодинамических исследований.
Увеличение под влиянием С. г. силы и скорости сердечных сокращений приводит к нек-рому повышению потребления кислорода здоровым сердцем. Однако при недостаточности кровообращения (см.) эти эффекты С. г. не сопровождаются увеличением потребления кислорода и субстратов окисления, поскольку С. г. существенно разгружают миокард и переводят его на энергетически более выгодный уровень работы, уменьшая объем сердца и развиваемое им напряжение.
Компенсируя по критерию изоос-мотичности увеличение внутриклеточной концентрации натрия и кальция, ионы К+ покидают кардиомиоциты. Градиент концентрации ионов К+ на мембране уменьшается, в результате чего потенциал покоя клеток сдвигается ближе к порогу деполяризации. В низких концентрациях С. г. мало изменяют величину потенциала покоя, в высоких — значительно снижают ее. В связи с этим при отравлениях С. г. увеличивается автоматизм всех элементов проводящей системы сердца (см.) и провоцируется появление эктопической активности. Неблагоприятный положительный батмотропный эффект С. г. усугубляется при гиперкальциемии, гипокалиемии, действии симпатомиметических аминов и эуфиллина. Уменьшение потенциала покоя сопровождается укорочением потенциала действия. Соответственно этому укорачивается эффективный рефрактерный период, что способствует возникновению предсердных и узловых аритмий (см. Аритмии сердца).
Отрицательное дромотропное действие С. г. проявляется уменьшением скорости атриовентрикулярной проводимости и соответствующим укорочением интервала PQ. Этот феномен обусловлен как прямым действием С. г. на миокард, так и активацией блуждающего нерва. Отрицательный дромотропный эффект С. г. является причиной развития вначале неполной, а затем и полной атриовентрикулярной блокады (см. Блокада сердца) и аритмий по механизму повторного входа возбуждения. Вместе с тем замедление атриовентрикулярной проводимости обеспечивает терапевтический эффект С. г. при суправентрикулярных тахикардиях, в т. ч. при мерцательной тахисистолии (см. Мерцательная аритмия). Внутрижелудочковую проводимость по волокнам Пуркинье, измеряемую по длительности комплекса QRS, сердечные гликозиды существенно не ухудшают.
В малых дозах С. г. оказывают отрицательное хронотропное действие в результате активации влияний блуждающего нерва на миокард. Этот эффект устраняется атропином (см.). При применении высоких доз С. г. преобладает прямое отрицательное дромотропное действие на синоатриальное соединение. Активация блуждающего нерва при влиянии С. г. осуществляется рефлекторно с барорецепторов синокаротидной и аортальной зон (синокардиальный рефлекс) и с рецепторов растяжения миокарда (так наз. эффект Бецольда, или кардио-кардиальный рефлекс Бецольда — Яриша). Одновременно снижается интенсивность рефлекса Бейнбриджа (см. Рефлексогенные зоны) вследствие уменьшения растяжения рецепторов устьев полых вен. Т. о., при сердечной недостаточности (см.) сердечные гликозиды в терапевтических дозах замедляют синусовый ритм гл. обр. в результате улучшения кровообращения.
Сердечные гликозиды вызывают более быстрое расслабление миокарда и изменяют направление процесса реполяризации, в связи с чем на ЭКГ уменьшается амплитуда зубца Т, а сегмент ST снижается ниже изолинии. Эти изменения не устраняются атропином и не являются признаком токсического действия.
Данные о влиянии С. г. на коронарное кровообращение противоречивы. В терапевтических дозах С. г. обычно не ухудшают его. Однако описаны случаи провокации приступов стенокардии (см.) под влиянием С. г.
Кардиотоническое действие всех С. г. в сопоставимых дозах идентично. Отдельные препараты С. г. отличаются друг от друга в основном фармакокинетическими параметрами (см. статьи, посвященные отдельным препаратам С. г.).
Показания и противопоказания к применению сердечных гликозидов
Основным показанием к применению С. г. является сердечная недостаточность (см.). С. г. наиболее эффективны при сердечной недостаточности, вызванной перегрузками, напр, при артериальной гипертензии, клапанных пороках сердца, атеросклеротическом кардиосклерозе. В других случаях, напр, при сдавлении опухолью устьев полых вен или обызвествленном перикарде, когда контрактильность сердца нормальна, С. г. не оказывают значимого леч. эффекта.
С. г. сравнительно мало эффективны при большинстве миокардиодистрофий (см.), кардиомиопатий (см.), миокардитов (см.), а также при аортальной недостаточности, особенно сифилитической этиологии (см. Пороки сердца приобретенные), и тиреотоксикозе (см.), если сохранен синусовый ритм, при легочном сердце (см.) без терапии основного заболевания. Однако С. г. не противопоказаны при этих заболеваниях, т. к. оказывают нек-рое лечебное действие, уменьшая симптомы сердечной декомпенсации. При острых миокардитах С. г. назначают только в уменьшенных дозах.
При приступах пароксизмальной суправентрикулярной тахикардии С. г. дают хороший профилактический и лечебный, эффект, но суправентрикулярная пароксизмальная тахикардия (см.) с атриовентрикулярной блокадой может появиться и при интоксикации С. г. Поэтому назначать С. г. можно, лишь точно зная, что ранее больные с указанной патологией не принимали эти препараты. С. г. высокоэффективны при тахисистолической форме мерцания или трепетания предсердий в сочетании с отеком легких. Желудочковая экстрасистолия (см.), возникшая на фоне лечения С. г., является одним из признаков интоксикации и требует отмены препарата. Вместе с тем экстрасистолия, связанная с перегрузкой желудочков при сердечной недостаточности, после адекватной терапии С. г. может исчезнуть.
При желудочковой тахикардии С. г. можно с осторожностью применять для лечения сопутствующей недостаточности кровообращения. Однако при появлении желудочковой тахикардии на фоне терапии С. г. необходимо отменить используемый препарат, т. к. нарушение ритма может быть следствием интоксикации С. г.
С. г. умеренно эффективны при острой левожелудочковой недостаточности разной степени, обусловленной острым инфарктом миокарда, но противопоказаны при кардиогенном шоке (см.). При остром инфаркте миокарда (см.) С. г. применяют в сниженных дозах, поскольку ишемизированные области миокарда аритмогенны. При осторожном применении в случаях острого инфаркта миокарда С. г. статистически достоверно не увеличивают ни смертность, ни количество аритмических осложнений.
При стенокардии, возникшей на фоне сердечной недостаточности и кар диомегалии, С. г. оказывают положительный эффект. Однако при отсутствии сердечной недостаточности они могут усугублять клин, проявления стенокардии и в ряде случаев провоцируют появление ее приступов. Поэтому при нестабильной стенокардии эти препараты применять нецелесообразно.
С. г. противопоказаны при идио-патическом субаортальном стенозе, т. к. вызываемое ими усиление сердечных сокращений увеличивает степень нарушения оттока крови из левого желудочка. При атриовентрикулярной блокаде второй степени С. г. противопоказаны вследствие опасности развития полной поперечной блокады, особенно на фоне приступов Морганьи — Адамса — Стокса (см. Морганьи — Адамса — Стокса синдром). Не следует применять С. г. при синдроме Вольф-фа — Паркинсона — Уайта (см. Вольффа — Паркинсона — Уайта синдром).
Во время беременности и кормления грудью С. г. необходимо назначать с осторожностью, т. к. они относительно легко проникают через плацентарный барьер и выделяются с материнским молоком.
Побочное и токсическое действие сердечных гликозидов
Различают сердечные и внесердечные проявления токсического действия С. г. Сердечные проявления интоксикации обусловлены особенностями механизма действия С. г. на миокард.
Так, вызываемое С. г. уменьшение амплитуды потенциала покоя, сопровождающееся укорочением рефрактерного периода, может явиться одной из причин фатальной фибрилляции желудочков, желудочковых и предсердных экстрасистол, часто протекающих по типу аллоритмий (вплоть до бигеминии). В связи с отрицательным дромотропным действием С. г. могут вызывать атриовентрикулярную блокаду различной степени. Для интоксикации С. г. характерны также непароксизмальные суправентрикулярные тахикардии с атриовентрикулярной блокадой. Возможна синусовая аритмия, синоатриальная блокада, остановка синусного узла, тахикардия из атриовентрикулярного соединения и политопная желудочковая тахикардия. Электрокардиографическими признаками интоксикации являются синусовая брадикардия, атриовентрикулярная диссоциация, желудочковые аритмии и суправентрикулярные аритмии с атриовентрикулярной блокадой.
К внесердечным проявлениям интоксикации относятся жел.-киш., неврологические и нек-рые другие расстройства. Нарушения функций жел.-киш. тракта (анорексия, тошнота, рвота) наиболее часто развиваются у больных, принимающих С. г. перорально. Однако в ряде случаев эти нарушения отмечаются и при внутривенном введении препаратов. К неврол. нарушениям, вызываемым С. г., относятся невралгии, головные боли и др.
При длительном приеме С. г. возможна брадикардия (см.), усугубление сердечной недостаточности, потеря веса, нарушение цветового зрения (скотома, видение в желтом или зеленом цвете, белые ореолы вокруг объектов), развитие делирия (см. Делириозный синдром), вялость, бессонница (см.), головокружение (см.).
К числу редких осложнений, вызываемых С. г., относятся гинекомастия (см.), кожные аллергические реакции, иммунная тромбоцитопения (см.). Одной из главных причин интоксикации С. г. является передозировка препаратов. Развитию интоксикации способствует изменение фармакокинетики С. г. при нек-рых патологических состояниях, напр. при гипотиреозе, почечной или печеночной недостаточности. Чувствительность к С. г. повышена у лиц пожилого возраста, а также при кардиомиопатиях, гипоксии миокарда (напр., при остром инфаркте), нарушениях кислотно-щелочного состояния, особенно при алкалозе (см.), гипомагниемии и гиперкальциемии (см.). Чаще всего развитию интоксикации С. г. способствует истощение запасов калия под влиянием салуретиков и в связи с вторичным гиперальдостеронизмом (см.). К провоцирующим аритмии факторам можно отнести также электрическую кардиоверсию.
Развитию интоксикации способствует назначение лекарственных средств, усиливающих действие С. г., напр, препаратов кальция, или средств, увеличивающих концентрацию ионов кальция в крови, напр, хинидина на фоне терапии дигоксином. Отмена препаратов, ослабляющих эффекты С. г., напр, фенобарбитала, бутадиона, холестирамина, препаратов калия, также может быть причиной усиления токсичности С. г.
При интоксикационных тахиаритмиях С. г. отменяют и назначают препараты калия, дифенин, кси-каин, бета-адреноблокаторы, напр, анаприлин. При наличии гипокалиемии (см.) назначают препараты калия, напр, калия хлорид внутрь (до 4—7 г в сутки) или внутривенно (на 5% р-ре глюкозы со скоростью 40 мэкв/час в течение 1—3 час.). Не рекомендуется назначать калий при атриовентрикулярной блокаде или гиперкалиемии. В таких случаях целесообразно применять дифенин.
Ксикаин весьма эффективен при желудочковых тахиаритмиях, возникающих при v интоксикации С. г. Однако его можно использовать только при отсутствии атриовентрикулярной блокады. В последнем случае может потребоваться применение искусственного водителя ритма (см. Кардиостимуляция). Для терапии желудочковых аритмий, вызванных С. г., нельзя пользоваться электрической кардиоверсией, т. к. она может привести к фибрилляции желудочков. При появлении фибрилляции электрическая дефибрилляция (см.) является методом выбора.
При интоксикациях Сердечными гликозидами эффективны также донаторы сульфгидрильных групп, напр. унитиол, и препараты, связывающие ионы кальция и снижающие их содержание в сыворотке крови, напр, динатриевая соль этилендиаминтетрауксусной кислоты.
Библиография: Вотчал Б. Е. и Слуцкий M: Е. Сердечные гликозиды, М., 1973, библиогр.; Гацура В. В. и Кудрин А. Н. Сердечные гликозиды в комплексной фармакотерапии недостаточности сердца, М., 1983; Машковский М. Д. Лекарственные средства, ч. 1, с. 341, М., 1977; Сивков И. И. и Кукес В. Г. Хроническая недостаточность кровообращения, Д., 1973; Сычева И. М. и Виноградов А. В. Хроническая недостаточность кровообращения, с. 72, М., 1977; Cardiac diagnosis and treatment, ed. by N. O. Fowler, p. 1009, Hagerstown, 1976; Harrison’s principles of internal medicine, ed. by K. J. Isselbacher a. o., p. 1064, N. Y., 1980; The heart, ed. by J. W. Hurst a. o., p. 1942, N. Y. a. o., 1978; Heart disease, ed. by E. Braunwald, p. 509; Philadelphia a. o., 1980; The pharmacological basis of therapeutics, ed. by A. G. Gilman а. о., N. Y., 1980.
Достижения медикаментозной терапии хронической сердечной недостаточности. Часть 1
Опубликовано в журнале:
ОБЗОРЫ ЛИТЕРАТУРЫ Сидоренко Б.А., Преображенский Д.В.
Медицинский центр Управления делами Президента Российской Федерации, Москва
Хроническая сердечная недостаточность (ХСН) является исходом многих сердечно-сосудистых заболеваний. По ракетам, распространенность ХСН в общей популяции составляет 1,5-2,0%, однако среди лиц старше 65 лет она достигает 6-10%. Несмотря на значительные достижения в лечении сердечно-сосудистых заболеваний, распространенность ХСН не только не снижается, но неуклонно возрастает. Отчасти это связано с постарением населения развитых стран мира в связи с увеличением продолжительности жизни. Ожидается, что в ближайшие 20-30 лет распространенность ХСН возрастет на 40-60%.
Ингибиторы АПФ
В 80-90-е годы было выполнено несколько десятков рандомизированных исследований, которые, в общем, подтвердили результаты исследования CONSENSUS. По сводным данным, применение ингибиторов АПФ снижает смертность больных с ХСН, в среднем на 23%, и уменьшает общее число случаев смерти и госпитализации в связи с декомпенсацией ХСН, в среднем на 35% [7].
Ингибиторы АПФ не только улучшают прогноз жизни больных с ХСН, но значительно уменьшают необходимость в их госпитализации в связи с декомпенсацией. По сводным данным 10 рандомизированных исследований, терапия ингибиторами АПФ длительностью не менее 3 месяцев уменьшает общее число случаев смерти и госпитализации в связи с декомпенсацией ХСН в среднем на 24% (р
Глюкозиды что это сердечные гликозиды
Термин сердечные гликозиды (СГ) объединяет растительные вещества и полусинтетические их производные, обладающие специфическим кардиотоническим и антиаритмическим эффектами, которые обусловлены общим механизмом действия.
Долгое время СГ применяли, как основное лекарственное средство для лечения хронической сердечной недостаточности. СГ нормализуют функции сердца, что способствует повышению ударного объема, увеличению переносимости физических нагрузок и снижению риска развития декомпенсации хронической сердечной недостаточности (ХСН). СГ ослабляют чрезмерную симпатическую активность и восстанавливают чувствительность кардиопульмональных рефлексов. Однако, несмотря на то, что кардиотоники на какое-то время улучшают качество жизни больных, продолжительность жизни не только не удлиняется, но при использовании многих «негликозидных» препаратов может даже укорачиваться (частично в результате их аритмогенного действия). В настоящее время кардиотоники все же продолжают применять, но они являются лишь одним из компонентов в комплексном лечении хронической сердечной недостаточности.
Классификация
СГ различаются по своим фармакокинетическим свойствам, которые определяют скорость развития их эффектов, продолжительность действия и способность накапливаться в организме. Узкий терапевтический индекс лекарственных средств и многочисленность факторов, изменяющих их фармакокинетику и чувствительность миокарда к ним, создает высокий риск развития токсических эффектов и обусловливает необходимость регулярного контроля за эффективностью и безопасностью терапии. Все СГ имеют в своей основе стероидное ядро с ненасыщенным лактоновым кольцом и один или несколько гликозидных остатков (сахаров). Основные фармакодинамические эффекты обусловлены стероидной структурой молекулы, а свойства сахаристой части определяют многие фармакокинетические характеристики СГ, такие как скорость и полнота всасывания, прочность связи с белками, особенности метаболизма.
Выделяют:
Также, в соответствии с фармакокинетическими свойствами все СГ делят на 3 группы: группа жирорастворимых ЛС, препараты с умеренной растворимостью в жирах и водорастворимые средства.
Представителями 1-й группы является дигитоксин и бета-ацетилдигитоксин. Ко 2-й группе относятся дигоксин, ланатозид С, метилдигоксин и мепросцилларин, к 3-й — строфантин К и ландыша гликозид.
Не все эти ЛС одинаково широко используются в клинической практике. Частота их применения зависит от степени изученности, фармакокинетических особенностей, доступности, наличия или отсутствия преимуществ перед основными представителями группы. Дигоксин и строфантин являются практически единственными СГ с наиболее изученными характеристиками.
Механизм действия
Однако назначение СГ здоровым людям не сопровождается повышением минутного выброса, так как величина последнего определяется не только силой сердечных сокращений, но и зависит от частоты сердечных сокращений, уровня пред- и посленагрузки. Рефлекторная регуляция этих гемодинамических механизмов препятствует заметному повышению минутного выброса при усилении сократимости здорового сердца. Важным дополнительным механизмом терапевтического действия СГ является их способность снижать нейрогуморальную активность симпатической нервной системы, компенсаторное повышение которой наблюдается при снижении насосной функции сердца ниже уровня, необходимого для поддержания адекватного метаболизма тканей.
Дальнейшее угнетение проводимости может привести к брадикардии или полной поперечной блокаде. Важно, что работа сердца повышается на фоне урежения сердечного ритма (отрицательное хронотропное действие) и удлинения диастолы. Это создает наиболее экономный режим работы сердца: сильные систолические сокращения сменяются достаточными периодами «отдыха» (диастолы), благоприятствующими восстановлению энергетических ресурсов в миокарде. Урежение ритма сердечных сокращений в значительной степени связано с кардио-кардиальным рефлексом.
Под воздействием сердечных гликозидов возбуждаются окончания чувствительных нервов сердца и рефлекторно, через систему блуждающих нервов возникает брадикардия. Не исключено, что определенную роль играет усиление рефлексов на сердце с механорецепторов синоаортальной зоны во время систолы в результате повышения артериального давления. На ЭКГ наблюдается увеличение интервала Р-Р. В высоких дозах СГ могут повышать активность симпатической нервной системы и прямо воздействовать на автоматизм сердечной мышцы (отрицательное дромотропное действие). Рефрактерный период предсердно-желудочкового (атриовентрикулярного) узла и предсердно-желудочкового пучка (пучок Гиса) увеличивается. Интервал Р-Q становится более продолжительным. Эти эффекты лежат в основе аритмогенного действия СГ, так как одновременное повышение автоматизма и подавление проводимости в системе Гиса—Пуркинье создают условия для развития тахиаритмий и фибрилляции желудочков. В токсических дозах сердечные гликозиды могут вызывать предсердно-желудочковый блок. Действие СГ на сосудистый тонус определяется как прямыми, так и непрямыми эффектами, которые по-разному реализуются в условиях здорового и декомпенсированного сердца. В отсутствие ХСН СГ проявляют прямое миотропное сосудосуживающее действие на артериолы и вены.
Фармакокинетика
Всасывание в организме определяется степенью растворимости СГ. Гидрофильные ЛС практически не всасываются, в связи с чем их необходимо вводить внутривенно. Биодоступность СГ, частично растворимых в жирах, во многом зависит от лекарственной формы препаратов. Наибольшей биодоступностью (до 75%) обладают эликсиры и гелевые инкапсулированные формы. Биодоступность таблетированных ЛС часто не превышает 40—60%. Прием пищи, заболевания, сопровождающиеся нарушением всасывания, и некоторые препараты могут изменять скорость и полноту всасывания СГ. Жирорастворимые СГ способны проникать во все органы и ткани. Они образуют прочные связи с белками плазмы (например, дигоксин на 30-35%, строфантин менее чем на 5%), что определяет длительную циркуляцию в кровотоке и высокую способность к кумуляции.
Период полувыведения СГ зависит от функции почек. Существует высокая корреляция между клиренсом креатинина и концентрацией дигоксина в плазме, что помогает корректировать дозы гликозидов этой группы в условиях почечной недостаточности. При сниженной функции почек дозы водорастворимых гликозидов также необходимо корректировать, поскольку они практически полностью экскретируются почками, мало подвергаясь метаболизму.
Скорость развития клинических эффектов и длительность циркуляции СГ в крови зависят от скорости и полноты всасывания, прочности связывания с белками, продолжительности биотрансформации и выраженности печеночно-кишечной циркуляции. Эффекты водорастворимых ЛС развиваются наиболее быстро, в течение нескольких минут, но длительность их пребывания в организме не превышает 1— 3 дней. Действие умеренно жирорастворимых гликозидов развивается медленнее, но они дольше циркулируют в крови и полностью выводятся из организма в течение 7 суток после прекращения приема. Жирорастворимые ЛС, обладающие выраженной способностью к кумуляции и элиминируют из организма через 3—4 недели.
Применение терапевтических доз СГ вызывает повышение концентрации ЛС в организме, продолжающееся до развития стабильного концентрационного равновесия между плазмой крови и периферическими органами и тканями, при котором проявляется полный терапевтический эффект данной дозы СГ. Это состояние, получившее название дигитализации, достигается через 3—5 Т1/2 препарата. При необходимости сократить период дигитализации в первые несколько дней лечения назначают более высокие, насыщающие, дозы с последующим переходом на поддерживающие. Схемы быстрой дигиталицации связаны с более высоким риском развития побочных и токсических явлений и требуют постоянного врачебного контроля.
Место в терапии
применяют сердечные гликозиды в кардиологии, главным образом, как сопутствующий компонент в терапии острой и хронической сердечной недостаточности. При острой сердечной недостаточности СГ вводят с коротким латентным периодом (строфантин, коргликон). Основным препаратом при хронической сердечной недостаточности является дигоксин. Иногда гликозиды (в основном препараты наперстянки) назначают при сердечных аритмиях (при фибрилляции предсердий, при пароксизмальной предсердной и узловой тахикардии). Эффективность гликозидов при указанных аритмиях связана с повышением тонуса блуждающего нерва и угнетением проведения возбуждения по проводящей системе сердца, а также зависит как от резервов самого сердца, так и от причин, лежащих в основе развития сердечной недостаточности. СГ наиболее эффективны в ситуациях, когда СН обусловлена систолической дисфункцией миокарда с дилатацией сердца и снижением фракции выброса (ФВ): постинфарктный и атеросклеротический кардиосклероз, дилатационная кардиомиопатия и др. СГ неэффективны или малоэффективны, если СН протекает с повышенным минутным объемом сердца (гипертиреоз, анемия) или обусловлена нарушением диастолической функции желудочков (митральный стеноз, амилоидоз сердца, выпотной и констриктивный перикардит) либо связана с гипертрофией левого желудочка без выраженной дилатации и снижения ФВ (как при артериальной гипертонии). СГ нецелесообразно применять при СН, вызванной инфекционным или токсическим миокардитом, активным ревматическим процессом или легочным сердцем. СГ не следует назначать не только в остром периоде ИМ, но и в раннем постинфарктном периоде, так как у больных этой категории дигоксин
является независимым фактором повышенного риска смерти. Также СГ не являются ЛС выбора для длительной терапии СН с систолической дисфункцией левого желудочка. Предпочтение, в этом случае, следует отдавать ингибиторам АПФ, которые при необходимости комбинируют с диуретиками и малыми дозами β- блокаторов. И лишь при недостаточной эффективности такой терапии больным с ХСН ФК III—IV по NYHA рекомендуется добавлять к терапии дигоксин. При внутривенном болюсном введении СГ могут увеличивать посленагрузку и вызывать сужение коронарных сосудов. Поэтому следует с большой осторожностью вводить дигоксин внутривенно не только при тяжелой СН, но и больным ишемической болезнью сердца.
Кроме того СГ возможно использовать при наличии у пациента суправентрикулярной тахиаритмии. Несмотря на то, что антиаритмическим эффектом в большей или меньшей степени обладают все СГ, при нарушениях ритма чаще всего используют дигоксин. Наиболее сильное ваготропное влияние дигоксин оказывает на синоатриальный и атриовентрикулярный узлы, поскольку именно в этих структурах парасимпатическая иннервация максимальна. В связи с этим дигоксин может быть полезен при аритмии, в возникновении которой атриовентрикулярный узел играет ключевую роль – АВ-узловая реципрокная тахикардия, фибрилляция и трепетание предсердий. При этом антиаритмический эффект дигоксина проявляется не в восстановлении ритма, а в урежении числа предсердных импульсов, которые могут быть проведены на желудочки в единицу времени. Дигоксин сохраняет свое значение в качестве лекарственного средства, обеспечивающего контроль частоты ритма желудочков у больных с тахикардическими формами наджелудочковых аритмий. Он эффективен при сочетании нарушений ритма и СН независимо от того, связана ли она с дисфункцией левого желудочка или нет, т.е. в случаях, когда другие антиаритмические ЛС, также блокирующие атриовентрикулярный узел (антагонисты кальция и β- блокаторы), могут вызвать ухудшение сердечной деятельности. Антиаритмический эффект дигоксина даже при внутривенном введении развивается достаточно медленно, в связи с чем редко используются для восстановления и поддержания ритма, отдавая предпочтение другим антиаритмикам, например, β- блокаторам, которые более эффективно контролируют желудочковый ритм, особенно при физической нагрузке.
Переносимость и побочные эффекты
Токсические эффекты СГ
При частой желудочковой экстрасистолии и пароксизмах тахиаритмии назначают препараты калия внутривенно даже в отсутствие гипокалиемии. Они противопоказаны при нарушении атриовентрикулярной проводимости и хронической почечной недостаточности. Для лечения желудочковых аритмий, вызванных дигиталисной интоксикацией и угрожающих нарушением сердечной гемодинамики применяют лидокаин (100 мг внутривенно в виде болюса) и фенитоин (100 мг внутривенно медленно, затем по 100 мг 4—6 р/сут внутрь), оказывающих минимальное действие на проводимость атриовентрикулярного узла.
Антиаритмические лекарственные средства группы хинидина могут быть полезны, но их применение связано с высоким риском развития новых аритмий и блокадой проведения. При наджелудочковых нарушениях ритма применяют β-блокаторы. При атриовентрикулярных блокадах II—III степени вводят атропин (0,5—1 мг внутривенно). Электроимпульсная терапия при интоксикации СГ малоэффективна. Для устранения дигиталисной интоксикации используют также унитиол или иммунологический способ детоксикации — введение моноклональных антител к сердечным гликозидам, нейтрализующих сам препарат. Так, к числу антидотов дигоксина относится один из таких препаратов Digoxin immune fab (Digibind).
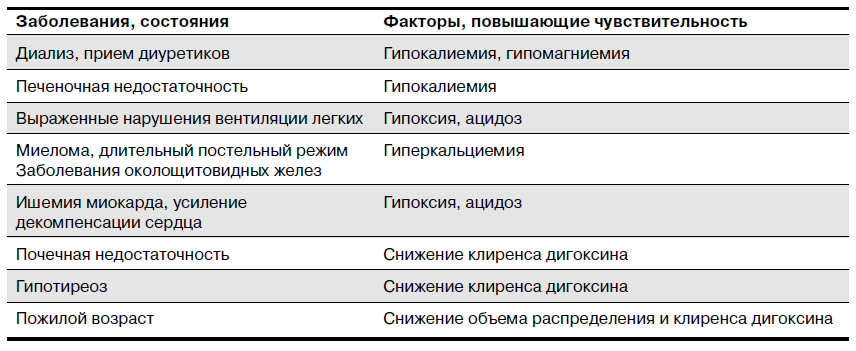
Дигиталисная интоксикация может развиться не только в результате передозировки ЛС, но и при приеме терапевтических доз вследствие повышенной чувствительности к ним или изменения их фармакокинетики. Многие заболевания и состояния способны изменять чувствительность миокарда к СГ. Выделяют заболевания и состояния, повышающие риск развития дигиталисной интоксикации.
Необходимо иметь в виду, что усиление застойных явлений, как и ишемия миокарда, может усугублять гипоксию и ацидоз и способствовать усилению токсических эффектов СГ. Если в пожилом возрасте, как правило, требуются меньшие дозы гликозидов, то детям младшего возраста (от 1 мес до 2 лет) для достижения терапевтического эффекта необходимы более высокие дозы, чем взрослым и детям младше 12 лет (в пересчете на единицу массы тела).
Это связано не только с более низкой чувствительностью миокарда детей к СГ, но и с различиями в их кинетике (объем распределения, общий и почечный клиренс). В то же время при лечении недоношенных и новорожденных детей требуются более низкие дозы гликозидов, что, возможно, связано с более низкой клубочковой фильтрацией почек в этом возрастном периоде и накоплением ЛС.
Противопоказания и предостережения
Противопоказаниями к применению сердечных гликозидов являются неполный предсердно-желудочковый блок, выраженная брадикардия, острый инфекционный миокардит, острый и ранний период инфаркта миокарда или при нестабильной стенокардии, так как состояние ишемии значительно повышает риск токсического действия на сердца.
Не следует назначать СГ для лечения фибрилляции предсердий или трепетании предсердий на фоне синдрома Вольфа—Паркинсона—Уайта, так как они способны укорачивать эффективный рефрактерный период дополнительного пучка и ускорять частоту желудочковых сокращений.
С осторожностью следует использовать сердечные гликозиды с препаратами кальция и при гипокалиемии. Это связано с тем, что при повышенном содержании ионов кальция в сыворотке крови чувствительность миокарда к сердечным гликозидам повышается и соответственно возрастает возможность токсического действия этих препаратов. Аналогичным образом меняется действие сердечных гликозидов при снижении содержания ионов калия (что может возникать при применении мочегонных средств из группы салуретиков, при диарее, в послеоперационном периоде).
Механизм действия
Однако назначение СГ здоровым людям не сопровождается повышением минутного выброса, так как величина последнего определяется не только силой сердечных сокращений, но и зависит от частоты сердечных сокращений, уровня пред- и посленагрузки. Рефлекторная регуляция этих гемодинамических механизмов препятствует заметному повышению минутного выброса при усилении сократимости здорового сердца. Важным дополнительным механизмом терапевтического действия СГ является их способность снижать нейрогуморальную активность симпатической нервной системы, компенсаторное повышение которой наблюдается при снижении насосной функции сердца ниже уровня, необходимого для поддержания адекватного метаболизма тканей.
Дальнейшее угнетение проводимости может привести к брадикардии или полной поперечной блокаде. Важно, что работа сердца повышается на фоне урежения сердечного ритма (отрицательное хронотропное действие) и удлинения диастолы. Это создает наиболее экономный режим работы сердца: сильные систолические сокращения сменяются достаточными периодами «отдыха» (диастолы), благоприятствующими восстановлению энергетических ресурсов в миокарде. Урежение ритма сердечных сокращений в значительной степени связано с кардио-кардиальным рефлексом.
Под воздействием сердечных гликозидов возбуждаются окончания чувствительных нервов сердца и рефлекторно, через систему блуждающих нервов возникает брадикардия. Не исключено, что определенную роль играет усиление рефлексов на сердце с механорецепторов синоаортальной зоны во время систолы в результате повышения артериального давления. На ЭКГ наблюдается увеличение интервала Р-Р. В высоких дозах СГ могут повышать активность симпатической нервной системы и прямо воздействовать на автоматизм сердечной мышцы (отрицательное дромотропное действие). Рефрактерный период предсердно-желудочкового (атриовентрикулярного) узла и предсердно-желудочкового пучка (пучок Гиса) увеличивается. Интервал Р-Q становится более продолжительным. Эти эффекты лежат в основе аритмогенного действия СГ, так как одновременное повышение автоматизма и подавление проводимости в системе Гиса—Пуркинье создают условия для развития тахиаритмий и фибрилляции желудочков. В токсических дозах сердечные гликозиды могут вызывать предсердно-желудочковый блок. Действие СГ на сосудистый тонус определяется как прямыми, так и непрямыми эффектами, которые по-разному реализуются в условиях здорового и декомпенсированного сердца. В отсутствие ХСН СГ проявляют прямое миотропное сосудосуживающее действие на артериолы и вены.