Грануляционная ткань что это такое в кишечнике
Доброкачественные опухоли
Толстая кишка
Толстая кишка является следующим за тонким кишечником отделом желудочно- кишечного тракта и подразделяется на слепую кишку, восходящую ободочную, поперечную ободочную, нисходящую, сигмовидную ободочную и прямую кишку.
Длина ободочной кишки 1,5—2 м, диаметр 4—6 см. Стенка толстой кишки представлена продольными мышечными волокнами, которые концентрируются в виде трех параллельных друг другу лент. Ширина каждой из них около 1 см. Они тянутся от места отхождения червеобразного отростка в слепой кишке до начальной части прямой кишки. Кишка как бы гофрируется, образуя выпячивания — гаустры. Внутренний (циркулярный) мышечный слой сплошной. Слизистая оболочка толстой кишки в отличие от тонкой кишки не имеет ворсинок. Подслизистая основа представлена рыхлой соединительной тканью, содержащей основную массу сосудов.
Восходящая ободочная кишка в правом подреберье образует печеночный изгиб и переходит в поперечную ободочную кишку длина которой составляет 50—60 см. В левом подреберье кишка образует левый (селезеночный) изгиб и переходит в нисходящую ободочную кишку. Нисходящая ободочная кишка переходит в сигмовидную ободочную кишку и далее в прямую кишку.
Функции ободочной кишки
Ободочная кишка выполяет:
Аномалии и пороки развития
Полипы и полипоз
Полипы относят к доброкачественным новообразованиям, исходящим из клеток эпителия толстой кишки, некоторые из них склонны к малигнизации (злокачественному перерождению). Полипы обнаруживают у 10—12 % проктологических больных. При проведении профилактической колоноскопии, — в 2—4 %. У мужчин полипы встречаютя в 2-3 раза чаще, чем у женщин. Полипы могут быть одиночными и множественными. Диаметр колеблется от 0,5 до 2 см, иногда они достигают 3—5 см. Полипы имеющие «ножку» свисают в просвет кишки, реже встречаются полипы на широком основании. Выделяют ювенильные, гиперпластические, аденоматозные (железистые), ворсинчатые полипы, ворсинчатые опухоли, а также множественный полипоз толстой кишки (истинный и вторичный).
Ювенильные полипы
Наблюдаются преимущественно у детей. Чаще поражается слизистая оболочка прямой кишки. Макроскопически полипы имеют вид виноградной грозди, поверхность их гладкая, окраска более интенсивная по сравнению с окружающей неизмененной слизистой оболочкой. Это типичные железисто-кистозные образования, в которых строма преобладает над железистыми элементами. Как правило, ювенильные полипы не малигнизируются.
Гиперпластические (метапластические) полипы
Мелкие (2-4 мм) образования, чаще имеют форму конуса. В них сохраняется нормальное строение слизистой оболочки кишки при значительном увеличении числа желез, за счет чего и создается впечатление об утолщении слизистой оболочки в виде полипа. Малигнизируются очень редко.
Аденоматозные (железистые) полипы
Наблюдаются в 90%. Аденоматозный полип имеет вид опухоли с гладкой поверхностью, округлой формы, располагается на ножке с широким основанием, представляет собой участок гиперплазии слизистой оболочки.. При размере более 2 см, малигнизация полипа встречается в 50% случаев.
Ворсинчатый полип (аденопапиллома)
Полипоз толстой кишки (множественные полипы)
бывает врожденным семейным и вторичным (как результат других поражений толстой кишки, например колит). Частота малигнизации достигает 70% и выше. Полипоз можно рассматривать как облигатный (обязательный) предрак. Врожденный семейный полипоз передается по наследству, поражая нескольких членов семьи. Заболевание обычно выявляют у детей и людей молодого возраста. Полипы могут локализоваться на всем протяжении желудочно-кишечного тракта. Сочетание множественного полипоза толстой кишки с доброкачественными опухолями мягких тканей и костей называют синдромом Гарднера. Сочетание полипоза пищеварительного тракта с пигментными пятнами на слизистой оболочке щек, вокруг рта и на коже ладоней называют синдромом Пейтца-Турена.
Для множественного полипоза толстой кишки характерны боли в животе без четкой локализации, понос, выделение крови и слизи с калом, похудание, анемия. Диагностику заболевания проводят на основании клинических симптомов, анамнестических данных и данных инструментального обследования.
Основным методом лечения полипов толстой кишки является хирургическое удаление полипа или части толстой кишки. Объем определяется на основании анамнеза, данных инструментального обследования и результатов гистологического исследования.
Грануляционная ткань что это такое в кишечнике
Изучение заболеваний желудочно-кишечного тракта, в частности желудка и двенадцатиперстной кишки, является основой узкого направления медицины – гастроэнтерологии. Причин возникновения заболеваний желудка множество: неправильное питание, стрессы, нарушение режима труда и отдыха, воздействие вредных веществ, активность бактерий Helicobacter pylori и т.д. [1–3]. Желудок – важный орган, отвечающий за общее состояние организма, из-за желудочных состояний страдают все системы. Поэтому важно знать причины болезней желудка, основные его заболевания. Если рассматривать заболевания желудка с ракурса онкологии, то предвестниками данной патологии могут стать часто встречающиеся в повседневной практике гастроэнтерологов язвенная болезнь желудка, острый и хронический гастрит, дуоденогастральный рефлюкс, полипы, а также эрозия желудка. В ходе мониторинга пациентов стационарного и амбулаторного лечения данная группа заболеваний желудочно-кишечного тракта занимает лидирующее положение среди расстройств, которые в совокупности различных факторов окружающей среды, а также индивидуальных особенностей чаще других приводят к канцерогенной активности. Любое предраковое заболевание развивается поэтапно с нарастанием и углублением отрицательных изменений, происходящих в желудке. На некоторых стадиях любой процесс полностью обратим, то есть болезнь излечима. По мере углубления деструкции возможность обратимости снижается, наступает стойкая хронизация процесса, а болезнь становится неизлечимой. Переходу в предрак или рак способствуют наиболее глубокие стадии, когда болезнь развивается внутри клеток. Гастрит – это одно из наиболее распространенных желудочно-кишечных заболеваний воспалительного или воспалительно-дистрофического характера, поражающих слизистую оболочку желудка [4]. В связи со множеством разновидностей этой болезни термин «гастрит» является собирательным и служит для обозначения различных по происхождению воспалительных и дистрофических изменений в слизистой этого органа. Гастриты классифицируют по нескольким показателям – по типу, локализации воспалительного процесса, этиологическому фактору, эндоскопической картине, морфологическим изменениям слизистой оболочки желудка. Все эти показатели очень важны для диагностики и выбора способа лечения заболевания. Особого внимания заслуживает атрофический гастрит – длительно текущая форма хронического заболевания, при которой происходят деструктивные изменения в слизистой оболочке желудка. В результате патологического процесса ее площадь и количество функционирующих клеток резко уменьшаются. Многие специалисты считают [5–7], что этот подвид хронического гастрита является предраковым состоянием, как следствие угроза развития злокачественного процесса очень велика. При атрофическом гастрите запускается механизм перерождения нормальных клеток желудка; главные и добавочные клетки, принимающие участие в выработке пепсиногена и хлороводородной кислоты – основных составляющих желудочного сока, перестают функционировать в оптимальном режиме. Вместо него добавочные клетки желудка в большем объеме начинают продуцировать мукополисахариды – слизь. В результате резко снижается кислотность желудочного сока. То, что клетки меняют свою специализацию и перестают выполнять основную функцию, свидетельствует о том, что в организме есть сбой в системе гормональных, иммунных, ферментных и прочих регуляторов физиологических процессов. Язвенная болезнь желудка является одной из основных причин заболеваемости и смертности среди более семи миллионов ежегодно диагностируемых патологий желудочно-кишечного тракта [8]. Диагностика язвенной болезни желудка и двенадцатиперстной кишки предполагает наличие таких симптомов, как потеря веса, перенасыщенность, боли в эпигастральной области, чувство переполнения, вздутие живота, тошнота. К сожалению, наличие данных симптомов также вписывается в клиническую картину гастроэзофагеальной рефлюксной болезни, диспепсии и гастрита, в связи с чем диагностирование язвенной болезни желудка затруднено. Бессимптомное протекание данной патологии часто не позволяет провести диагностику на ранних стадиях развития болезни, заболевание остается незамеченным вплоть до клинических проявлений, а именно кровотечений желудочно-кишечного тракта [9]. Слизистая оболочка желудка выстлана одним слоем эпителиальных клеток, который поддерживается тонкими элементами рыхлой соединительной ткани, покрытой тонким слоем гладких мышечных волокон. У многих людей желудочный эпителий, помимо собственных кислых и ферментативных выделений желудка, подвергается воздействию Helicobacter pylori. Маленькие грамотрицательные палочки Helicobacter pylori обладают уникальной приспособленностью к колонизации желудка человека [10]. Наличие данных микроаэрофильных микроорганизмов приводит к возникновению ряда субклинических и клинических показателей, которые зависят от свойств заражающего штамма, хозяина и окружающей среды [11]. Ряду пациентов с язвенной болезнью желудка или развивающейся лимфомой желудка, которые ранее подвергались лечению с использованием нестероидных противовоспалительных препаратов, показана эрадикационная терапия. Но нельзя игнорировать тот факт, что данная терапия может ухудшить гастроэзофагеальную рефлюксную болезнь и увеличить риск развития рака пищевода [12]. Желудочные полипы представляют собой аномально растущую массу клеток, которые образуются на слизистой оболочке желудка. Наличие данной патологии является редкостью, и чаще всего заболевание протекает бессимптомно [13]. Большие полипы вызывают кровотечение, анемию, боль в животе или редко могут приводить к обструкции из-за своей локализации. Только определенные типы полипов способны обладать канцерогенной активностью и увеличивать риск развития онкологии в будущем, и в зависимости от этого выбирается дальнейшая стратегия лечения, которая может включать как хирургическое удаление полипа, так и мониторинг его изменений, и консервативное лечение [14].
Оценка морфологической структуры клеток возможна с помощью цитологического исследования, которое широко применяют в клинической практике как исключительно чувствительный, точный, эффективный метод диагностики злокачественных опухолей и ряда неопухолевых поражений всех органов пищеварительной трубки у больных с симптомами заболевания органов ЖКТ, а также при скрининге в группах высокого риска по развитию рака этих органов [15]. Микроскопически злокачественные клетки выстилают желудочные железы и крипты и представляют собой эпителиальные клетки, прорывающиеся через базальную мембрану и вторгающиеся в подслизистую оболочку и мышечный слой. Отдельные клетки теряют свою дифференцированность по отношению к соседним клеткам и представлены многочисленными митотическими фигурами [16]. Для предупреждения развития онкологических заболеваний важно раннее выявление таких состояний, а также их качественное обследование. Внедрение и максимальное использование современной эндоскопической техники значительно расширило возможности цитологической диагностики органов ЖКТ и, более того, открыло перспективы применения метода, поскольку цитологический материал пригоден для проведения имеющих неоценимое дифференциально-диагностическое значение иммуноморфологических, молекулярно-биологических и генетических исследований [17, 18].
Провести сравнительный анализ и выявить характерные морфологические цитологические признаки при различных доопухолевых заболеваниях желудка.
Материал и методы исследования
Результаты исследования и их обсуждение
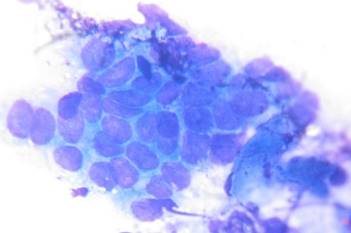
Рис. 1. Клетки покровно-ямочного эпителия с признаками гиперплазии
В случаях кишечной метаплазии в мазках-отпечатках обнаруживались высокие клетки цилиндрической, призматической или бокаловидной формы (рис. 2).
Рис. 2. Клетки покровно-ямочного эпителия с признаками кишечной метаплазии по тонкокишечному типу
Наблюдаются ядра больших и средних размеров, их расположение в клетках эксцентричное, окрашены интенсивно. Цитоплазма характеризуется базофильной окраской, у ядра и апикальной части почти прозрачная, широкая в апикальной части и узкая, более вытянутая в базальной. В исследуемых тканях имеются скопления лимфоидных элементов, а также плазматические клетки и сегментоядерные нейтрофилы. Эндоскопическая картина заживающей язвы характеризуется уменьшенной гиперемией слизистой оболочки, отсутствием некротических тканей и гнойных масс. Исчезает глубина язвы, воспаленные края язвы сглаживаются, формируется «красный рубец» – гиперемированная ткань слизистой оболочки, которая впоследствии после втяжения стенок формирует соединительнотканный «белый рубец» [23, 24]. Микроскопическое строение слизистой оболочки зависит от периода развития язвы. В цитологических мазках определяли десквамированные клетки эпителия, лейкоциты и эритроциты, фибробласты, гистиоциты, плазматические клетки и лимфоциты. Непосредственно по краю хронической язвы слизистая оболочка желудка подвергается значительному утолщению за счет интенсивной пролиферации ямочного эпителия. В цитологических препаратах можно найти все упомянутые выше клеточные элементы. В материале, полученном с краев хронической язвы, обычно обнаруживали полиморфные, различной степени зрелости клетки покровно-ямочного эпителия. Преобладание незрелых крупных клеток с большими ядрами и базофильной цитоплазмой может свидетельствовать об интенсивной пролиферации эпителия. В период обострения язвы в большом количестве встречаются дегенеративно измененные эпителиальные клетки без четких границ с укрупненными ядрами. Рисунок хроматина в них разреженный, в виде грубых волокон. В связи с большим клеточным распадом и явлениями цитолиза в материале, особенно полученном со дна язвы, можно видеть много «голых» ядер. В этих препаратах преобладали сегментоядерные лейкоциты и в значительном количестве встречаются элементы грануляционной ткани. В период рубцевания язвы в мазки попадают очень полиморфные клетки гистиоцитарного типа, которые бывает трудно отличить от атипических эпителиальных клеток [25]. В ходе эндоскопического исследования полипов оценивались количество, форма, размеры, поверхность, цвет, консистенция, воспалительные процессы и локализация новообразований. Цитологические препараты характеризовались большим количеством пластов и скоплений покровно-ямочного эпителия. При аденоматозных полипах встречаются также и железистоподобные структуры. По сравнению с цитологическими описаниями гастритов при этих заболеваниях отмечалось преимущество незрелых клеток, ядра светлые, укрупнены, рисунок хроматина нежно-сетчатый. Клетки эпителия желез и лимфоидные элементы определяются в небольшом количестве. В случаях грануляционных полипов с обильными воспалительными инфильтратами в их строме в цитологические препараты могут попадать в значительном количестве нейтрофильные лейкоциты.
В ходе проведенных исследований выявлены изменения в составе и морфологии клеток слизистой оболочки желудка, которые наблюдаются при гастрите, полипозе и язве, не являются строго специфическими. При всех этих заболеваниях может определяться различная степень пролиферации покровно-ямочного эпителия: в одних наблюдениях отмечается только незначительный полиморфизм эпителиальных клеток, в других – явно преобладают молодые элементы с некоторыми признаками атипии. Для установления диагноза необходимо применять дополнительные методы исследования, так как на основании только цитологических данных не представляется возможным диагностировать эти процессы.
Полипы и полипоз толстой кишки
Полипы и аденомы по своей сути являются опухолями кишечника.
Опухоль – это новообразованная ткань.
Причиной возникновения опухолей является генетическая патология, в результате которой в клетке нарушается правильный и адекватный рост и она начинает безудержно развиваться, причем с нарушением своей дифференцировки.
Все опухоли по характеру своего роста делятся на злокачественные и доброкачественные.
Что такое «полип»?
Полип – это разрастание железистого эпителия.
По своей форме полипы могут быть в виде шляпки гриба на тонкой или на толстой ножке.
Причины образования полипов
Установить точную причину возникновения полипа в том или ином случае довольно трудно, так как зачастую они никак не проявляются. Чаще всего такие доброкачественные полипы обнаруживаются случайно.
Такие пациенты обычно обращаются к врачу с жалобами на нарушение функции кишечника, чувство дискомфорта, боли в области заднего прохода, иногда на патологические выделения в виде крови или гноя со слизью.
Такие симптомы характерны и для других заболеваний прямой и толстой кишки, например, проктита, геморроя, анальной трещины, колита, рака прямой или толстой кишки и т.д.
Встречаемость
Но, конечно, истинная частота возникновения полипов толстой кишки выше, так как при этом обследовании исследователи не осматривали другие отделы толстой кишки, в которых располагается около 50 % всех полипов и аденом толстой кишки.
Среди причин или точнее факторов, которые влияют на появление полипов толстой кишки, можно отметить состояние экологии, а также гиподинамию. Не менее важным фактором образования полипов толстой кишки является характер питания.
Как известно, в современных экономически развитых странах у людей в рационе преобладают продукты, богатые жиром и углеводами, а количество растительной клетчатки низкое. Это становится причиной плохой моторики толстой кишки, застое в ней каловых масс, желчных кислот, которые оказывают влияние на слизистую кишечника.
Это в свою очередь влияет на состав естественной микрофлоры толстого кишечника, что также отражается на состав ферментов, которые она выделяет.
Исследователи также нашли взаимосвязь между образованием полипов и такими факторами, как мужской пол, атеросклероз сосудов, злокачественные опухоли, дивертикулы в ЖКТ, а также воспалительные заболевания кишечника.
Классификация доброкачественных опухолей толстой кишки
Все доброкачественные опухоли толстой кишки можно разделить на:
2. Аденоматоз (аденоматозный полипоз кишечника)
Опухолеподобные поражения. К ним относятся:
2. Гетеротопии
3. Воспалительный полип
4. Гиперпластический (метапластический) полип
5. Доброкачественный лимфоидный полип и полипоз
6. Глубокий кистозный колит
7. Эндометриоз
Для гиперпластического полипа характерны мелкие размеры (до половины сантиметра). Он немного возвышаются над уровнем слизистой и представляют собой разрастание мягкой консистенции и обычного цвета.
Для железистых и железисто-ворсинчатых полипов характерны более крупные размеры (до 2-3 см в диаметре). Как правило такие полипы имеют ножку, иногда даже широкое основание. Цвет таких полипов обычный, как и цвет слизистой толстой кишки, но по своей консистенции они могут быть плотнее. Нередко такие полипы могут изъязвляться или кровоточить.
Для ворсинчатых аденом характернo дольчатое строение. Такая поверхность внешне напоминает ягоду малины. Размеры таких полипов больше, чем у тубулярной аденомы.
Классификация полипов
Самым частым типом всех доброкачественных опухолей толстой кишки являются эпителиальные опухоли. Они встречаются в 92% случаев всех доброкачественных новообразований. Причем именно железистые опухоли в наибольшей степени подвержены злокачественному перерождению – малигнизации.
По своему гистологическому строению полипы толстой кишки делятся на:
Отмечено, что величина полипа влияет на риск его малигнизации – чем она больше, чем выше риск злокачественного перерождения полипа.
Кроме того, полипы толстой кишки могут быть:
Различают также диффузный (семейный) полипоз.
При семейном полипозе риск злокачественного перерождения довольно значительный и достигает 80-100%.
Ворсинчатая опухоль обычно при внешнем осмотре (посредством ректороманоскопии или колоноскопии) бывает красноватого цвета благодаря обилию кровеносных сосудов в ней. Такие сосудики обычно легко травмируются и кровоточат, что важно учитывать, так как это не является признаком малигнизации, а лишь характерной их особенностью.
Проявления полипов толстой и прямой кишки
Чаще всего доброкачественные новообразования прямой и толстой кишки у пациентов протекают бессимптомно, либо выявляются случайно при эндоскопическом исследовании (колоноскопии, ректороманоскопии) по поводу других заболеваний.
Если же полип достигает более крупных размеров (до 2-3 см), то появляются патологические выделения (кровянистые, слизистые). Пациенты могут жаловаться на появление чувства дискомфорта в животе и в заднем проходе, на боли. Появляются нарушения моторики кишечника, например, запор или понос.
Итак, основными проявлениями полипов толстой кишки являются:
Диагностика полипов прямой и толстой кишки
Почти все виды рака прямой или толстой кишки возникают изначально на фоне полипов. Но полипы растут довольно медленно, обычно в течение нескольких лет. Поэтому очень важная роль в профилактике раковых заболеваний толстого кишечника принадлежит методам исследования. Выявление малигнизации полипа на ранней его стадии обеспечивает успех его излечения в 90%.
Самым первым методом исследования в проктологии является пальцевое ректальное исследование.
Этот метод позволяет врачу оценить состояние участка прямой кишки до 10 см от края заднего прохода. Это исследование должно применяться всегда. Пальцевое ректальное исследование позволяет выявить и другие заболевания прямой кишки, такие как геморрой, ректальные свищи, анальные трещины. Кроме того, такое исследование позволяет определить состояние простаты у мужчин, выявить заболевания окружающей клетчатки (кисты и опухоли).
Далее следует другой, не менее важный метод диагностики при заболеваниях толстой и прямой кишки – ректороманоскопия.
Перед тем как проводить ректороманоскопию пациенту проводится очистительная клизма, назначаются слабительные. Метод ректороманоскопии не могут заменить никакие другие методы, такие как рентгеноскопия, УЗИ и т.д., так как он позволяет врачу увить «воочию» наличие полипов и оценить состояние стенки прямой кишки.
Известно, что более половины всех полипов толстой кишки локализуется в прямой и сигмовидной кишках, т. е. их можно выявить ректоскопом.
Если полипы выявлены в сигмовидной кишке, рекомендуется провести исследование более высоких отделов толстой кишки, так как довольно часто такие полипы сочетаются полипами в других отделах ЖКТ.
Колоноскопия – это эндоскопический метод исследования толстой кишки. Он отличается от ректороманоскопии тем, что в этом случае используется более длинная гибкая трубка, которая вводится в прямую кишку и продвигается выше сигмовидной кишки. Для проведения колоноскопии требуется тщательная подготовка больного клизмами.
Анализ кала на скрытую кровь: это важный метод исследования патологии ЖКТ. Он заключается в исследовании кала на наличие компонентов крови. Для его проведения нужно следовать инструкциям врача. Они заключаются в том, что накануне перед анализом нельзя чистить зубы, принимать некоторые препараты (в частности препараты железа). Анализ кала на скрытую кровь не является специфичным для полипов. Полипы могут вообще не кровоточить, а наличие крови в кале может быть и при многих других заболеваниях прямой и толстой кишки, о которых мы уже упоминали.
Среди новых методов исследования ЖКТ на наличие полипов и других новообразований можно отметить компьютерную томографию.
Гиперпластические полипы обычно представляют собой мелкие разрастания размером о,5 см, которые возвышаются над слизистой толстой кишки. Они обладают мягкой консистенцией и дня них характерен обычный цвет.
Для аденоматозных полипов характерно то, что они могут достигать размеров до 2-3 см, быть на ножке или на широком основании. По своему цвету они похожи на слизистую кишки, а вот консистенция у них более плотная.
Аденопапилломатозные полипы (железисто-ворсинчатые) обычно бывают более 1 см в размере. Они имеет бархатистую поверхность, которая иногда может быть мелкодольчатой. Такие полипы могут эрозироваться и кровоточить.
Гипертрофические и келоидные рубцы
Рубцы это результат замещения поврежденных собственных тканей на грубую соединительную в результате оперативных вмешательств и различных травмирующих факторов (механических, температурных, химических, ионизирующего излучения, глубокого
Рубцы это результат замещения поврежденных собственных тканей на грубую соединительную в результате оперативных вмешательств и различных травмирующих факторов (механических, температурных, химических, ионизирующего излучения, глубокого деструктивного воспаления и т. д.) [1, 2, 3]. Рубцы, являясь выраженным косметическим недостатком, часто приводят к психоэмоциональному дискомфорту, а также к развитию психосоциальной дезадаптации и снижению качества жизни.
Формирование рубца проходит несколько стадий:
Образование рубца происходит в основном за счет внеклеточного матрикса, в частности с помощью коллагена. Внеклеточный матрикс — это супромолекулярный комплекс, включающий химические соединения различного типа (белки, полисахариды, протеогликаны и прочие). Его можно сравнить с гелем, в котором «плавают» волокнистые протеины (коллагены и эластин) и вязкие протеины (фибронектин, ламинин), обеспечивающие взаимосвязи молекул друг с другом и с поверхностями клеток [2, 9, 14, 17]. Из всех протеинов коллагены составляют основной компонент внеклеточного матрикса и являются наиболее распространенными протеинами организма, занимая около 1/3 части всех его белков. Это нерастворимые в воде внеклеточные гликопротеины, синтезируемые фибробластами, хондробластами и остеобластами. Из-за формы белковой молекулы коллагены относят к фибриллярным белкам [16]. Рост избыточного внеклеточного матрикса в рубце происходит в результате деятельности «раневых» фибробластов. В интактной (здоровой) коже фибробласты отвечают за ремодулирование компонентов дермы, они разрушают старый коллаген и откладывают новый. При ранениях, травмах, ожогах и оперативных вмешательствах в ранах появляются миофибробласты, которые стремятся «заделать брешь» в тканях, усиленно откладывая компоненты внеклеточного матрикса: коллаген, гликозаминогликаны, эластин и другие белки. Именно из-за пролиферации фибробластов и продуцирования ими избыточного внеклеточного матрикса и происходит рост рубцов [2,19].
Можно выделить следующие разновидности рубцов: нормотрофические, гипертрофические и атрофические. При нормальном физиологическом процессе происходит формирование нормотрофического рубца. Это плоские рубцы светлого цвета с нормальной или сниженной чувствительностью и эластичностью, близкой к нормальным тканям. Такие рубцы являются оптимальными. В типичной ране спустя 6–8 недель после повреждения устанавливается равновесие между анаболическими и катаболическими процессами. В этой стадии, прочность раны составляет приблизительно 30–40% прочности здоровой кожи. С развитием рубца предел его прочности увеличивается в результате прогрессивных связей волокон коллагена.
При избыточной реакции соединительной ткани на травму на фоне неблагоприятных условий заживления (воспаление, растяжение рубца и т. д.) формируются гипертрофические рубцы. В условиях гипоксии и воспаления происходит активизация фибробластов биологически активными веществами. Появляются недифференцированные, патологические, функционально активные клетки с высоким уровнем синтеза коллагена. Образование коллагена преобладает над его распадом из-за уменьшения выработки коллагеназы, специфического фермента, разрушающего коллаген, вследствие чего развивается мощный фиброз тканей в виде гипертрофических или келоидных рубцов. Гипертрофические рубцы часто объединяют в общую с келоидными рубцами группу в связи с тем, что оба вида отличаются избыточным образованием фиброзной ткани и возникают в результате неадекватного воспаления, присоединения вторичной инфекции, снижения местных иммунологических реакций и т. д. Однако имеются и существенные различия, на основании которых проводится дифференциальная диагностика между этими двумя видами рубцов, которые будут упоминаться ниже [3].
Атрофические рубцы возникают в результате сниженной реакции соединительной ткани на травму. Коллагена образуется недостаточно. Атрофические рубцы располагаются ниже уровня окружающей кожи (западают). При небольшой ширине они практически не отличаются от нормотрофических. Нередко атрофические рубцы возникают на местах бывших эксфолиаций (угревой болезни) — так называемое «постакне».
Келоид (keloidum: греч. kele выбухание, припухлость + eidos вид; син.: Алибера келоид) — плотное разрастание соединительной ткани кожи, напоминающее опухоль [2]. Келоидные рубцы развиваются как следствие извращенной реакции тканей на травму, это особая, наиболее тяжелая группа рубцов, отличающихся от других по виду и патогенезу. Как правило, келоиды образуются на фоне сниженных показателей общего и тканевого иммунитета. При исследовании келоидной ткани обнаруживаются чрезвычайно активные фибробласты, степень их активности в 4 раза выше, чем у клеток при нормальном процессе заживления [9]. Коллаген (большей частью незрелый) располагается в виде широких рыхлых пучков и узлов, эластин отсутствует. Келоидный рубец имеет упругую консистенцию, неровную, слегка морщинистую поверхность. Келоид принято классифицировать на истинный и ложный. Истинный (самопроизвольный) келоидный рубец возникает спонтанно без каких-либо предпосылок, чаще на коже груди, по наружной поверхности верхней трети плеча, в редких случаях — по всему телу. Ложный келоид может развиваться в любом месте, где до этого наблюдалась травма кожных покровов (механическая, ожог и т. д.). Например, казуистический случай наблюдали Chawla B., Agarwal A., Kashyap S. (2007), которые диагностировали келоидное образование на роговице глаза после операции. В настоящее время данная классификация носит относительный характер. Большинство исследователей полагают, что самопроизвольному келоиду предшествует микротравматизация кожи и этиологически он ничем не отличается от ложного (по патогенезу и морфологии эти рубцы абсолютно идентичны) [2]. Келоид на месте ссадин или царапин представляет собой возвышение. Цвет и интенсивность окраски зависит от степени васкуляризации (ярко-розовый, бледный, цианотичный). Для келоидного рубца характерен пульсирующий рост, подобно приливу-отливу. Рубцовая ткань при келоиде простирается за границы первоначальной раны, обычно не регрессирует спонтанно и имеет тенденцию рецидивировать после иссечения.
Теоретически келоид может появляться в любом возрасте, но чаще развивается во время и после пубертата. Юные индивидуумы более часто травмируются, и молодая кожа создает большее натяжение, в то время как кожа пожилых менее эластична и более регидна. Уровень синтеза коллагена также выше в более молодом возрасте. В настоящее время определен средний возраст пациентов — 25,8 (22,3 у женщин и 22,6 у мужчин) [5].
Обычно диагностика келоида не представляет трудностей. Gulamhuseinwala N., Mackey S., Meagher P. (2008), проведшие ретроспективное исследование 568 пациентов с келоидами, установили, что клинический диагноз совпадал с гистологическим в 94% случаев. Однако при дебюте возникновения рубцов встает вопрос дифференциального диагноза между гипертрофическим рубцом и келоидом. Как уже упоминалось выше, имеются существенные различия между этими видами рубцов. Рост гипертрофического рубца начинается сразу же после заживления и характеризуется образованием «плюс ткани», по площади равной раневой поверхности, в то время как границы келоида всегда выходят за зону повреждения. При гипертрофическом рубце субъективные ощущения отсутствуют или незначительные. Келоидные образования вызывают различные субъективные ощущения (зуд, боль, чувство стянутости кожи, парастезии и т. д.). Изменение цвета гипертрофического рубца от розового до белесоватого происходит в те же сроки, что и у нормотрофических рубцов, и со временем они заметно уплощаются. Келоид остается насыщенного цвета и спонтанно не регрессирует. Обычно у одного больного наблюдается несколько келоидных образований. Келоидный рубец чаще встречается у людей в возрасте 10–30 лет, в то время как гипертрофические шрамы могут возникнуть в любом возрасте. Морфологическая картина также имеет существенные различия. Известно, что синтез коллагена в келоидах приблизительно в 8 раз выше, чем в гипертрофических рубцах, что объясняет меньшее количественное содержание коллагеновых волокон в гипертрофических рубцах, а следовательно, и массу рубца. В гипертрофических рубцах клеток фибропластического ряда меньше, чем в келоидных, отсутствуют гигантские, незрелые формы «зоны роста» [1, 7, 8, 9, 12, 21].
Исследователями отмечена неодинаковая частота локализации келоидообразования у лиц имеющих, различную расовую принадлежность. Например, у белокожих келоид чаще образуется на лице (щека и ушная раковина), верхних конечностях и стернальной области; а у азиатов стернальная область почти не поражается, у чернокожих наряду с ушной раковиной и шеей чаще затрагиваются нижние конечности [5]. Это дало предположение о ведущей роли наследственности келоидообразования. Однако до настоящего времени никакой определенный ген или набор генов не был идентифицирован как отвечающий за развитие келоида [5, 8]. Кроме того, не выявлены никакие существенные различия между ДНК-фибробластами келоида и ДНК-фибробластами нормальной кожи. Это предполагает, что в развитии келоидообразования имеет значение не увеличение числа фибробластов, производящих нормальное количество коллагена, а то, что каждый фибробласт производит больше коллагена, чем необходимо для восстановления раны [13].
Лечение келоида и гипертрофических рубцов
Первое правило при лечении келоида и гипертрофических рубцов — это их предупреждение. Во-первых, необходимо избегать ненужной косметической хирургии у пациентов, предрасположенных к образованию келоида и грубых рубцов. Возможным исключением может быть обезображивающий келоид на ушной раковине. Если операции не избежать, то закрытие всех хирургических ран должно происходить с минимальным натяжением по складкам кожи, когда это возможно. Желательно, чтобы разрезы не проходили через поверхность суставов и в средней части груди.
Методы лечения келоида и гипертрофических шрамов можно разделить на несколько групп:
Лекарственные средства
Кортикостероиды. Внутрирубцовое введение стероидов остается основой лечения. Кортикостероиды уменьшают рубцеобразование посредством уменьшения синтеза коллагена, глюкозаминогликанов, медиаторов воспаления и пролиферации фибробластов в процессе заживления раны. Наиболее часто используемый кортикостероид — триамцинолона ацетат в концентрации 10–40 мг/мл, назначаемый в зону повреждения посредством введения иглой с интервалом 4–6 недель. Эффективность такого введения, как мономодели и как добавление к процедуре эксцизии рубца, очень высока. Также широко применяются топические кортикостероидные средства, которые наносятся ежедневно непосредственно на образование. Осложнения при лечении кортикостероидами включают атрофию, телеангиоэктазии и нарушения пигментации.
Иммуномодуляторы. Новым методом в лечении келоидных и гипертрофических рубцов является терапия интерфероном. Интерферон, введенный в линию шва, после иссечения келоидного рубца может профилактически предотвращать рецидивы. Рекомендуется вводить по 0,5–1,0 млн. МЕ через день 2–3 недели, затем по 0,1–0,5 млн. МЕ 1–2 раза в неделю в течение трех месяцев.
Препараты, уменьшающие гиперпролиферацию клеток соединительной ткани. Классическим средством для лечения рубцов является гиалуронидаза. Гиалуронидаза расщепляет основной компонент межуточного вещества соединительной ткани — гиалуроновую кислоту, являющуюся цементирующим веществом соединительной ткани, и, таким образом, повышает тканевую и сосудистую проницаемость, облегчает движение жидкостей в межтканевых пространствах; уменьшает отечность ткани, размягчает и уплощает рубцы, предупреждает их формирование. Препараты, содержащие гиалуронидазу (Лидаза и Ронидаза), получают из семенников крупного рогатого скота. Раствор Лидазы (1 мл) вводят в этих случаях вблизи места поражения под кожу или под рубцово-измененные ткани. Инъекции производят ежедневно или через день; курс лечения состоит из 6–10–15 и более инъекций. При необходимости проводят повторные курсы с промежутками 1, 5–2 мес.
Новым ферментным препаратом для лечения заболеваний, сопровождающихся ростом соединительной ткани, является «Лонгидаза». «Лонгидаза» это химическое соединение гиолуронидазы с полиоксидонием. Сочетание ферментативной активности гиалуронидазы с иммуномодулирующими, антиоксидантными и умеренными противовоспалительными свойствами полиоксидония, обеспечивает широту фармакологических свойств. Наиболее эффективно использовать препарат «Лонгидаза» методом ультрофонофореза или фонофореза. При ультрофонофорезе Лонгидаза 3000 МЕ разводится в 2–5 мл геля для ультразвуковой терапии. Воздействие осуществляется малым ультразвуковым излучателем (1 см2), с частотой ультразвука 1 МГц, интенсивностью 0,2–0,4 Вт/см2, в непрерывном режиме, время воздействия 5–7 мин., курс 10–12 процедур ежедневно или через 1 день. Методом фонофореза (1500 Гц) 3000 МЕ Лонгидазы вводится ежедневно (общее время воздействия 5 мин., курс — 10 процедур). Также возможно введение препарата внутрь рубца:
Хорошо известным препаратом, тормозящим пролиферацию клеток соединительной ткани и одновременно оказывающим противовоспалительный эффект, является Контрактубекс. В течение многих лет Контрактубекс применяется в хирургии и косметологии в лечении послеоперационных и послеожоговых рубцов, в том числе грубых, препятствующих движению и келоидных, а также растяжек (стрий) после родов или после резкого снижения веса.
Ферментный препарат из 9 коллагенолитических протеаз «Ферменкол» представляет собой принципиально новый протеолититческий препарат. Противорубцовый эффект Ферменкола основан на редукции избыточного внеклеточного матрикса в рубцовой ткани. Эффект при использовании противорубцовых средств наблюдается примерно через 3 недели после начала применения средства и достигает оптимального результата обычно после 2–3 курсов электрофореза или фонофореза, по 10–15 сеансов или аппликаций в течение 30–60 дней.
Физические и физиотерапевтические методы
С разным успехом в лечении гипертрофических рубцов и келоида применяются силиконовые пластинки и силиконовые обтурирующие повязки. При применении силиконовых повязок в большей степени эффект проявляется в результате комбинации давления и гидрации поверхности, чем эффект от самого силикона. Исследования показывают, что действенность таких повязок при их использовании 24 часа в сутки в течение 12 месяцев наблюдалась только у ≈1/3 пациентов [20]. Метод сжатие/давление, достигаемый с помощью силиконовых пластин, вызывает истончение кожи. В одном исследовании прикладывание двух пластин к ушным мочкам после удаления келоида предотвращало его рецидивирование в срок от 8 месяцев до 4 лет. Выраженным дискомфортом метода является необходимость ношения повязок/пластинок в течение суток, а также невозможность их прикрепления в некоторых анатомических областях (сгибы, шея и т. д.). Другие устройства (специальное компрессионное белье и пластырь с оксидом цинка) также используются от 12 до 24 часов в день в течение 8–12 месяцев, что является явным недостатком метода. По данным различных авторов, эффективность их не превышает 40% [4, 5].
Криохирургия. Криохирургические средства, такие как жидкий азот, поражают микроциркуляторное русло и вызывают гибель клеток через образование внутриклеточных кристаллов. Обычно 1–3 цикла замораживания-оттаивания по 10–30 секунд достаточно для достижения желательного эффекта. Особое внимание следует уделять кратковременности аппликаций жидкого азота, чтобы избежать появления обратимых гипопигментаций. Следует учитывать, что криотерапия может быть болезненной и вызывать депигментацию. Более перспективным методом является комбинированное воздействие криотерапией и кортикостероидами [15]. Простым и эффективным методом облегчения внутрирубцового введения стероидов является очень легкое криовоздействие, предшествующее введению, — этот шаг вызовет отек ткани и последующее клеточное и коллагеновое разрушение. Жидкий азот наносится на 5–15 секунд, не доводя кожу до замерзания. Такая техника позволяет лучше распределить препарат в келоидной ткани и минимизировать его проникновение в окружающие ткани.
Лазерная терапия. Аргоновый лазер (488 nm) сходен с углекислым лазером, может способствовать сокращению коллагена за счет локального нагрева. Импульсный лазер на красителях (585 nm) вызывает процесс фототермолиза, приводящий к микроваскулярному тромбозу. В начале 1980-х годов авторы отметили, что при применении импульсного лазера на красителях рубцы становятся менее эритематозными, более мягкими и менее гипертрофическими. Лазерная обработка келоида и гипертрофического рубца при использовании углекислого лазера (10,600 nm) может удалять (может рассекать и прижигать) повреждение, создавая сухую хирургическую окружающую среду с минимальной травмой ткани. Когда углекислый лазер используется как мономодель, процент рецидивирования келоида достаточно высокий, поэтому рекомендуется комбинировать лазерную обработку с постоперативным введением стероидов, что значительно снижает уровень рецидивирования.
Лучевая терапия. Использования радиационной терапии для лечения келоидных рубцов остается спорным. В одном ретроспективном исследовании установлено, что применение поверхностной лучевой терапии после резецированния рубцов вызвало рецидивирование у 53% пациентов [18]. Более перспективным считается преоперативная обработка раствором гиалуронидазы рубцов с последующим хирургическим удалением и затем наружное облучение, для снижения вероятности рецидива [6].
Рентгенотерапия (лучи Букки) основана на действии ионизирующего излучения на соединительную ткань, вызывающем отечность и разрушение коллагеновых волокон, фибробластов. Рентгенотерапия назначается до 6 сеансов облучения с интервалом в 6–8 недель при одноразовой дозе до 15000 Р. Действию ионизирующего облучения подвергаются только поверхностные слои кожи (в частности, рубца), а на подлежащие ткани рентгеновская нагрузка незначительна. Противопоказанием к назначению Букки-терапии являются болезни почек, декомпенсация кровообращения, наличие дерматитов и остаточных ран. Идея применения рентгенотерапии очень рациональна, потому что в случае деструкции некоторого количества фибробластов достигается баланс между синтезом и деградацией сложного коллагена вплоть до изменения самой его структуры. Эта идея, в частности, реализована при использовании современной лазерной техники. Общая доза облучения для предотвращения рецидива келоидного рубца составляет от 15 до 20 Гр. Рекомендуют также одноразовое облучение раны в день снятия швов в тех же дозах — 15–20 Гр. Иногда такую процедуру повторяют до 6 раз с интервалами в 1,5–2 месяца.
Иссечение. Желательно избегать хирургического вмешательства, особенно при наличии келоида. Иссечение дает рецидив в 45–100% случаях и должно крайне редко использоваться как отдельная модель терапии. После иссечения необходима длительная противорецидивная терапия. Когда возможно, применяются давящие на рану повязки и белье в раннем послеоперационном периоде. Снижение рецидивов достигается комбинацией иссечения с другими методами, такими как лучевая или рентгенотерапии, введение интерферона или кортикостероидов [10].
После оперативных вмешательств или травм кожи необходимо проводить профилактические мероприятия, снижающие риск возникновения образования келоида или гипертрофических швов. Период активной терапии должен начинаться на 2-й стадии формировании рубца, т. е. на 10–30 сутки после травмы. По мнению авторов, существует пропорциональная зависимость от эффективности терапевтического лечения от возраста рубцов: рубцы старше 6 месяцев хуже поддаются терапии, чем более молодые. Скорее всего, снижение эффективности лечебных мероприятий связано с уменьшением количества сосудов и уплотнением рубцовой ткани, что ухудшает ее трофику [3]. Профилактические методы могут включать: окклюзивные повязки, компрессионную терапию, наружные аппликации или внутрикожное введение глюкокортикостероидов, Контрактубекс, Лонгидазу, иммунотерапию.
При сформировавшемся рубце с длительностью существования до 12 месяцев возможно проводить терапию всеми методами, а при длительно существующем образовании (более 12 месяцев) эффективны только агрессивные методы: введение кортикостероидов в зону поражения, иссечение, лучевая терапия, Букки-терапия, лазерная терапия.
Косметические процедуры, направленные на внешнюю коррекцию дефекта. Наиболее популярные косметологические процедуры (пилинги, мезотерапия, дермабразия) не несут какой-либо терапевтической цели при воздействии на рубцы. Использование этих методов способствует эстетической коррекции небольших рубцов. Важно знать, что гипертрофические рубцы можно подвергать шлифовке только после того, как они придут в спокойное состояние. Для получения удовлетворительных результатов в лечении рубцов со сроком существования более полугода к косметическим процедурам необходимо подключать 1–2 инъекции кортикостероидов (Дипроспана) [2]. Пескоструйная дермабразия (10–15 сеансов с интервалом в 10–14 дней) при обычном курсовом лечении оказывает удовлетворительные результаты, но при проведении двух курсов по 10–15 процедур эффективность лечения возрастает [2]. Оперативная дермабразия гипертрофических рубцов требует повторной операции через полгода. Полная эпитализация гипертрофических рубцов после их глубокой оперативной дермабразии происходит значительно позже эпителизации нормотрофических и гипотрофических рубцов и растягивалась на 3–4 недели, даже при использовании ранозаживляющих мазей [2]. О. С. Озерская (2002) с целью профилактики рецидива рубцов после их дермабразии провела пересадку аутологичных кератиноцитов. Беспрепятственное снятие повязок возможным на 7–8 день, полная эпитализация рубцов наступила в сроки до 14 дней. Таким образом, очевидно значительное ускорение эпитализации при операции дермабразии рубцов с трансплантацией кератиноцитов. Во избежание еще большей гипертрофии и гипер- или депигментации корректировать гипертрофические рубцы агрессивными методами нельзя, а срединные пилинги можно делать только после проведения курса поверхностных пилингов. Что касается келоидных рубцов, то их лучше не подвергать воздействию раздражающих методов, т. к. велика вероятность спровоцировать их дальнейший рост.
Пилинг фруктовыми кислотами. Во время пилинга происходит отшелушивание ороговевших клеток кожи, стимуляция процессов регенерации ее глубокого слоя. Фруктовые кислоты мягко проникают в кожу, не травмируя ее, и стимулируют выработку коллагена и эластина. Благодаря этому повышается упругость кожи, выравнивается рельеф и уменьшается гиперпигментация, что внешне корректирует косметический дефект небольших рубцов.
Химические пилинги. Для небольших, слабо выраженных гипертрофических рубцов химические пилинги лучше провести в два этапа. При этом в ежедневный домашний уход на 21-й день с целью сглаживания рубцовой гипертрофии включают силиконовый дерматологический крем, который создает окклюзионную пленку, защищая кожу от потери влаги, снимает воспаление и эритему, стимулирует репарацию. Параллельно с пилингами можно проводить сеансы мезотерапии с регенерантами и усилителями локальной микроциркуляции. Терапия слабо выраженных гипертрофированных рубцов после курса химических пилингов может быть продолжена топическими препаратами. При выраженных гипертрофических рубцах пилинги проводятся через шесть-восемь месяцев после иссечения патологического рубца или проведенного курса физиотерапии (гальвано-, фонофорез) с гиалуронидазой и гепарином. Курс химических пилингов тоже проводят в два этапа: сначала несколько сеансов мультифруктовых пилингов (гликолевая, салициловая, молочная, лимонная кислоты) один раз в неделю, затем комплексный ретиноловый желтый пилинг. Пилинг выполняют по индивидуальной схеме в соответствии с параметрами рубца и реакцией кожи.
В заключение необходимо отметить, что терапия келоидных и гипертрофических рубцов, при всем многообразии методов лечения, требует строго индивидуального подхода с учетом основных параметров рубца: размеров и длительности его существования.
По вопросам литературы обращайтесь в редакцию.
Ю. А. Галлямова*, доктор медицинских наук
З. З. Кардашова**
* РМАПО, ** РГНКЦ, Москва
Ключевые слова: гипертрофические рубцы, келоидные рубцы, келоидная болезнь, келоид, келоидообразование, лечение келоида, лечение рубцов, профилактика рубцов.