Гравидарный эндометрий гистология что это
Патология полости матки

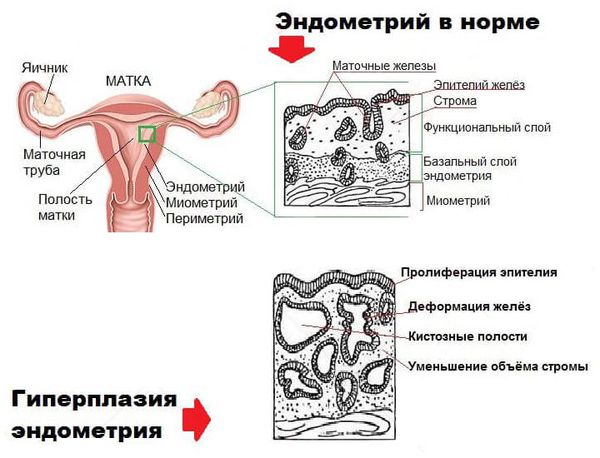
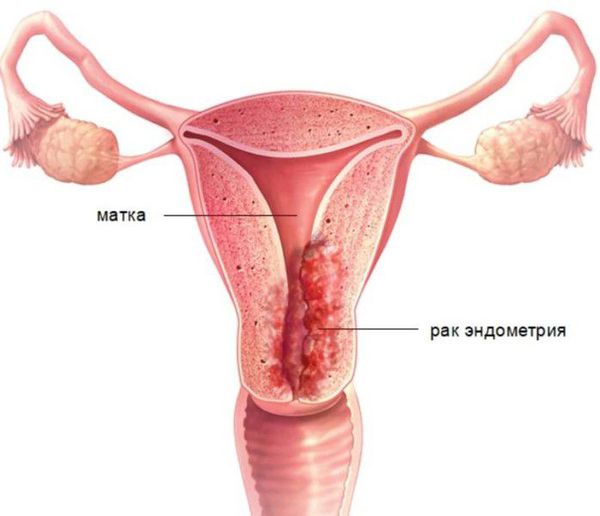
Рисунок 1. Нормальная анатомия женских половых органов
Данный раздел необходимо начать с определения понятия «полость матки». Полость матки – это полость, ограниченная со всех сторон эндометрием (внутренней оболочкой матки).
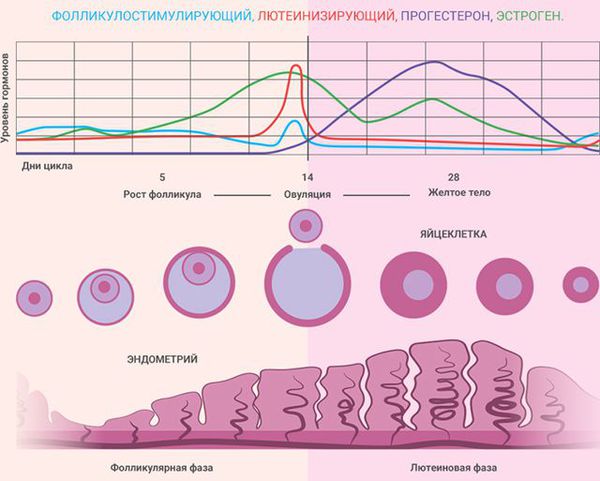
Эндометрий в течение менструального цикла подвергается циклическим изменениям. В норме, в первый день менструации верхний слой эндометрия отслаивается, что сопровождается менструальным кровотечением. Далее менструация прекращается, и эндометрий начинает пролиферировать (то есть разрастаться).
После овуляции, начинается следующая фаза цикла, во время которой эндометрий как бы «набухает» и его толщина увеличивается. Таким образом, организм женщины как бы готовится к возможной беременности.
Если оплодотворение происходит, то «пышный» эндометрий полностью готов к имплантации (прикреплению) оплодотворенной яйцеклетки, и созданы все условия для развития беременности.
Если оплодотворение не происходит, то под воздействием определенных гормонов, эндометрий, который «вырос» в течение цикла, вновь отслаивается, то есть начинается менструация.
Патология полости матки
Исходя из вышеперечисленной информации, патология полости матки может быть условно подразделена на несколько подгрупп:
Основные виды патологии полости матки представлены на Рисунке 2.

Рисунок 2. Основные виды патологии полости матки
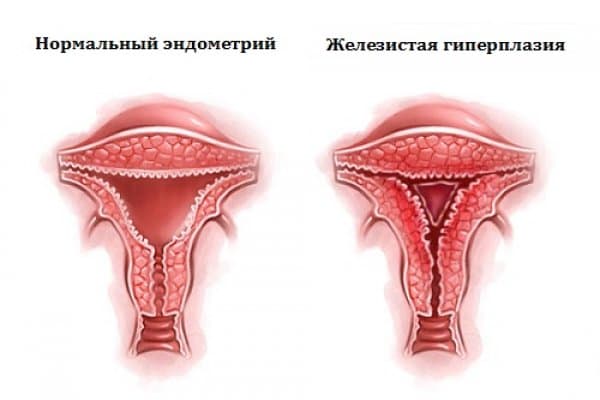
Гиперплазия эндометрия
Рассмотрим одну из самых распространенных патологий полости матки – гиперплазию эндометрия.
Гиперплазия эндометрия – процесс, характеризующийся неадекватной и неинвазивной пролиферацией (разрастанием) желез эндометрия с различным качеством предлежащей стромы. В последнее время большое значение в развитии данного процесса придается неадекватному избыточному росту сосудов, т.е. избыточному ангиогенезу. В будущем, при создании препаратов, которые смогут блокировать эти процессы, т.е. обладать антиангиогенными свойствами, гиперплазия эндометрия и лечение будет весьма легкой задачей для врача.
Классификация гиперплазии эндометрия
Эндометрий в норме состоит из железы и стромы (основы). В зависимости о того, какая ткань разрастается, выделяют следующие основные виды гиперплазии эндометрия:
Атипическая гиперплазия эндометрия может быть обнаружена как в гиперплазированном эндометрии, так и в атрофичном, и в полипах. Этот тип гиперплазии эндометрия характеризуется высокой частотой ее перехода в рак эндометрия. Атипическая гиперплазия характеризуется структурной перестройкой желез и более интенсивной пролиферацией по сравнению с другими видами гиперплазии эндометрия.
Причины гиперплазии эндометрия
Что же является основными причинами развития гиперплазии эндометрия? В настоящее время основными причинами, вызывающими гиперплазию, считаются:
Однако до сих пор остается непонятным, почему эта патология развивается у одних женщин и не развивается у других при прочих равных условиях. Достаточно часто, железистая гиперплазия эндометрия встречается у пациенток с хронической ановуляцией (например, при поликистозных яичниках). К сожалению, при проведении стимуляции овуляции и воздействии гормональных препаратов на эндометрий, формирование железистой гиперплазии также диагностируется также довольно-таки часто.
Согласно последним данным, существует генетическая предрасположенность у некоторых женщин к патологическому образованию новых сосудов в тканях, в частности, в слизистой полости матки (нарушение ангионенеза), а также к нарушению запрограммированной гибели клеток в организме, что происходит в норме. Эти генетические факторы сейчас считаются основными патологическими звеньями развития многих гинекологических заболеваний, в том числе и гиперплазии эндометрия.
Гиперплазия эндометрия подразделяется на несколько основных видов:
Атипическая гиперплазия эндометрия всегда вызывает особую настороженность, поскольку считается основой для развития злокачественных изменений эндометрия. Такие процессы могут длительно персистировать, но, к сожалению, время перехода их в злокачественную форму установить невозможно.
По данным литературы риск развития злокачественных процессов при наличии атипической гиперплазии (по классификации ВОЗ) колеблется от 15 до 40%, что связано с широкой вариабельностью дифференциально-диагностических критериев.
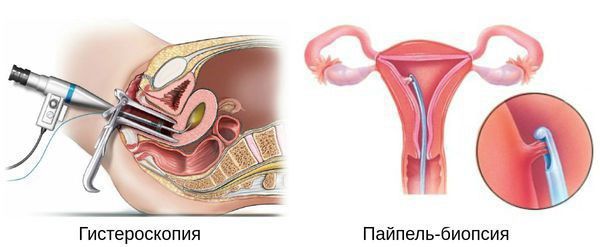
Диагноз «Гиперплазия эндометрия», предварительно установленный на основании клинических данных и проведения УЗИ, требует проведения гистероскопии и раздельного диагностического выскабливания с последующим гистологическим исследованием для уточнения формы патологии и выбора правильной тактики дальнейшего лечения. В ряде случаев гистероскопия является не только методом диагностики, но и методом лечения.
Лечение гиперплазии эндометрия начинается с хирургического удаления эндометрия с последующим гистологическим исследованием. После того, как установлен точный диагноз, возможно определить дальнейшую тактику ведения. Она определяется, как гистологическим типом патологии, так и рядом других факторов: заинтересованность в беременности, возраст, наличие сопутствующих заболевания и многими другими.
Таким образом, основным методом диагностики и лечения гиперплазии эндометрия является гистероскопия. Только после установления диагноза есть возможность выбирать дальнейшую тактику ведения.
Полип эндометрия
Полип эндометрия – это отдельный вырост слизистой полости матки. Полипы эндометрия бывают железистыми, фиброзными и смешанными, в зависимости от причины, которой они вызваны. Универсальным методом диагностики и лечения полипов эндометрия является гистероскопия (гистерорезектоскопия).
Внутриматочные синехии
Внутриматочные синехии – это спайки в полости матки, которые очень часто мешают имплантации оплодотворенной яйцеклетки, что приводит к бесплодию. Причинами внутриматочных синехий могут быть воспалительные заболевания органов малого таза, так и внутриматочные вмешательства (аборты, выскабливания по поводу замершей беременности, оперативные вмешательства на матке).
Наличие внутриматочных синехий безопасно для жизни, и может проявлять себя скудными менструациями или их отсутствием. Однако, при возникновении вопросов беременности, внутриматочные сращения могут быть серьезной проблемой, особенно при распространенных формах и выраженном повреждении матки./p>
Субмукозная миома матки
Субмукозная миома матки также нарушает анатомию полости матки и «выполняет» роль спирали, также способствуя развитию бесплодия.
Гиперплазия эндометрия матки
Тел.: 8-800-25-03-03-2
(бесплатно для звонков из регионов России)
Санкт-Петербург, наб. реки Фонтанки, д. 154
Тел.: +7 (812) 676-25-25
Санкт-Петербург, В.О., Кадетская линия, д. 13-15
Тел.: +7 (812) 676-25-25
Санкт-Петербург, ул. Циолковского, д.3
Тел.: +7 (812) 676-25-10
Эндометрий представляет собой нежную тонкую слизистую ткань, которая выстилает полость матки изнутри. Данная ткань каждый месяц быстро растет и утолщается под действием женских половых гормонов. В случае наступления беременности, эндометрий является «пуховой периной» на которую прикрепляется оплодотворенная яйцеклетка. При отсутствии беременности под действием гормонов эндометрий отторгается, выходит в виде менструальной крови.
Классификация гиперплазии эндометрия по локализации
Классификация гиперплазии эндометрия (по гистологической картине)
Причины гиперплазии эндометрия
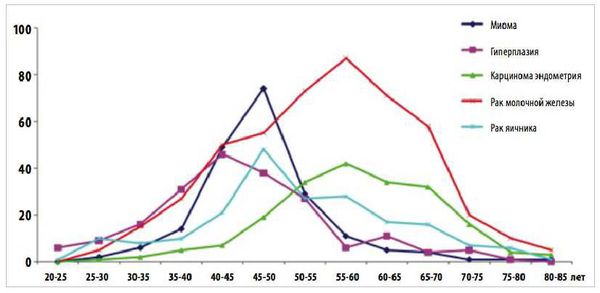
В настоящее время основной причиной развития гиперплазии считается нарушение баланса женских половых гормонов, который чаще всего встречается в пубертатном периоде и перименопаузе.
Факторы риска развития гиперплазии эндометрия
Симптомы, которые встречаются при гиперплазии эндометрия
Основные из них при гиперплазии эндометрия могут быть:
Обследования, которые помогут выявить и поставить диагноз гиперплазии эндометрия
Лечение гиперплазии эндометрия
Практически в 100% случаев лечение гиперплазии эндометрия хирургическое.
Методами хирургического лечения гиперплазии эндометрия является гистероскопия и гистерорезектоскопия.
Данная операция проводится под общей анестезией. Продолжительность операции не превышает 30 минут, короткий период нахождения под общей анестезией позволяет врачам в тот же день отпустить пациентку домой.
Осложнения гиперплазии
При отсутствии должного и адекватного лечения гиперплазия эндометрия приводит к тяжелой анемии с значительным снижением уровня гемоглобина, появлению слабости, повышенной усталости, сонливости, что связано с большими потерями крови во время менструации. У молодых женщин гиперплазия эндометрия может быть причиной бесплодия и невынашивания беременности. Отдельные формы гиперплазии эндометрия (железистая и кистозная гиперплазии эндометрия) являются предраковым состоянием и в случае длительного наблюдения, при отсутствии лечения, могут переродиться в рак матки.
Профилактические мероприятия при данном заболевании необходимы для того, чтобы снизить риск развития рака эндометрия и предотвратить рецидив гиперплазии.
Гиперплазия эндометрия. Часто задаваемые вопросы
1. Что это такое? Доброкачественный процесс, который характеризуется чрезмерным разрастанием внутреннего слоя матки.
2. Из-за чего она возникает? Из-за постоянного воздействия полового гормона эстрогена на эндометрий, который вызывает его чрезмерное разрастание. Гиперэстрогения возникает из-за нарушения центральной регулиции менструального цикла, гормонопродуцирующих опухолей яичников, неправильного использования гормональных препаратов, дефицита прогестерона (гормон II фазы менструального цикла), обладающего антипролиферативным действием, так же в результате ановуляторных циклов.
3. Это распространенное заболевание? Частота встречаемости в структуре гинекологической заболеваемости 15-50%. По данным обращаемости пациенток частота встречаемости ГПЭ- 30%. В позднем репродуктивном возрасте и в перименопаузе встречается с частотой- 50%
4. Это заболевание очень опасно? Пристального внимания врачей заслуживают:
При отсутствии должного лечения гиперплазия эндометрия может приводить к серьезным маточным кровотечениям, со снижением гемоглобина крови и вытекающими отсюда последствиями.
5. Возможно ли забеременеть на фоне гиперплазии эндометрия? Ответ – нет. Гиперплазия эндометрия не возникает спонтанно, это следствие нарушений в репродуктивной системе женщины. Нарушение баланса между звеньями регуляции менструального цикла вызывает избыток эстрогенов в организме женщины, нехватку прогестерона, вследствие этого отсутствие овуляции (выхода яйцеклетки из фолликула для оплодотворения). Так же сам эндометрий структурно изменен, поэтому является неблагоприятным для имплантации (прикрепление плодного яйца к стенке матки).
7. Как диагностировать атипическую гиперплазию эндометрия? Большую информацию врач получает при опросе пациентки во время общения (возраст менархе или время наступления менопаузы, все особенности менструального цикла- его длительность, характер выделений и т.д.).
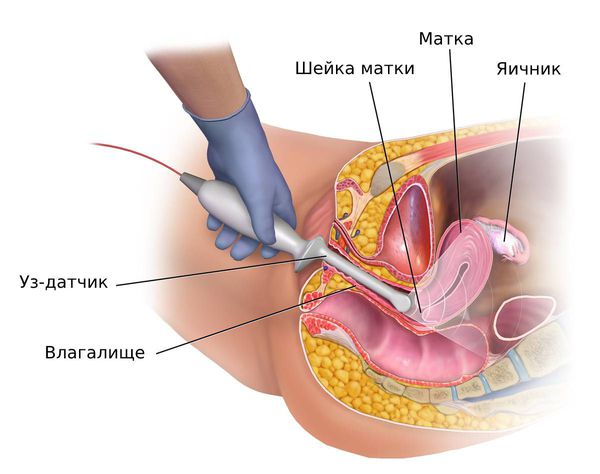
УЗ-исследование в зависимости от периода жизни женщины, а также фазы менструального цикла может дать информацию о состоянии эндометрия. По этим данным можно заподозрить проблему, однако подтвердить или опровергнуть атипию в клетках эндометрия нельзя. Только проведение гистероскопии с последующим гистологическим исследованием материала является золотым стандартом для диагностики этого состояния. Информативность метода более 90%.
8. Обязательно ли проводить выскабливание эндометрия при гиперплазии? Раздельное выскабливание цервикального канала и полости матки несет за собой лечебный и диагностический характер. Механическое удаление измененной патогенной ткани из полости матки предотвращает маточное кровотечение, что составляет лечебный эффект. Полученный соскоб отправляется на гистологическое исследование, после которого будет дано заключение о характере ткани, наличии или отсутствии признаков злокачественного поражения.
9. Возможен ли рецидив гиперплазии эндометрия? Да, возможен. Так как причиной гиперплазии эндометрия является нарушение гормонального баланса в организме женщины, то требуется обследование её гормонального фона. Для профилактики рецидива необходимо соответствующее лечение и исключение факторов риска.
Что такое гиперплазия эндометрия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Анькина А. О., врача УЗИ со стажем в 9 лет.
Определение болезни. Причины заболевания
Диагноз « гиперплазия эндометрия » ставится только по заключению гистологического исследования. Без своевременной диагностики и целенаправленного лечения повышается риск развития рака эндометрия.
В составе маточного эндометрия есть специфические рецепторы, которые делают его органом-мишенью для половых гормонов. При гормональном сбое нарушается рост и дифференцировка эндометриальных клеток, что приводит к разрастанию эндометрия.
Факторы риска развития гиперплазии эндометрия [1] [8] [11] :
Симптомы гиперплазии эндометрия
В период перехода к менопаузе основным симптомом заболевания являются нерегулярные обильные менструации, сменяющиеся длительными мажущими кровянистыми выделениями.
Женщины менопаузального возраста жалуются на скудные кровянистые выделения из половых путей. Они могут проявляться эпизодически либо быть продолжительными.
Патогенез гиперплазии эндометрия
Состояние эндометрия зависит от фазы менструального цикла:
В патогенезе гиперплазии эндометрия выделяют два варианта развития событий:
В случае гиперплазии эндометрия с атипией избыток желёз эндометрия сочетается с клеточными мутациями (атипическим перерождением). Атипическая гиперплазия эндометрия является предраковым состоянием.
Классификация и стадии развития гиперплазии эндометрия
Международная классификация болезней 10-го пересмотра (МКБ-10):
Пересмотренная классификация ВОЗ 2014 года:
Осложнения гиперплазии эндометрия
Анемия. Для гиперплазии эндометрия характерны аномальные маточные кровотечения. В связи с этим женщины часто страдают от хронического малокровия разной степени выраженности.
Бесплодие. Гормональные изменения отражаются на качестве эндометрия, что создаёт риск неудачной имплантации эмбриона. Помимо этого, гиперплазия эндометрия часто выявляется на фоне хронической ановуляции, при которой зачатие невозможно.
Диагностика гиперплазии эндометрия
Диагностика основана на анализе данных анамнеза пациентки (истории болезни), клинической картины заболевания (жалоб и физикального осмотра), а также на результатах ультразвукового и гистероскопического исследования с обязательным патоморфологическим анализом соскоба из полости матки.
Диагноз «гиперплазия эндометрия» ставится только на основании гистологического исследования материала, полученного при диагностическом выскабливании слизистой оболочки матки или удалении матки.
Анамнез и клиническая картина
При сборе анамнеза врач-гинеколог задаёт пациентке вопросы:
Физикальный осмотр включает в себя местный осмотр наружных половых органов, исследование влагалища и шейки матки в зеркалах, а также бимануальное (двумя руками) исследование матки и придатков. Осмотр проводится на первичном приёме, чтобы исключить воспалительные заболевания и/или объёмные опухолевые образования.
Инструментальная диагностика
У женщин репродуктивного и пременопаузального возрастов при подозрении на гиперплазию эндометрия ТВУЗИ органов малого таза проводится на 5 – 7-й день менструального цикла. В норме в это время толщина эндометрия не превышает 6 мм. Патологию эндометрия подозревают, когда его толщина не соответствует определённой фазе менструального цикла:
Гистероскопия с раздельным диагностическим выскабливанием (РДВ) матки и цервикального канала — информативный метод в диагностике гиперпластических процессов эндометрия. При помощи гистероскопа (эндоскопического прибора для осмотра полости матки) врач оценивает состояние слизистой оболочки матки и цервикального канала. При необходимости удаляет локальные поражения и обязательно берёт материал для последующего гистологического исследования.
Если выскабливание проводят как лечебную процедуру при обильном маточном кровотечении, врач полностью удаляет слизистую оболочку матки под контролем гистероскопии.
Дифференциальная диагностика гиперплазии эндометрия проводится с полипом эндометрия, субмукозной (подслизистой) миомой матки, эндометритом, прервавшейся беременностью и раком эндометрия.
Лечение гиперплазии эндометрия
Лечение патологии эндометрия основывается на трёх принципах:
Тактика лечения будет зависеть от результата гистологического исследования эндометрия, полученного в ходе выскабливания, от возраста женщины, сопутствующих заболеваний и репродуктивных планов.
Гиперплазия эндометрия без атипии:
Гиперплазия эндометрия с атипией:
Медикаментозное лечение гормональными препаратами проводится пациенткам репродуктивного возраста с неатипической гиперплазией эндометрия при наличии симптомов, факторов риска, отсутствии регресса за 6 месяцев наблюдения и при атипической гиперплазии эндометрия у женщин, планирующих беременность.
Гормональную терапию назначают не менее чем на 6 месяцев:
В качестве негормональной терапии возможно применение препаратов:
Лечение нужно сочетать с низкокалорийной диетой и достаточной физической нагрузкой согласно общему физическому развитию женщины. При необходимости врач назначает препараты, которые нормализуют метаболизм углеводов в организме: подавляют образование глюкозы клетками печени, повышают чувствительность тканей к инсулину, расщепляют сложные сахара.
Хирургическое лечение. Атипическая гиперплазия эндометрия на начальном этапе требует обязательной консультации онкогинеколога, который должен установить, нужна ли операция и в каком объёме.
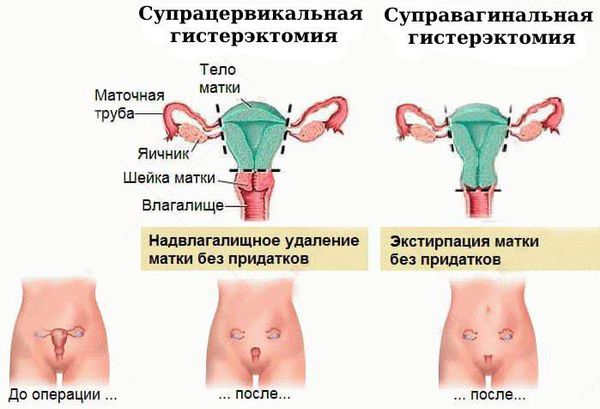
Чаще всего выполняется надвлагалищная ампутация матки — суправагинальная гистерэктомия (удаление тела и шейки матки). Вопрос о сохранении яичников решается строго индивидуально, зависит от возраста пациентки и факторов риска.
Показания к гистерэктомии:
Прогноз. Профилактика
Обследование для исключения гиперплазии или рака эндометрия показано в следующих случаях:
1. Если есть аномальные маточные кровотечения [29] [31] :
2. Если по результатам цитологического исследования соскоба шейки матки отмечается:
Профилактика:
Гравидарный эндометрий гистология что это
Балтийский институт репродуктологии человека, Санкт-Петербург, Россия
Dеcidua — знакомая и неизвестная
Журнал: Проблемы репродукции. 2017;23(4): 13-17
Никитин А. И. Dеcidua — знакомая и неизвестная. Проблемы репродукции. 2017;23(4):13-17.
Nikitin A I. Dеcidua — familiar and unknown. Russian Journal of Human Reproduction. 2017;23(4):13-17.
https://doi.org/10.17116/repro201723413-17
Балтийский институт репродуктологии человека, Санкт-Петербург, Россия
Гравидарная перестройка эндометрия — процесс, обеспечивающий имплантацию эмбриона. В настоящее время в качестве ее основных признаков рассматриваются изменения поверхностного эпителия эндометрия в виде появления пиноподий и децидуализация стромы эндометрия с формированием децидуальной оболочки — материнской части плаценты. Однако и исследователей, и врачей всегда «ставят в тупик» случаи внематочных беременностей: трубных, шеечных, яичниковых и даже брюшных. Ведь в этих органах нет эндометрия. Как в таких случаях происходит имплантация бластоцисты? Фактами, от которых следует отталкиваться при поиске ответа на этот вопрос, являются обнаружение при патогистологическом исследовании «материала» внематочных беременностей участков децидуальной ткани. Важно отметить, что такие участки обнаруживались вне матки и при маточных беременностях. На основе собственного опыта и анализа данных литературы автор в работе делает вывод о том, что эндометрий не является структурой, с только ей присущей способностью претерпевать гравидарную трансформацию, а последнюю можно рассматривать как системную физиологическую реакцию клеток стромы не только эндометрия, но и других органов на рост в организме женщины прогестерона. Поэтому у бластоцисты, оказавшейся вне матки, есть шанс имплантироваться, если в строме маточной трубы, яичника или какого-либо органа брюшной полости развивается децидуальная реакция. После имплантации эктопическая децидуальная ткань становится децидуальной оболочкой бластоцисты, которая, как и при маточной беременности, выполняет те же функции, которые выполняет decidua basalis матки: снабжение эмбриона питанием, иммунологическую функцию, защиту зародыша от патогенных микроорганизмов и т.п. В результате вне матки развивается беременность, нередко — до срока.
Балтийский институт репродуктологии человека, Санкт-Петербург, Россия
Прегравидарная (в дальнейшем — гравидарная) перестройка эндометрия — процесс, обеспечивающий успешную имплантацию эмбриона. В настоящее время в качестве его основных морфологических признаков рассматриваются своеобразные изменения поверхностного эпителия эндометрия (появление пиноподий) и «децидуализация» стромы эндометрия. Однако и исследователей, и врачей всегда «ставят в тупик» случаи внематочных беременностей: трубных, шеечных, яичниковых и даже брюшных. Ведь в этих органах нет эндометрия. Как в таких случаях происходит имплантация бластоцисты? Каким образом плацентация, прежде всего — при брюшной беременности, не сопровождается врастанием хориона в прилежащие к месту имплантации органы с их разрушением и неизбежным кровотечением? Разрыв маточной трубы при трубной беременности происходит, по-видимому, чаще из-за того, что в этом случае просто не хватает пространства для растущего плодово-плацентарного комплекса. Из всего этого возникает неизбежный вопрос: действительно ли эндометрий является уникальной структурой, обеспечивающей успешную имплантацию зародыша. Недавно это уже было в статье В.С. Корсака [1], описавшего случай доношенной брюшной беременности.
Для выяснения генеза «эктопий» децидуа следует напомнить процесс формирования в матке decidua basalis материнской части плаценты, в которую и имплантируется бластоциста в естественных условиях наступления беременности. Изменения эндометрия, направленные на его подготовку к восприятию зародыша, начинаются с так называемой его прегравидарной перестройки. Она развивается во второй (лютеиновой, секреторной) фазе менструального цикла и не зависит от наступления беременности. Ее начало совпадает с началом функционирования желтого тела, что говорит о безусловной роли в этом процессе прогестерона. Прегравидарные изменения эндометрия наиболее выражены в его компактном (поверхностном) и спонгиозном (промежуточном) слоях и в меньшей степени затрагивают базальный слой, остающийся источником регенерации эндометрия после менструаций и родов. В процессе прегравидарной перестройки компактного слоя отмечаются своеобразные изменения поверхностного эпителия (появление пиноподий), а также клеточных элементов и сосудов стромы. Они включают прежде всего такой процесс, как трансформация фибробластов межуточной ткани в клетки, напоминающие децидуальные. Они округляются, увеличиваются в размерах, накапливают гликоген и липиды, но пока не формируют крупные группы, характерные для истинной децидуальной реакции. Поэтому этот процесс называют децидуоподобной реакцией. Одновременно отмечается рост так называемых спиральных артерий, которые удлиняются и достигают поверхности эндометрия. Их стенки утолщаются, они становятся более извитыми и спирально закручиваются в «клубки». Изменение скорости кровотока и увеличение проницаемости стенок сосудов приводит к росту гидрофильности стромы компактного слоя, ее отеку и разрыхлению. Железы эндометрия, преимущественно губчатого слоя, становятся извитыми, увеличивается их просвет и возрастает секреторная активность. В них накапливается слизистый секрет, содержащий мукоиды, гликоген, глюкопротеиды и другие химические элементы [4].
Все эти изменения приводят к тому, что определяемая при ультразвуковом исследовании «толщина» эндометрия увеличивается с 1—3 мм (в фолликулярную фазу цикла) до 8—10 мм. Это именно та величина, на которую как оптимальную, обеспечивающую имплантацию бластоцисты, ориентируются специалисты, работающие по программам ВРТ.
Если оплодотворение не происходит и бластоциста не формируется, описанная децидуоподобная перестройка эндометрия претерпевает обратное развитие, а функциональный слой его после падения уровня прогестерона отторгается (менструация). Если же наступает беременность и формируется бластоциста, децидуоподобная реакция переходит в процесс «децидуализации эндометрия». Фибробласты стромы эндометрия при этом округляются и увеличиваются в размере в несколько раз (до 50 мкм), превращаясь в децидуальные клетки. В них появляются крупные гранулы гликогена и капли липидов. Они обогащаются белковыми веществами, в них обнаруживаются протеолитические ферменты, фосфатаза, гистаминаза, кальций, железо и другие химические элементы. С помощью микроворсинок на их поверхности децидуальные клетки объединяются в группы, что приводит к началу формирования decidua basalis. В ее состав, кроме децидуальных, входят также лимфомиелоидные клетки, главным образом — макрофаги и эндометриальные гранулоциты. Одновременно продолжает увеличиваться гидрофильность стромы эндометрия, происходит дальнейшее развитие сети спиральных артерий. Капилляры, проходящие в компактном слое под поверхностным эпителием, расширяются и принимают форму синусоиды. В железах спонгиозного слоя появляются сосочковые выросты, содержащие капилляры [4]. Ряд авторов [5] обозначают процесс децидуализации стромы эндометрия как генетически запрограммированное «ремоделирование ткани» (tissue remodelling), контролируемое гормонами (прогестерон, эстрадиол), простагландинами, гормонами роста, цитокинами и другими факторами.
Достигшей полости матки бластоцисте необходимо «выбрать» место для имплантации. Как установлено [5—8], это происходит в результате сложных реципрокных взаимодействий бластоцисты и структур эндометрия. Главную роль в этом процессе играют так называемые молекулы клеточной адгезии. В настоящее время наибольшее значение придается интегринам, поверхностным гетеродимерным гликопротеинам, обеспечивающим адгезию клеток друг к другу, а также к компонентам внеклеточного матрикса. Экспрессия интегринов находится под контролем прогестерона, факторов роста и «информационных пептидных молекул» — цитокинов. Важно отметить, что механизмы рецепции, контролирующие взаимодействие бластоцисты и эндометрия, формируются в процессе децидуализации последнего. При этом продуцентами интегринов являются и эпителий, и «стромальные клетки» эндометрия [5]. В свою очередь и бластоциста (трофобласт) продуцирует сигнальные пептидные молекулы, в основном — цитокины: факторы роста, интерлейкины и др. Таким образом, в обмене химическими сигналами с бластоцистой «задействован» не только эпителий эндометрия, но и децидуальные клетки. При этом формирование именно decidua basalis является наиболее важной составляющей процессов, связанных с имплантацией бластоцисты, так как эта структура станет «маточной частью плаценты» и обеспечит маточно-плацентарный кровоток, а decidua capsularis и parietalis сформируют остальную часть децидуальной оболочки, в которой на протяжении всей беременности будут заключены эмбрион/плод, околоплодные воды и плацента. С началом секреции трофобластом хорионического гонадотропина (с 7-го дня после оплодотворения) этот гормон также становится одним из «сигнальных факторов» в «диалоге» между эмбрионом и организмом матери.
Таким образом, процесс децидуализации происходит в результате реакции фибробластов соединительной ткани на воздействие прогестерона. Поскольку фибробласты являются необходимым компонентом стромы любого органа, можно допустить, что децидуальная реакция при состоявшемся оплодотворении и сформировавшейся бластоцисте может иметь место не только в матке, но и в других органах и ее в этих случаях можно считать по сути не «эктопией», а результатом местной трансформации фибробластов стромы органа. При этом эмбрион, попавший, например, в брюшную полость (что происходит, вероятно, много чаще, чем мы думаем) или «застрявший» в трубе начинает получать биохимические «сигналы» от участков децидуальной ткани («я тут») и сам начинает направлять ей свои «сигналы». Так, обменявшись «приветствиями» с децидуальными клетками, зародыш начинает процесс имплантации. В результате «эктопическая децидуальная ткань» становится децидуальной оболочкой бластоцисты, и, как и при маточной беременности, выполняет те же функции, которые выполняет decidua basalis матки: и защитную, предохраняющую подлежащий орган от врастания в него ворсин хориона, и (до сформирования плаценты) функцию снабжения эмбриона питательными веществами (гистиотрофное питание), и функцию, обеспечивающую иммунологическую толерантность организма матери к «чужому» для нее плоду, и функцию защиты зародыша от патогенных микроорганизмов и т. д. Все сказанное позволяет признать реальным вывод о том, что эндометрий не является уникальной структурой, с только ей присущей способностью претерпевать прегравидарную и гравидарную трансформацию, а последняя носит закономерный общий для организма характер, который можно рассматривать как системную физиологическую реакцию клеток стромы органов на рост в организме женщины прогестерона.
Сделанный вывод, как было сказано выше, подтверждается рядом исследований. В России уже в начале прошлого века, в работах К.П. Улезко-Строгановой [9], первого руководителя лаборатории нормальной и патологической морфологии «Императорского клинического повивального института» в Санкт-Петербурге и в работах других авторов [10—14] было показано, что «децидуальному превращению» могут подвергаться клетки стромы брюшины, сальника, лимфоузлов, маточных труб, яичников, влагалища, аппендикса, мочевого пузыря, почек, диафрагмы, серозных оболочек плевральной полости, эндотелий кровеносных сосудов, даже — слизистая гортани.
Следует особо отметить, что до сих пор дискутирующийся в литературе взгляд на возможность трансформации клеток стромы в децидуальные в других, кроме матки, органах, как это ни удивительно («хорошо забытое старое») был с полной определенностью, подтвержденной собственными наблюдениями, высказан еще в 1887 г. в упомянутой выше работе А. Walker [2], описавшего 2 случая брюшной беременности.
Таким образом, можно допустить, что бластоциста, попавшая в брюшную полость, имплантируется не в ткань органа (сальника, маточной трубы, яичника и др. органов), а в сформировавшуюся в этих органах «родную» децидуальную ткань, в которой, как и в decidua матки после имплантации зародыша образуются «кровяные лакуны», в которые погружаются ворсины хориона и т. д. В результате формируется, как и в матке, децидуальная оболочка, а затем плацента и развивается, нередко — доношенная, беременность. Это позволяет также сделать вывод о том, что эмбриону для имплантации достаточно, вероятно, присутствия только децидуальной ткани.
Ярким свидетельством роли прогестерона в процессе «эктопической децидуализации» может служить сообщение L. Tang и соавт. [15], описавших случай обнаружения масс децидуальной ткани с кровоизлиянием в дугласово пространство у женщины с симптомами внутрибрюшного кровотечения. Как выяснилось, пациентка длительно применяла с целью контрацепции препараты прогестерона.
Вопросы, касающиеся распространенности и частоты «эктопической децидуализации», как и шансов эмбриона на успешную имплантацию, в этих случаях остаются открытыми, так как сообщения на эту тему появляются редко и, преимущественно, в виде описания отдельных случаев.
В связи с вышесказанным следует затронуть еще один важный аспект разбираемой проблемы. Он касается возникновения серьезных диагностических ошибок при обнаружении «эктопий» децидуальной ткани. Хотя опытный патогистолог без труда распознает децидуальную ткань, описаны случаи, когда эту ткань принимали за опухоль, чаще всего — мезотелиому, метастазы опухоли, особенно — при обнаружении участков децидуализации в лимфатических узлах, туберкулез и другие патологические процессы [16—18]. Это может иметь далеко идущие неблагоприятные, особенно — при беременности, последствия. Описаны и «обратные» ситуации, когда мезотелиома, в том числе и злокачественная, принималась за децидуальную ткань и необходимые лечебные мероприятия не проводились или проводились с опозданием [17, 19]. В этих случаях для дифференциальной диагностики в гистологической практике рекомендуют использовать специальный набор (панель) гистохимических реакций [20]. Описаны случаи внутрибрюшных кровотечений из мест эктопий децидуальной ткани [21], появление симптомов раздраженного кишечника при «децидуализации сальника» [22].
Отдельно cледует рассмотреть возникновение случаев пневмоторакса, в том числе — повторных, у молодых женщин в «перименструальном периоде», а также случаев судорожных приступов у молодых женщин, страдающих эпилепсией, также закономерно возникающих в перименструальном периоде [23, 24]. Поскольку прослежена четкая связь развития и пневмоторакса, и приступов эпилепсии с менструльным периодом, их еще называют «менструальным пневмотораксом» (catamenial pneumotorax — от греч. саtamenia — менструация), и «менструальной эпилепсией» (catamenial epilepcy). Что касается пневмоторакса, то здесь почти всегда есть морфологический материал для исследования, так как в большинстве случаев требуется оперативное вмешательство. Следует отметить, что нередко гистологически при менструальном пневмотораксе в плевре и диафрагме обнаруживаются наряду с типичной децидуальной тканью очаги эндометриоза. Поэтому последний рассматривают как основную причину пневмоторакса. Хотя в любом случае появление децидуальной ткани, в которой заложен механизм отслоения («отпадающая оболочка»), указывает на ее, возможно, ведущую роль в механизме возникновения этой патологии.
Понятно, что морфологический материал в случаях менструальной эпилепсии недоступен для изучения. Большинство авторов, описывающих случаи менструальной эпилепсии, связывают их, естественно, с гормональными изменениями в период менструации. Это логично. Однако поскольку они же одновременно считают, что многое в патогенезе приступов остается неясным, можно допустить предположение и о возможности трансформации каких-либо клеток ткани мозга мезодермального происхождения в децидуальные и их «задействование» в патогенезе приступов.
Поэтому возникающие при беременности (и вне ее у молодых женщин) патологические процессы неясного происхождения следует рассматривать и в аспектах возможной роли в этом «эктопий» децидуальной ткани.
Авторы заявляют об отсутствии конфликта интересов.
1 Употребление термина «децидуальная ткань» не является строго корректным, так как в международной и отечественной гистологической номенклатуре такой ткани нет, однако удобство использования и широкое распространение в научной литературе этого термина позволило нам также использовать его.