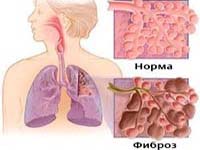
Идиопатический фиброз легких что это
Идиопатический легочный фиброз
Идиопатический легочный фиброз: причины развития
Аномальная фибропролиферация в легких связана с нарушением функции альвеолярных эпителиальных клеток либо их перепрограммированием, что может быть обусловлено экологическими, генетическими или прочими неустановленными факторами.
Идиопатический легочный фиброз: симптомы и признаки
Для идиопатического легочного фиброза характерно постепенное развитие симптоматики: одышки при физических нагрузках и непродуктивного кашля. В редких случаях могут наблюдаться системные проявления (появление субфебрильной температуры, миалгии).
Классически ИЛФ проявляется хорошо различимыми сухими потрескиваниями на вдохе (подобными треску целлофана) в обоих основаниях. В 50% случаев у больных изменяются концевые фаланги пальцев («барабанные палочки»). В терминальной стадии болезни отмечается появление легочной гипертензии. Может развиться систолическая дисфункция правого желудочка.
Идиопатический легочный фиброз: лечение
Единственным методом полного излечения от ИЛФ является трансплантация легкого, так как рубцевание органа фиброзной тканью является необратимым процессом.
Однако своевременное медикаментозное лечение с помощью антифибротических средств обеспечивает значительное замедление патологического процесса, что способствует улучшению качества и продлению жизни больных. Кроме того, пациентам клиники терапии Юсуповской больницы предлагается проведение кислородотерапии, легочной реабилитации.
Фиброзирующий альвеолит – это патологический процесс, в основе которого лежит обширное поражение интерстициальной ткани легких, приводящее к развитию фиброзных изменений и дыхательной недостаточности. Прогрессирование фиброзирующего альвеолита сопровождается неуклонным нарастанием слабости, похудания, одышки, малопродуктивного кашля, болей в грудной клетке, цианоза. Диагностика основывается на данных рентгенографии и компьютерной томографии легких, спирометрии, биопсии легких. Лечение фиброзирующего альвеолита включает противовоспалительную и иммуносупрессивную терапию, оксигенотерапию; по показаниям – трансплантацию легких.
МКБ-10
Общие сведения
Альвеолит фиброзирующий идиопатический (синонимы: фиброз легочный идиопатический, синдром Хаммена-Рича) – прогрессирующее диффузное двухстороннее поражение альвеол и интерстициальной легочной ткани, сопровождающееся развитием диффузного фиброза и нарастающей дыхательной недостаточности. Фиброзирующий альвеолит имеет исключительно легочную локализацию, плохо поддается терапии, часто оканчивается летальным исходом.
Фиброзирующий альвеолит – относительно редкое заболевание неясной этиологии, однако имеет тенденцию к возрастанию. Фиброзирующий альвеолит чаще поражает мужчин старше 50 лет (20 случаев из 100 тыс.), чем женщин (13 случаев из 100 тыс.). Летальность при фиброзирующем альвеолите достигает 3,3 случая на 100 тыс. населения.
Причины
Причины возникновения фиброзирующего альвеолита неясны. Существуют предположения об аутоиммунном характере заболевания, вирусной природе (герпесвирус, вирус гепатита С, аденовирусы, цитомегаловирус), наследственной предрасположенности.
В распространённости фиброзирующего альвеолита имеют значение профессиональные, экологические, бытовые и географические факторы. Так, замечено, что развитию идиопатического фиброзирующего альвеолита в наибольшей степени подвержены фермеры, разводящие птиц, рабочие, контактирующие с древесной, асбестовой, металлической и силикатной пылью, курящие пациенты.
Патогенез
Воспалительные явления в альвеолах вызывают необратимое утолщение их стенок и снижение проницаемости для газообмена. Развитие идиопатического фиброзирующего альвеолита характеризуется тремя взаимосвязанными процессами: интерстициальным отеком, интерстициальным воспалением (альвеолитом) и интерстициальным фиброзом.
В острой стадии интерстициального отека происходит поражение альвеолярных капилляров и эпителия, их отек и формирование гиалиново-мембранных комплексов, препятствующих расширению альвеолярной ткани при дыхании. На этой стадии возможен регресс процесса либо развитие интерстициальной пневмонии. Хроническая стадия интерстициального воспаления характеризуется дальнейшим прогрессированием процесса, отложением в альвеолах коллагена и развитием распространенного фиброза с обширным повреждение легочной ткани.
В терминальной стадии интерстициального фиброза происходит полное замещение капиллярной сети и альвеолярной ткани фиброзной с формированием полостных расширений. Ткань легкого напоминает по внешнему виду пчелиные соты. Необратимые изменения в альвеолярно-капилярной системе легких при фиброзирующем альвеолите приводят к рестриктивным изменениям, расстройству газообмена, прогрессированию дыхательной недостаточности и к гибели пациента.
Классификация
В клинической пульмонологии выделяют 3 формы фиброзирующих альвеолитов:
Симптомы фиброзирующего альвеолита
Развитие заболевания постепенное с развитием необратимых изменений в альвеолах и неуклонным нарастанием одышки. Длительное время пациенты не придают этому значения и не обращаются к врачу, объясняя изменения в своем самочувствии усталостью на работе, прекращением спортивных занятий, набором веса и т. д. Обычно от начала первых симптомов фиброзирующего альвеолита до обращения в медицинское учреждение проходит от 3 месяцев до 1-3 лет.
Ведущими жалобами при фиброзирующем альвеолите служат выраженная одышка при минимальных физических нагрузках и малопродуктивный кашель. Пациентов беспокоят боли в грудной клетке (под лопатками), препятствующие глубокому вдоху, похудание, слабость, мышечные и суставные боли, повышенная температура тела. У половины пациентов с фиброзирующим альвеолитом ногтевые фаланги приобретают характерный вид «барабанных палочек» с «часовыми стеклами». Цианоз и одышка резистентны к проводимой терапии. В дальнейшем происходит нарастание гипоксемии, легочной гипертензии и правожелудочковой недостаточности.
Осложнения
В терминальной стадии фиброзирующего альвеолита усиливаются признаки дыхательной недостаточности и развития легочного сердца: серо-пепельный диффузный цианоз, набухание вен шеи, отеки, развитие кахексии. Течение фиброзирующего альвеолита вызывает прогрессирующую дыхательную недостаточность, развитие легочного сердца, может осложниться отеком легких.
Диагностика
При фиброзирующем альвеолите в легких выслушивается жесткое дыхание, крепитация (симптом «треска целлофана») и сухие хрипы; перкуторный звук укорочен. Изменения со стороны сердца характеризуются тахикардией и приглушенностью тонов. Этапы диагностики:
Проведение открытой биопсии легких при фиброзирующем альвеолите позволяет определить стадию болезни, выбор соответствующего лечения, развитие заболевания. При гистологическом исследовании выделяют пять степеней изменений:
Дифференциальная диагностика
Фиброзирующий альвеолит следует дифференцировать с пневмонией, гранулематозом, саркоидозом, диссеминированным туберкулезом, бронхиолоальвеолярным раком, пневмокониозом, диффузным амилоидозом и др.
Выработаны большие и малые критерии диагностики фиброзирующего альвеолита. С наибольшей вероятностью фиброзирующий альвеолит может быть диагностирован при определении 4-х больших и 3-х малых критериев. Большими критериями верификации идеопатического фиброзирующего альвеолита служат:
К малым критериям идеопатического фиброзирующего альвеолита относятся:
Лечение фиброзирующего альвеолита
Немедикаментозная терапия
Целью проводимого врачом-пульмонологом лечения является облегчение течения заболевания, замедление прогрессирования фиброза легочной ткани, качественное улучшение жизни пациента. К немедикаментозному лечению фиброзирующего альвеолита относятся специальные реабилитационные программы, включающие физические тренировки, психологическую поддержку пациентов. Выраженным терапевтическим эффектом обладает кислородная терапия, уменьшающая одышку и повышающая выносливость физических нагрузок у пациентов с фиброзирующим альвеолитом.
Фармакотерапия
Для достижения состояния ремиссии в медикаментозную терапию фиброзирующего альвеолита включают противовоспалительные (глюкокортикостероиды) и антифиброзные (пеницилламин, колхицин) препараты, иммунодепрессанты (азатиоприн), а также их комбинацию. Одновременно назначаются верошпирон, препараты калия, пиридоксин, бронхолитики. Медикаментозная терапия дает эффект лишь в случаях отсутствия выраженного пневмофиброза. С целью предупреждения вирусных инфекций всем пациентам с фиброзирующим альвеолитом показана противогриппозная и антипневмококковая вакцинация.
Радикальное лечение фиброзирующего альвеолита предусматривает трансплантацию легких, дающую высокий процент 5-летней выживаемости – до 50-60%. Показаниями к пересадке легких служат выраженные гипоксемия, диспноэ, снижение ЖЕЛ ниже 70%, снижение диффузной способности легких.
Прогноз и профилактика
В течении идиопатического фиброзирующего альвеолита после проведения лекарственной терапии наблюдаются периоды ремиссии, однако заболевание все равно постепенно прогрессирует. Средний процент выживаемости при диагностике нелеченных фиброзирующих альвеолитов составляет 3-4 года. Более благоприятным течением отличаются аллергические и токсические альвеолиты, которые при устранении провоцирующего фактора на ранних стадиях могут регрессировать.
Меры профилактики идиопатического фиброзирующего альвеолита включают предупреждение инфекций, исключении вредных профессиональных, экологических и бытовых факторов. Пациенты с фиброзирующим альвеолитом должны находиться на диспансерном учете у пульмонолога, аллерголога и врача-профпатолога.
Идиопатический легочный фиброз (ИЛФ): современный подход к классификации и диагностике
Идиопатический легочный фиброз (ИЛФ) – это вариант идиопатической интерстициальной пневмонии (ИИП), характеризующийся неуклонным прогрессирующим течением и высокой смертностью. В отличие от большинства ИИП, иммуносупрессивная терапия не оказывает влияния на скорость прогрессирования ИЛФ. В течение последнего десятилетия установлена эффективность двух антифибротических препаратов в лечении ИЛФ – пирфенидона и нинтеданиба. Чтобы своевременно начать патогенетическую терапию, необходимо как можно быстрее установить диагноз ИЛФ на основании диагностического алгоритма, предполагающего анализ клинических, лабораторных и инструментальных данных, прежде всего результатов компьютерной томографии высокого разрешения (КТВР). При недостаточной информативности последней может быть использована малоинвазивная трансбронхиальная криобиопсия легкого, которая по точности сопоставима с хирургической биопсией легкого. Продолжается поиск молекулярно-биологических и генетических маркеров ИЛФ.
Согласно классификации Американского торакального общества/Европейского респираторного общества (ATS):1–112. /ERS):1–112. ) [1], идиопатический легочный фиброз (ИЛФ) представляет собой форму идиопатической интерстициальной пневмонии (ИИП) (табл. 1). Доля ИЛФ составляет 20-30% в структуре всех ИИП, а заболеваемость – от 7 до 17 случаев на 100 000 населения [2]. Мужчины болеют несколько чаще, чем женщины (соотношение мужчин/женщин приблизительно 1,5:1) [3]. ИЛФ развивается в основном у людей среднего и пожилого возраста: возраст 65% пациентов на момент постановки диагноза составляет 60 лет и более [4].
| Частые формы ИИП |
| Идиопатический легочный фиброз (ИЛФ) |
| Идиопатическая неспецифическая интерстициальная пневмония |
| Респираторный бронхиолит, ассоциированный с интерстициальным заболеванием легких |
| Десквамативная интерстициальная пневмония |
| Криптогенная организующая пневмония |
| Острая интерстициальная пневмония |
| Редкие формы ИИП |
| Идиопатическая лимфоцитарная интерстициальная пневмония |
| Идиопатический плевропаренхиматозный фиброэластоз |
| Неклассифицируемые формы (ИИП) |
В 2018 году P. Wolters и соавт. предложили выделять 4 варианта легочного фиброза в зависимости от патогенеза заболевания (табл. 2) [5]. ИЛФ характеризуется прогрессирующим течением с развитием дыхательной недостаточности и среди всех ИИП обладает самым неблагоприятным прогнозом: средняя выживаемость составляет от 2 до 5 лет [6,7]. Высокая смертность пациентов с ИЛФ объясняется особенностями патогенеза заболевания – преобладанием фиброза при незначительной выраженности воспалительных изменений [8,9]. Основным механизмом, приводящим к развитию прогрессирующего легочного фиброза, является персистирующее повреждение альвеолярного эпителия с последующим нарушением процессов его регенерации, избыточным отложением компонентов внеклеточного матрикса, активацией фибробластов и миофибробластов [10]. Указанные изменения определяют неэффективность традиционной иммуносупрессивной терапии у пациентов с ИЛФ [11]. Тем не менее, в настоящее время достигнуты значительные успехи в лечении ИЛФ, связанные с применением антифибротических препаратов – пирфенидона (антагониста трансформирующего фактора роста бета – TGF β) и нинтеданиба (множественного ингибитора тирозинкиназ), замедляющих уменьшение легочных объемов, в первую очередь, форсированной жизненной емкости легких (ФЖЕЛ), и улучшающих выживаемость без прогрессирования заболевания [12]. При отсутствии противопоказаний трансплантация легких также рассматривается в качестве варианта лечения у пациентов с прогрессирующим ИЛФ, осложнившимся тяжелой дыхательной недостаточностью [13,14].
| Группа 1: ЛФ, индуцированный дисфункцией эпителиальных клеток | ИЛФ |
| Группа 2: ЛФ, индуцированный дисфункцией клеток воспалени | Системная склеродермия, ревматоидный артрит, синдром Шегрена, экзогенный аллергический альвеолит, саркоидоз, НСИП |
| Группа 3: ЛФ, вызванный приемом лекарственных препаратов или воздействием профессиональных факторов | Асбестоз, силикоз, лекарственное поражение легких |
| Группа 4: ЛФ, связанный с курением | Десквамативная интерстициальная пневмония, респираторный бронхиолит, ассоциированный с интерстициальным заболеванием легких, Лангерганс-клеточный гистиоцитоз |
Клиническая картина
Основные жалобы у пациентов с ИЛФ – прогрессирующая одышка и сухой кашель, усиливающиеся при физической нагрузке. Реже отмечаются боль и дискомфорт в грудной клетке, повышенная утомляемость, общая слабость, снижение массы тела. В ряде случаев заболевание на начальных этапах протекает бессимптомно, а первыми проявлениями оказываются изменения функциональных легочных параметров [1]. Типичным аускультативным феноменом при ИЛФ является крепитация, преимущественно в задне-базальных отделах легких. У больных c развернутой стадией ИЛФ могут отмечаться признаки вторичной артериальной легочной гипертензии с развитием легочного сердца и правожелудочковой сердечной недостаточности [15].
При ИЛФ может определяться незначительное повышение СОЭ. Несмотря на наличие прогрессирующей дыхательной недостаточности, выраженное увеличение концентрации гемоглобина наблюдается крайне редко. уменьшением всех легочных объемов в сочетании со снижением диффузионной способности легких (DLCO). Одним из ранних проявлений ИЛФ может быть изолированное снижение DLCO при относительной сохранности легочных объемов. Также к ранним проявлениям ИЛФ относят увеличение альвеолоартериального градиента по кислороду, что часто характеризуется нормальными показателями сатурации крови в покое и десатурацией при физической нагрузке [16].
Диагностический алгоритм
Диагноз ИЛФ основывается на отсутствии известных причин легочного фиброза и наличии картины обычной интерстициальной пневмонии (ОИП) [17]. Даже при наличии гистологической картины ОИП при хирургической биопсии легкого (ХБЛ) окончательный диагноз требует исключения других патологических состояний, ассоциированных с развитием ОИП, включая диффузные заболевания соединительной ткани, пневмокониозы, поражение легких, связанное с приемом лекарственных препаратов, семейный легочный фиброз [18]. При отсутствии данных за альтернативный диагноз, согласно действующим клиническим рекомендациям [4], диагноз ИЛФ устанавливают на основании характерных данных компьютерной томографии высокого разрешения (КТВР) и, при необходимости, результатов биопсии легкого (табл. 3). Следует отметить, что в представленной гистологической классификации выделены «возможный ИЛФ» и «вероятный ИЛФ», когда невозможно однозначно подтвердить или исключить наличие ИЛФ. В таком случае показана повторная оценка данных КТВР и биопсии легкого для уточнения диагноза.
| КТ-картина | Гистологические данные | Диагноз |
|---|---|---|
| ОИП | ОИП | ИЛФ |
| Вероятная ОИП | ||
| Возможная ОИП | ||
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП | Не-ИЛФ | |
| Возможная ОИП | ОИП Вероятная ОИП | ИЛФ |
| Возможная ОИП | Вероятный ИЛФ | |
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП | Не-ИЛФ | |
| Не соответствует ОИП | ОИП | Возможный ИЛФ |
| Вероятная ОИП | Не-ИЛФ | |
| Возможная ОИП | ||
| Неклассифицируемый фиброз | ||
| Не соответствует ОИП |
КТ-диагностика
КТВР играет ключевую роль в диагностике ИЛФ и позволяет установить диагноз приблизительно в 2/3 случаев. В ряде исследований было показано, что КТ-картина типичной ОИП по данным КТВР согласуется с наличием гистологической картины типичной ОИП по данным биопсии легкого в 90-100% случаев [4]. Наличие достоверных КТ-признаков ОИП в настоящее время считают достаточным для диагностики ИЛФ без биопсии легкого. Проведение хирургической биопсии легкого (ХБЛ) рекомендуется при наличии КТ-картины, не типичной для ОИП. В таких случаях диагноз устанавливают на основании сочетания данных КТВР и гистологической картины (табл. 3). Таким образом, точная интерпретация данных КТВР является необходимым условием для постановки диагноза [1].
В настоящее время выделяют три КТ-варианта ОИП «типичная ОИП», которая исключает необходимость проведения ХБЛ, «возможная ОИП» и «не соответствует ОИП». При наличии последних двух вариантов требуется проведение ХБЛ [19].
КТ-картина типичной ОИП включает в себя преимущественно базальные и периферические ретикулярные изменения с образованием сотового легкого в сочетании с тракционными бронхоэктазами или без них. Критериями «сотового легкого» считают преимущественно субплевральные кисты диаметром 3-10 мм с четкими, относительно толстыми стенками (1-3 мм), расположенные слоями. Все КТ-признаки, рассматриваемые как «не соответствующие» ОИП, должны отсутствовать (рис. 1). Если все вышеуказанные критерии выполнены, данные КТВР достаточны для диагностики ОИП, а необходимости в проведения биопсии легкого нет [4]. Относительно признаков типичной ОИП заключения разных специалистов обычно хорошо согласуются [20,21]. Тем не менее, следует отметить, что ОИП и ИЛФ не являются синонимами, так как КТизменения, характерные для ОИП, могут отмечаться при ряде других заболеваний, прежде всего диффузных заболеваниях соединительной ткани.
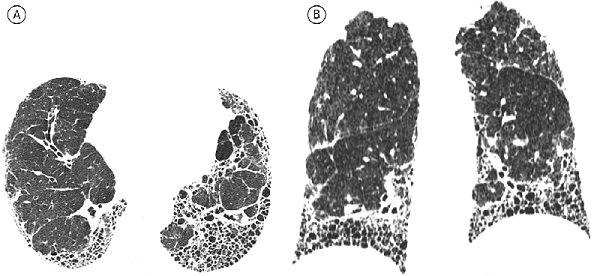
При возможной ОИП наблюдаются преимущественно базальные и периферические ретикулярные изменения без формирования зон сотового легкого. При этом изменения, не соответствующие ОИП, отсутствуют (рис. 2). Картина возможной ОИП менее специфична для ИЛФ, чем картина типичной ОИП. В данном случае дифференциальный диагноз следует проводить, в первую очередь, с неспецифической интерстициальной пневмонией (НСИП), для которой характерны отсутствие участков сотового легкого, преобладание затемнений по типу «матового стекла» над ретикулярными изменениями, относительная сохранность субплевральных зон. Участки сотовой трансформации редко встречаются при НСИП. В одном исследовании они были выявлены менее чем у 5% пациентов с идиопатической НСИП [23].
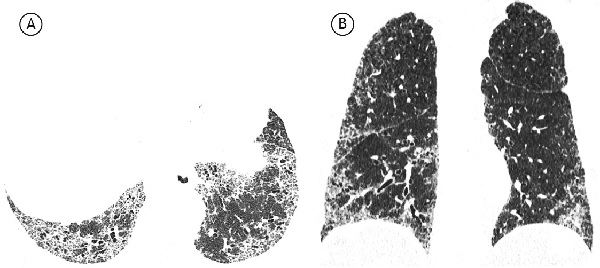
Изменения по данным КТВР, которые считают не соответствующими ОИП, включают в себя следующие: а) преобладание изменений в верхних и средних отделах легких; б) преимущественно перибронховаскулярные изменения; в) значительные по размеру зоны затемнения по типу «матового стекла», распростра ненность которых превышает таковую ретикулярных изменений; г) двусторонние очаговые изменения, преимущественно в верхних отделах легких; д) наличие кист (множественных, двусторонних) вне зон фиброза; е) картина мозаичного затемнения легочной ткани/ наличие «воздушных ловушек» (двусторонние изменения в трех и более долях); ж) наличие зон консолидации (рис. 3).
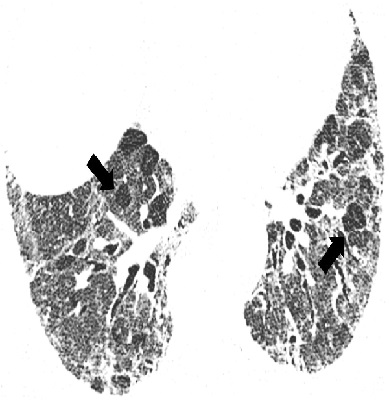
Несмотря на высокую вероятность наличия ИЛФ при типичной ОИП по данным КТВР, отсутствие зарактерной КТ-картины не должно служить основанием для исключения диагноза ИЛФ [22]. В 2017 г. D. Lynch и соавт. предложили новую КТ-классификацию ОИП, в которой впервые выделена группа неопределенной ОИП (табл. 4) [24].
| Типичная ОИП | Вероятная ОИП | Неопределенная ОИП | Наименее вероятно соответствует ОИП |
|---|---|---|---|
| Преобладание в базальных и субплевральных отделах (редко диффузные изменения); часто неоднородное распределение Зоны «сотового легкого»; ретикулярные изменения с периферическими тракционными бронхо эктазами и бронхиолоэктазами; отсутствие данных за альтернативный диагноз | Преобладание в базальных и субплевральных отделах; часто неоднородное распределение Ретикулярные изменения с периферическими тракционным бронхоэктазами и бронхиолоэктазами; отсутствие зон «сотового легкого»; отсутствие данных за альтернативный диагноз | Вариабельное или диффузное распределение Наличие фиброза в сочетании с небольшими по объему изменениями, не соответствующими ОИП | Преобладание в верхних и средних отделах легких; перибронховаскулярное распределение с относительной сохранностью субплевральных зон Любое из нижеперечисленного: преобладание зон консолидации; значительные по размеру зоны затемнения по типу «матового стекла» (при отсутствии обострения ИЛФ); диффузные очаговые или кистозные изменения; выраженное мозаичное затемнение легочной ткани с наличием «воздушных ловушек» |
Клиническое течение ИЛФ может быть различным. У большинства пациентов отмечается медленно прогрессирующее течение, однако у некоторых пациентов происходит стабилизация патологического процесса, тогда как у других отмечается довольно быстрое прогрессирование заболевания. Что касается выраженности легочных изменений по данным КТВР, то зоны затемнения по типу «матового стекла» чаще всего трансформируются в ретикулярные изменения, которые, в свою очередь, могут прогрессировать и формировать зоны «сотового легкого», размер которых со временем обычно увеличивается. Следует отметить, что общий паттерн легочных изменений также может изменяться: так, КТкартина возможной ОИП может трансформироваться в типичную ОИП [22].
Биопсия легкого
Если однозначные данные о наличии ИЛФ при КТВР отсутствуют, то для подтверждения диагноза показано выполнение хирургической биопсии легких, которую чаще проводят с помощью видеоторакоскопической методики. С целью повышение эффективности биопсия легких должна производиться из разных долей легких. Хотя ХБЛ является наиболее достоверным методом определения гистологической картины ИИП, ее проведение связано с риском возникновения ряда осложнений, наиболее тяжелым из которых является обострение ИЛФ, особенно у пациентов с тяжелой дыхательной и/или сердечной недостаточностью [25]. В связи с этим решение о ее проведении должно приниматься индивидуально с учетом клинической картины, возможных преимуществ для постановки точного диагноза, а также согласия пациента.
В течение последнего десятилетия для гистологического подтверждения диагноза ИЛФ и других вариантов ИИП разработана методика трансбронхиальной криобиопсии легкого (ТБКБЛ). Ее основными преимуществами являются малоинвазивность, отсутствие необходимости в проведении интубации и ингаляционного наркоза и, вследствие этого, низкая частота развития осложнений в сочетании с возможностью получения большого по объему биоптата легкого, достаточного, в абсолютном большинстве случаев, для гистологической верификации диагноза [26]. Так, у пациентов без типичной картины ОИП по данным КТВР проведение ТБКБЛ позволяло установить диагноз приблизительно в 2/3 случаев, что сопоставимо с эффективностью ХБЛ в сходной ситуации [27]. При этом для ТБКБЛ характерны более низкий риск периоперационных осложнений (чаще всего отмечают развитие пневмоторакса и не угрожающего жизни кровотечения в месте проведения биопсии) и смерти, более короткий период госпитализации, что позволяет проводить ТБКБЛ у пациентов с высоким уровнем анестезиологического риска и наличием противопоказаний к ХБЛ [28].Таким образом, внедрение ТБКБЛ в клиническую практику может расширить показания к биопсии легкого и повысить диагностическую точность алгоритма обследования пациентов с подозрением на ИЛФ.
При морфологическом исследовании у пациентов с подозрением на ИЛФ G. Raghu и соавт. выделяют пять возможных гистологических паттернов заболевания (табл. 5) [29,4]. В сочетании с рентгенологическими данными они используются для подтверждения/исключения диагноза ИЛФ (табл. 3) [4,30].
Дифференциальный диагноз
У пациентов с подозрением на ИЛФ должен проводиться тщательный дифференциальный диагноз. При выявлении КТ-картины, соответствующей вероятной или возможной ОИП, что происходит довольно часто, в круг дифференциального диагноза следует включать, в первую очередь, хронический экзогенный аллергический альвеолит и фибротический вариант НСИП. Тем не менее, у части пациентов рекомендованная в данном случае ХБЛ не проводится в связи с наличием противопоказаний (тяжелой дыхательной недостаточности, сопутствующих заболеваний, возрастных ограничений) или нежеланием пациента.
При проведении дифференциального диагноза важно также исключить поражение легких в рамках системного заболевания соединительной ткани, в частности, ревматоидного артрита, системной склеродермии, дерматомиозита, синдрома Шегрена [31], в том числе при наличии КТ-картины типичной ОИП. При наличии у пациента отдельных клинических проявлений или повышения уровня лабораторных аутоиммунных маркеров, не соответствующих конкретному системному заболеванию соединительной ткани, может быть установлен диагноз интерстициальной пневмонии с аутоиммунными чертами [32].
Генетические маркеры ИЛФ
В настоящее время выявлен ряд мутаций и полиморфизмов генов, участвующих в ремоделировании легочной ткани и регуляции врожденного и приобретенного иммунитета, ассоциированных с развитием ИЛФ [33]. К ним относятся, в частности, мутации в генах, кодирующих сурфактантные протеины А и D (S):1–112. P-A и S):1–112. PD), описанные при семейных формах ИЛФ [34]. В ряде исследований выявлена ассоциация генетических полиморфизмов с прогнозом заболевания: в частности, наличие отдельных однонуклеотидных полиморфизмов в гене TLR-3 (Toll-подобный рецептор 3-го типа) ассоциировано с более быстрым прогрессированием заболевания [35]. Также при ИЛФ описан ряд полиморфизмов в генах муцина 5B (MUC5B) и TOLLIP (протеин, взаимодействующий с Toll-подобным рецептором) [36]. Хотя исследование генетических полиморфизмов не является частью диагностического алгоритма при ИЛФ, продолжается поиск генетических маркеров, способных служить предикторами различных вариантов течения заболевания и ответа на терапию.
Обострение ИЛФ
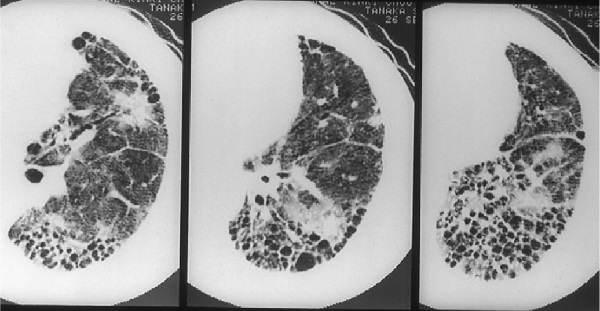
Обострение ИЛФ – это тяжелое жизнеугрожающее состояние, проявляющееся в виде быстрого нарастания дыхательной недостаточности у пациентов с ранее установленным диагнозом ИЛФ [37]. Как правило, характеризуется крайне тяжелым течением; смертность в ряде исследований достигала 85% [38]. В отличие от стабильного или медленно прогрессирующего течения ИЛФ, критерии диагностики его обострения определены менее четко. Согласно данным Н. Collard и соавт. [39], критерии обострения ИЛФ включают в себя наличие предшествующего или впервые выявленного ИЛФ с резким нарастанием одышки, развитием дыхательной недостаточности за предшествующие 30 дней без установленной причины, а также появление новых зон затемнения легочной ткани по типу «матового стекла» и/или консолидации на фоне имевшихся ранее изменений, соответствующих ОИП – зон ретикулярных изменений и «сотового легкого» (рис. 4) [40]. Тем не менее, вышеуказанные критерии обладают низкой специфичностью, в связи с чем при подозрении на обострение ИЛФ должен проводиться дифференциальный диагноз с инфекционным процессом, тромбоэмболией легочной артерии и ее ветвей, пневмотораксом, а также острой левожелудочковой недостаточностью с развитием отека легких [41].
Заключение
Появление новых методов лечения, в частности, антифибротических препаратов, и неэффективность традиционной иммуносупрессивной терапии при ИЛФ подчеркивают важность как можно более ранней постановки диагноза и начала терапии. В течение последнего десятилетия был достигнут значительный прогресс в разработке диагностических алгоритмов для пациентов с ИЛФ. Этому способствовало повышение качества визуализационных методов, более полное понимание роли биопсии легких и разработка гистологических критериев ИЛФ. Все вышеперечисленные параметры должны исследоваться мультидисциплинарной командой специалистов, что в настоящий момент является стандартом диагностики ИЛФ. Несмотря на достигнутые успехи, в диагностике ИЛФ остаются нерешенные вопросы, в основном касающиеся применения инвазивных методов диагностики, в частности, хирургической биопсии легкого. Необходимо продолжать поиск молекулярно-биологических и генетических маркеров ИЛФ и разработку малоинвазивных биопсийных методов для максимально раннего установления диагноза, определения прогноза и разработки стратегии терапии ИЛФ.