Инсулинемия что это такое
Инсулинома
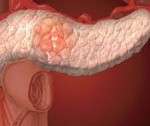
Инсулинома – гормонально-активная опухоль β-клеток островков поджелудочной железы, в избыточном количестве секретирующая инсулин и приводящая к развитию гипогликемии. Гипогликемические приступы при инсулиноме сопровождаются дрожью, холодным потом, чувством голода и страха, тахикардией, парестезиями, речевыми, зрительными и поведенческими нарушениями; в тяжелых случаях – судорогами и комой. Диагностика инсулиномы проводится с помощью функциональных проб, определения уровня инсулина, С-пептида, проинсулина и глюкозы крови, УЗИ поджелудочной железы, селективной ангиографии. При инсулиноме показано хирургическое лечение – энуклеация опухоли, резекция поджелудочной железы, панкреатодуоденальная резекция или тотальная панкреатэктомия.
Общие сведения
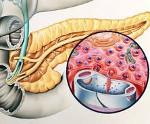
Инсулинома – доброкачественная (в 85-90% случаев) или злокачественная (в 10-15% случаев) опухоль, исходящая из β-клеток островков Лангерганса, обладающая автономной гормональной активностью и приводящая к гиперинсулинизму. Неконтролируемая секреция инсулина сопровождается развитием гипогликемического синдрома – комплекса адренергических и нейрогликопенических проявлений.
Среди гормонально-активных опухолей поджелудочной железы инсулиномы составляют 70-75%; примерно в 10% наблюдений они являются компонентом множественного эндокринного аденоматоза I типа (наряду с гастриномой, опухолями гипофиза, аденомой паращитовидных желез и др.). Инсулиномы чаще выявляются у лиц в возрасте 40-60 лет, у детей встречаются редко. Инсулинома может располагаться в любой части поджелудочной железы (головке, теле, хвосте); в единичных случаях она локализуется экстрапанкреатически – в стенке желудка или двенадцатиперстной кишки, сальнике, воротах селезенки, печени и др. областях. Обычно размеры инсулиномы составляют 1,5 – 2 см.
Патогенез гипогликемии при инсулиноме
Развитие гипогликемии при инсулиноме обусловлено избыточной, неконтролируемой секрецией инсулина опухолевыми b-клетками. В норме при падении уровня глюкозы в крови происходит снижение продукции инсулина и его поступления в кровяное русло. В опухолевых клетках механизм регуляция выработки инсулина нарушается: при понижении уровня глюкозы его секреция не подавляется, что создает условия для развития гипогликемического синдрома.
Наиболее чувствительными к гипогликемии являются клетки головного мозга, для которых глюкоза служит основным энергетическим субстратом. В связи с этим при инсулиноме отмечаются явления нейрогликопении, а при длительной гипогликемии развиваются дистрофические изменения ЦНС. Гипогликемическое состояние стимулирует выброс в кровь контринсулярных гормонов (норадреналина, глюкагона, кортизола, соматотропина), которые обусловливают адренергическую симптоматику.
Симптомы инсулиномы
В течении инсулиномы выделяют фазы относительного благополучия, на смену которым периодически приходят клинически выраженные проявления гипогликемиии и реактивной гиперадреналинемии. В латентном периоде единственными проявлениями инсулиномы могут являться ожирение и повышенный аппетит.
Острый гипогликемический приступ является результатом срыва адаптационных механизмов ЦНС и контринсулярных факторов. Приступ развивается натощак, после продолжительного перерыва в приеме пищи, чаще в утренние часы. Во время приступа происходит падение содержания глюкозы в крови ниже 2,5 ммоль/л.
Нейрогликопенические симптомы инсулиномы могут напоминать различные неврологические и психиатрические нарушения. У больных может возникать головная боль, мышечная слабость, атаксия, спутанность сознания. В некоторых случаях гипогликемический приступ у больных с инсулиномой сопровождается состоянием психомоторного возбуждения: галлюцинациями, бессвязными выкриками, двигательным беспокойством, немотивированной агрессией, эйфорией.
Реакцией симпатико-адреналовой системы на резкую гипогликемию служит появление тремора, холодного пота, тахикардии, страха, парестезий. При прогрессировании приступа могут развиться эпилептический припадок, потеря сознания и кома. Обычно приступ купируется внутривенным вливанием глюкозы; однако, придя в себя, больные о случившемся не помнят. Во время гипогликемического приступа возможно развитие инфаркта миокарда вследствие острого нарушения питания сердечной мышцы, признаки локального поражения нервной системы (гемиплегия, афазия), которые могут быть ошибочно приняты за ОНМК.
При хронической гипогликемии у пациентов с инсулиномой нарушается функционирование центральной и периферической нервной системы, что отражается на течении фазы относительного благополучия. В межприступном периоде имеет место преходящая неврологическая симптоматика, нарушения зрения, миалгия, снижение памяти и умственных способностей, апатия. Даже после удаления инсулиномы снижение интеллекта и энцефалопатия обычно сохраняются, что приводит к утрате профессиональных навыков и прежнего социального статуса. У мужчин при часто повторяющихся приступах гипогликемии может развиваться импотенция.
При неврологическом обследовании у пациентов с инсулиномой выявляется асимметрия периостальных и сухожильных рефлексов, неравномерность или снижение брюшных рефлексов, патологические рефлексы Россолимо, Бабинского, Маринеску-Радовича, нистагм, парез взора вверх и др. Ввиду полиморфности и неспецифичности клинических проявлений, больным с инсулиномой могут ставиться ошибочные диагнозы эпилепсии, опухоли головного мозга, вегетососудистой дистонии, инсульта, диэнцефального синдрома, острого психоза, неврастении, остаточных явлений нейроинфекции и пр.
Диагностика инсулиномы
Установить причины гипогликемии и дифференцировать инсулиному от других клинических синдромов позволяет комплекс лабораторных тестов, функциональных проб, визуализирующих инструментальных исследований. Проба с голоданием направлена на провокацию гипогликемии и вызывает патогномоничную для инсулиномы триаду Уиппла: снижение глюкозы крови до 2,78 ммоль/л или ниже, развитие нервно-психических проявлений на фоне голодания, возможность купирования приступа пероральным приемом или внутривенным вливанием глюкозы.
С целью индуцирования гипогликемического состояния может использоваться инсулиносупрессивный тест с введением экзогенного инсулина. При этом отмечаются неадекватно высокие концентрации C-пептида в крови на фоне крайне низких показателей глюкозы. Проведение инсулинпровокационного теста (внутривенного введения глюкозы или глюкагона) способствует высвобождению эндогенного инсулина, уровень которого у больных с инсулиномой становится существенно выше, чем у здоровых лиц; при этом соотношение инсулина и глюкозы превышает 0,4 (в норме менее 0,4).
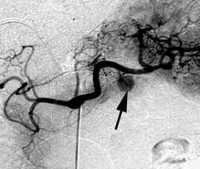
При положительных результатах провокационных проб проводится топическая диагностика инсулиномы: УЗИ поджелудочной железы и брюшной полости, сцинтиграфия, МРТ поджелудочной железы, селективная ангиография с забором крови из портальных вен, диагностическая лапароскопия, интраоперационная ультрасонография поджелудочной железы. Инсулиному приходится дифференцировать от лекарственной и алкогольной гипогликемии, гипофизарной и надпочечниковой недостаточности, рака надпочечников, демпинг-синдрома, галактоземии и др. состояний.
Лечение инсулиномы
В эндокринологии в отношении инсулиномы предпочтение отдается хирургической тактике. Объем операции определяется локализацией и размерами образования. При инсулиноме может выполняться как энуклеация опухоли (инсулиномэктомия), так и различные виды резекций поджелудочной железы (дистальная, резекция головки, панкреатодуоденальная резекция, тотальная панкреатэктомия). Эффективность вмешательства оценивается с помощью динамического определения уровня глюкозы крови в процессе операции. В числе послеоперационных осложнений могут развиваться панкреатит, панкреонекроз, свищи поджелудочной железы, абсцесс брюшной полости или перитонит.
При неоперабельных инсулиномах проводят консервативную терапию, направленную на купирование и профилактику гипогликемии, с помощью гипергликемизирующих средств (адреналина, норадреналина, глюкагона, глюкокортикоидов и др.). При злокачественных инсулиномах проводится химиотерапия (стрептозотоцин, 5-фторурацил, доксорубицин и др.).
Прогноз при инсулиноме
У 65-80% больных после хирургического удаления инсулиномы наступает клиническое выздоровление. Ранняя диагностика и своевременное хирургическое лечение инсулиномы приводят к регрессу изменений со стороны ЦНС по данным ЭЭГ.

Чем опасна инсулинорезистентность?
Даже у людей без серьезных изменений в обмене веществ инсулинорезистентность запускает процессы раннего старения, также сегодня известно, что именно она связана с тяжелыми сердечно-сосудистыми патологиями и их опасными осложнения (инсульт, инфаркт, острые нарушения мозгового кровообращения, диабетическая нейропатия и пр.).
Инсулинорезистентность распространена очень широко. У 10-15% взрослых людей (без хронических заболеваний и диагнозов) может быть выявлена случайно, при каких-либо обследованиях. А это значит, что тысячи людей не только не знают о ней, но и находятся под прицелом опасных заболеваний!
Может показаться, что инсулинорезистентность — очень коварный и скрытый враг здоровья, но на самом деле эта маскировка весьма условна, потому что отклонение можно заподозрить при наличии конкретных проблем внешности и самочувствия.
Например, всем женщинам, особенно среднего возраста, знакома проблема избыточного веса. Наступает момент, когда лишние килограммы буквально срастаются с организмом, их практически невозможно сбросить, никакие диеты не помогают. Причем создается ощущение, что вес лишний вес сконцентрирован в области живота — вот почему многие женщины мечтают похудеть именно в талии, накачать пресс, не придавая значения другим частям тела. Между тем, возраст и скопление жировой ткани в области живота (так называемое абдоминальное ожирение, по центральному типу) — это два важнейших фактора, запускающих развитие инсулинорезистентности и поддерживающих ее усиление.
У женщин после 35 лет возможны разнообразные гормональные отклонения, которые в этом возрасте пока не приводят к развитию заболеваний, но создают «шторм» в организме. Колебания содержания эстрогенов и тестостерона (причем задолго до наступления климакса), уменьшение концентрации гормонов щитовидной железы и повышенное выделение гормонов стресса — адреналина, кортизола — все это влияет в первую очередь на физическое здоровье. Постепенно копятся проблемы, которые связаны друг с другом: избыточный вес, повышение уровня холестерина в крови, высокое давление. Инсулинорезистентность может быть как следствием этих изменений в организме, так и их верным спутником.
Если задуматься, то в жизни каждой из нас есть хотя бы парочка перечисленных вредных факторов, так что если какая-то проблема беспокоит давно и серьезно (никак не получается похудеть, постоянно повышенное давление, головные боли и слабость), стоит обратиться к врачу и описать ему полную картину своих симптомов. Нередко расставить все точки над i помогает врач-эндокринолог и проведение нескольких анализов (глюкоза, глюкозотолерантный тест, гликированный гемоглобин, индекс инсулинорезистентности и др.).
Роль инсулина в организме
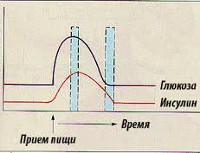
Инсулин — важнейший гормон, который выделяется в поджелудочной железе, и единственный гормон организма, снижающий концентрацию глюкозы в крови. Инсулин участвует во многих важных биологических реакциях, например, активирует образование белков в мышцах, поддерживает накопление жиров в печени, но именно регулирующий эффект в отношении глюкозы составляет основу его уникального действия.
Многие ткани в организме зависимы от присутствия инсулина: это, в первую очередь, мышечная и жировая ткани (и все остальные ткани, кроме нервной). Инсулин здесь работает как ключ — открывает доступ глюкозы в клетку, где она используется для получения энергии, сжигается. Если этот механизм перестает работать, клетки становятся нечувствительны к инсулину, развивается инсулинорезистентность.
Записаться на прием вы можете по телефонам:
+7(495) 210-02-48 +7(495) 799-02-06
Инсулинорезистентность, сахарный диабет и метаболический синдром
Устойчивость тканей к действию инсулина связывают в первую очередь с развитием сахарного диабета второго типа, но выявлена также четкая связь с ожирением, артериальной гипертонией, тяжелыми нарушениями липидного обмена. Когда инсулинорезистентность сочетается с другими факторами и показателями организма, говорят о метаболическом синдроме (синдроме инсулинорезистентости). При постановке такого диагноза имеют значение очень многие показатели, но самые основные следующие (сочетание по крайней мере 3 из них):
Важно вовремя обнаружить патологические изменения в организме и начать лечение, основой которого являются прежде всего изменение образа жизни, правильное питание. Врач-эндокринолог составит рацион, порекомендует режим активности и, при необходимости, лекарственные средства.
Коррекция инсулинорезистентности и метаболического синдрома
В обоих случаях проблема решаема: сегодня разработаны эффективные схемы коррекции этих обменных нарушений. При грамотном профессиональном подходе удается восстановить чувствительность к инсулину, улучшить обмен веществ и привести организм в норму.
Соблюдение определенной диеты, в результате которой снижается масса тела, является той мерой, без которой нельзя обойтись! Нередко одно только снижение веса приводит к улучшению самочувствия, смягчению течения хронических заболеваний (артериальной гипертензии, ишемической болезни сердца, жировой болезни печени и других), к нормализации показателей анализов (например, снижается концентрация «плохого» холестерина, увеличивается концентрация «хорошего»).
Причем тот режим питания, которые рекомендован мировыми медицинскими сообществами, ничего общего не имеет с диетами для быстрого снижения веса: для здоровья и восстановления организма важна медленная потеря килограммов (от 500 г до 1 кг в неделю, в течение 4-6 месяцев), таким образом уходит до 15% исходной массы, а риск возвращения килограммов очень низкий.
Осторожно нужно относиться к диетам, при соблюдении которых теряется более 5 кг в месяц, так как это может усилить обменные нарушения и привести впоследствии к увеличению массы тела. Строгие диеты негативно сказываются на психологическом состоянии, особенно у женщин в начальном периоде климакса, необходимость соблюдения диеты сама по себе неприятна, поэтому организм требует компенсации! Из-за этого на фоне постоянного голода возможны переедания, на фоне стресса — возврат к вредным привычкам (курение, алкоголь). Кроме того, жесткие ограничения в еде (отсутствие углеводов, очень низкая калорийность и пр.) мало того, что приводят к потере мышечной массы, еще и способствуют развитию или усилению инсулинорезистентности.
Питание строится на принципах здорового образа жизни:
Физкультура нужна людям с любыми значениями массы тела, так как именно двигательная активность закрепляет эффект снижения веса и положительно влияет на сердечно-сосудистую и опорно-двигательную системы. Очень важно участие в процессе спортивного врача, фитнес-тренера или инструктора по ЛФК, так как это гарантирует отсутствие нежелательных явлений при занятиях, хорошее самочувствие и снижает риск обострений хронических заболеваний.
Лечение имеющихся болезней и отклонений
Весь процесс коррекции инсулинорезистентности и метаболического синдрома невозможен без лечения имеющихся заболеваний. Это может быть артериальная гипертония, стенокардия, сахарный диабет, заболевания пищеварительной системы, суставов и позвоночника. Необходимо соблюдать все рекомендации врача по применению лекарственных средств при этих патологиях.
Диагностика и коррекция инсулинорезистентности в ТН-Клинике.
Для определения инсулинорезистентности и скрытого диабета проводятся разнообразные анализы. Наибольшее практическое значение имеют следующие:
пероральный глюкозо-толерантный тест, в процессе проведения которого оценивается дважды уровень глюкозы в крови (из вены) — до и после (через 2 часа) приема 75 мл раствора глюкозы; тест проводится при отклонениях от нормы концентрации глюкозы натощак или при наличии высокого риска развития диабета; анализ сдается строго натощак;
анализ крови на гликированный гемоглобин (форма гемоглобина, образующаяся при соединении с глюкозой) отражает средний уровень глюкозы в крови за последние 3 месяца; используется в том числе для диагностики скрытого сахарного диабета; анализ сдается натощак.
Оценка результатов анализов — это задача врача. В ТН-Клинике опытные врачи-эндокринологи проанализируют полученные данные и при необходимости составят план коррекции состояния. Исследования и оценка результатов занимают несколько часов, пациент все это время находится в клинике.
Обратившись в ТН-Клинику, вы сможете точно узнать, что именно является причиной лишнего веса, проблем внешности и здоровья. Небольшие корректировки питания и образа жизни помогут вернуться к нормальному весу и улучшить состояние здоровья.
Остались вопросы
Записаться на прием и получить подробную информацию вы всегда можете у специалистов нашего консультативного отдела по телефонам:
Титова Елена Ивановна
Главный врач ТН-Клиники. Врач-гинеколог, маммолог, кандидат медицинских наук, нутрициолог, специалист по антивозрастной медицине.
Ультразвуковое исследование щитовидной железы и паращитовидных желез
Биопсия щитовидной железы и паращитовидных желез под контролем УЗИ
Гиперинсулинизм
Гиперинсулинизм — клинический синдром, характеризующийся повышением уровня инсулина и снижением сахара в крови. Гипогликемия приводит к слабости, головокружению, повышению аппетита, тремору, психомоторному возбуждению. При отсутствии своевременного лечения развивается гипогликемическая кома. Диагностика причин состояния основывается на особенностях клинической картины, данных функциональных проб, динамическом исследовании глюкозы, ультразвуковом или томографическом сканировании поджелудочной железы. Лечение панкреатических новообразований – хирургическое. При внепанкреатическом варианте синдрома проводят терапию основного заболевания, назначают специальную диету.
Общие сведения
Причины гиперинсулинизма
Врожденная патология возникает вследствие внутриутробных аномалий развития, задержки роста плода, мутаций в геноме. Причины возникновения приобретенной гипогликемической болезни разделяют на панкреатические, приводящие к развитию абсолютной гиперинсулинемии, и непанкреатические, вызывающие относительное повышение уровня инсулина. Панкреатическая форма болезни встречается при злокачественных или доброкачественных новообразованиях, а также гиперплазии бета-клеток поджелудочной железы. Непанкреатическая форма развивается при следующих состояниях:
Патогенез
Глюкоза является главным питательным субстратом центральной нервной системы и необходима для нормального функционирования головного мозга. Повышенный уровень инсулина, накопление гликогена в печени и торможение гликогенолиза приводит к снижению уровня глюкозы в крови. Гипогликемия вызывает торможение метаболических и энергетических процессов в клетках головного мозга. Происходит стимуляция симпатоадреналовой системы, увеличивается выработка катехоламинов, развивается приступ гиперинсулинизма (тахикардия, раздражительность, чувство страха). Нарушение окислительно-восстановительных процессов в организме приводит к снижению потребления кислорода клетками коры головного мозга и развитию гипоксии (сонливость, заторможенность, апатия). Дальнейший дефицит глюкозы вызывает нарушение всех обменных процессов в организме, увеличение притока крови к мозговым структурам и спазм периферических сосудов, что может привести к инфаркту. При вовлечении в патологический процесс древних структур мозга (продолговатый и средний мозг, варолиев мост) развиваются судорожные состояния, диплопия, а также нарушение дыхательной и сердечной деятельности.
Классификация
В клинической эндокринологии наиболее часто используется классификация гиперинсулинемии в зависимости от причин возникновения заболевания:
Симптомы гиперинсулинизма
Клиническая картина гипогликемической болезни обусловлена понижением уровня глюкозы в крови. Развитие приступа начинается с повышения аппетита, потливости, слабости, тахикардии и ощущения голода. Позже присоединяются панические состояния: чувство страха, тревога, раздражительность, дрожь в конечностях. При дальнейшем развитии приступа отмечается дезориентация в пространстве, диплопия, парестезии (онемение, покалывание) в конечностях, вплоть до возникновения судорог. При отсутствии лечения наступает потеря сознания и гипогликемическая кома. Межприступный период проявляется снижением памяти, эмоциональной лабильностью, апатией, нарушением чувствительности и онемением в конечностях. Частый прием пищи, богатой легкоусвояемыми углеводами, провоцирует увеличение массы тела и развитие ожирения.
В современной практике выделяют 3 степени гиперинсулинизма в зависимости от тяжести течения болезни: легкую, среднюю и тяжелую. Легкая степень проявляется отсутствием симптоматики межприступного периода и органического поражения коры головного мозга. Обострения болезни проявляются реже 1 раза в месяц и быстро купируются медикаментозными препаратами или сладкой пищей. При средней степени тяжести приступы возникают чаще 1 раза в месяц, возможна потеря сознания и развитие коматозного состояния. Межприступный период характеризуется легкими нарушениями поведенческого характера (забывчивость, снижение мышления). Тяжелая степень развивается при необратимых изменениях коры головного мозга. При этом приступы случаются часто и заканчиваются потерей сознания. В межприступном периоде пациент дезориентирован, память резко снижена, отмечается тремор конечностей, характерна резкая смена настроения и повышенная раздражительность.
Осложнения гиперинсулинизма
Осложнения можно условно разделить на ранние и поздние. К ранним осложнениям, возникающим в ближайшие часы после приступа, относят инсульт, инфаркт миокарда вследствие резкого снижения метаболизма сердечной мышцы и головного мозга. В тяжелых ситуациях развивается гипогликемическая кома. Поздние осложнения проявляются спустя несколько месяцев или лет от начала болезни и характеризуются нарушением памяти и речи, паркинсонизмом, энцефалопатией. Отсутствие своевременного диагностики и лечения заболевания приводит к истощению эндокринной функции поджелудочной железы и развитию сахарного диабета, метаболического синдрома, ожирения. Врожденный гиперинсулинизм в 30% случаев приводит к хронической гипоксии головного мозга и снижению полноценного умственного развития ребенка.
Диагностика гиперинсулинизма
Диагностика основывается на клинической картине (потеря сознания, тремор, психомоторное возбуждение), данных анамнеза заболевания (время начала приступа, его связь с приемом пищи). Эндокринолог уточняет наличие сопутствующих и наследственных заболеваний (жировой гепатоз, сахарный диабет, синдром Иценко-Кушинга), после чего назначает лабораторные и инструментальные исследования. Пациенту проводится суточное измерение уровня глюкозы крови (гликемический профиль). При выявлении отклонений выполняют функциональные пробы. Проба с голоданием используется для дифференциальной диагностики первичного и вторичного гиперинсулинизма. Во время теста измеряют С-пептид, иммунореактивный инсулин (ИРИ) и глюкозу в крови. Повышение данных показателей свидетельствует об органическом характере болезни.
Для подтверждения панкреатической этиологии заболевания проводят тесты на чувствительность к толбутамиду и лейцину. При положительных результатах функциональных проб показано УЗИ, сцинтиграфия и МРТ поджелудочной железы. При вторичном гиперинсулинизме для исключения новообразований других органов выполняют УЗИ брюшной полости, МРТ головного мозга. Дифференциальная диагностика гипогликемической болезни проводится с синдромом Золлингера-Эллисона, началом развития сахарного диабета 2 типа, неврологическими (эпилепсия, новообразования головного мозга) и психическими (неврозоподобные состояния, психоз) заболеваниями.
Лечение гиперинсулинизма
Тактика лечения зависит от причины возникновения гиперинсулинемии. При органическом генезе показано хирургическое лечение: частичная резекция поджелудочной железы или тотальная панкреатэктомия, энуклеация новообразования. Объем оперативного вмешательства определяется местоположением и размерами опухоли. После операции обычно отмечается транзиторная гипергликемия, требующая медикаментозной коррекции и диеты с пониженным содержанием углеводов. Нормализация показателей наступает через месяц после вмешательства. При неоперабельных опухолях проводят паллиативную терапию, направленную на профилактику гипогликемии. При злокачественных новообразованиях дополнительно показана химиотерапия.
Функциональный гиперинсулинизм в первую очередь требует лечения основного заболевания, вызвавшего повышенную продукцию инсулина. Всем больным назначается сбалансированная диета с умеренным снижением потребления углеводов (100-150 гр. в сутки). Отдается предпочтение сложным углеводам (ржаные хлебцы, макароны из твердых сортов пшеницы, цельнозерновые крупы, орехи). Питание должно быть дробным, 5-6 раз в день. В связи с тем, что периодические приступы вызывают у пациентов развитие панических состояний, рекомендована консультация психолога. При развитии гипогликемического приступа показано употребление легкоусвояемых углеводов (сладкий чай, конфета, белый хлеб). При отсутствии сознания необходимо внутривенное введение 40 % раствора глюкозы. При судорогах и выраженном психомоторном возбуждении показаны инъекции транквилизаторов и седативных препаратов. Лечение тяжелых приступов гиперинсулинизма с развитием комы осуществляют в условиях реанимационного отделения с проведением дезинтоксикационной инфузионной терапии, введением глюкокортикоидов и адреналина.
Прогноз и профилактика
Профилактика гипогликемической болезни включает в себя сбалансированное питание с интервалом в 2-3 часа, употребление достаточного количества питьевой воды, отказ от вредных привычек, а также контроль уровня глюкозы. Для поддержания и улучшения обменных процессов в организме рекомендованы умеренные физические нагрузки с соблюдением режима питания. Прогноз при гиперинсулинизме зависит от стадии заболевания и причин, вызывавших инсулинемию. Удаление доброкачественных новообразований в 90% случаев обеспечивают выздоровление. Неоперабельные и злокачественные опухоли вызывают необратимые неврологические изменения и требуют постоянного контроля за состоянием пациента. Лечение основного заболевания при функциональном характере гиперинсулинемии приводит к регрессии симптомов и последующему выздоровлению.